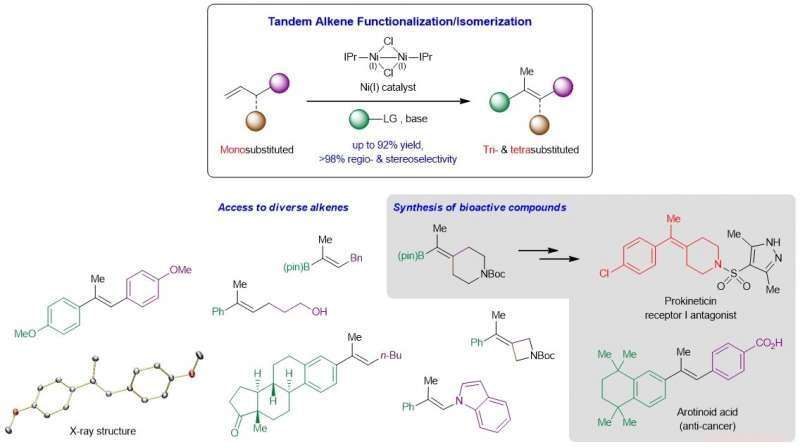
 p Esquema que mostra o desenvolvimento de um novo sistema catalisado por Ni que converte olefinas monossubstituídas baratas e prontamente disponíveis em análogos tri- e tetrassubstituídos de alto valor, e sua aplicação à síntese de compostos bioativos complexos. Crédito: Catálise Natural / Universidade Nacional de Singapura
p Esquema que mostra o desenvolvimento de um novo sistema catalisado por Ni que converte olefinas monossubstituídas baratas e prontamente disponíveis em análogos tri- e tetrassubstituídos de alto valor, e sua aplicação à síntese de compostos bioativos complexos. Crédito: Catálise Natural / Universidade Nacional de Singapura
p Os químicos da NUS desenvolveram uma nova maneira de acessar alcenos tri e tetrassubstituídos valiosos por meio de um processo em tandem catalisado por níquel envolvendo uma reação de Heck seguida pela migração da ligação dupla carbono-carbono (C =C). p O desenvolvimento de métodos confiáveis que proporcionam alcenos acíclicos tri- e tetrassubstituídos estereoquimicamente definidos é um objetivo de longa data na síntese orgânica. Essas ligações C =C altamente substituídas geralmente residem em inúmeras moléculas de interesse, incluindo materiais orgânicos e entidades biologicamente ativas, e são intermediários-chave para derivatização posterior para um espectro mais amplo de produtos de alto valor. As reações existentes que convertem compostos de carbonil ou ligações insaturadas de carbono-carbono em olefinas tri e tetrassubstituídas frequentemente envolvem longas rotas sintéticas, exibem compatibilidade limitada de grupo funcional, sofrem de controle insatisfatório de regio- ou estereosseletividade, e / ou não são suficientemente gerais. Uma complicação surge da pequena diferença de energia entre o
cis e
trans isômeros desses alquenos altamente substituídos, o que aumenta a dificuldade de geração desses compostos em alta estereosseletividade.
p Uma equipe de pesquisa liderada pelo Prof Koh Ming Joo, do Departamento de Química, Universidade Nacional de Cingapura, em colaboração com o Prof Osvaldo Gutierrez, da Universidade de Maryland, concebeu uma estratégia em tandem que mescla a reação de Heck regiocontrolada e a migração da ligação C =C estereocontrolada em uma única etapa (ver Figura). Estudos mecanísticos e computacionais mostraram que a reação prossegue por uma via não radical, e que tanto a base alcóxido de tamanho considerável como
N -ligando carbeno heterocíclico (NHC) são cruciais para o processo catalítico.
p Prof Koh disse, "Nossa incursão inicial nesta área de pesquisa foi perguntar hipoteticamente como podemos transformar α-olefinas monossubstituídas, uma classe altamente abundante de produtos químicos como matéria-prima, para os análogos trissubstituídos e tetrassubstituídos mais valiosos, mas difíceis de sintetizar, em um único processo. Acontece que a solução para isso foi projetar uma reação em tandem que primeiro reage com o substrato monossubstituído, em seguida, isomeriza-o ao produto desejado. Um controle bem orquestrado de regio- e estereosseletividade era fundamental, o que nos levou a descobrir a eficácia única dos catalisadores de níquel ligados a NHC. "
p "Esperamos que nossa nova metodologia aprimore a maneira como muitas moléculas bioativas são sintetizadas, e servir como um projeto para o projeto de transformações catalíticas em tandem para construir blocos de construção importantes a partir de materiais não preciosos, "acrescentou o Prof Koh.
p A equipe de pesquisa planeja explorar os insights obtidos neste trabalho para desenvolver novas transformações em tandem para facilitar a síntese química fina.
