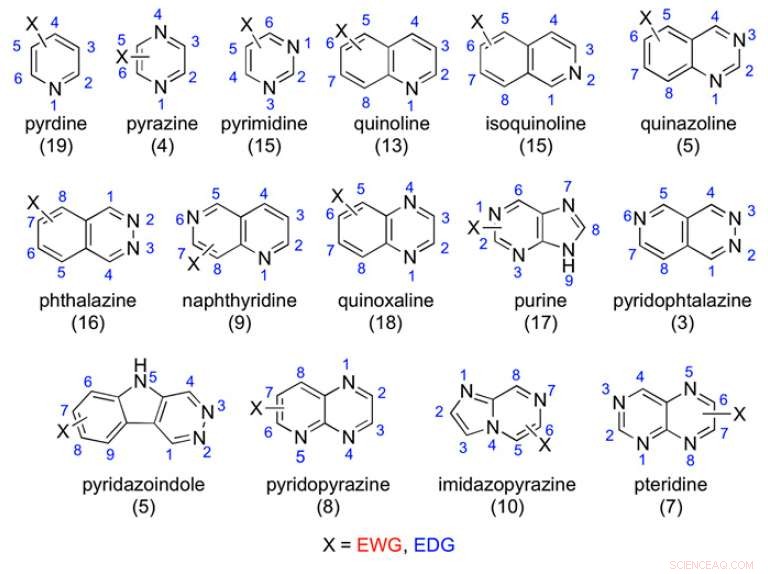
Exemplos de andaimes aza-aromáticos estudados:o número de compostos testados é relatado entre parênteses. Crédito:(c) Proceedings of the National Academy of Sciences (2017). DOI:10.1073 / pnas.1618881114
(Phys.org) - O projeto da droga envolve tentativa e erro guiada. A forma como o corpo metaboliza um determinado medicamento é importante para determinar a eficácia do medicamento. Tem havido muitos estudos para entender como os xenobióticos interagem com o citocromo P450s, uma importante classe de enzimas no metabolismo de drogas, mas pouca pesquisa foi feita para entender o metabolismo da aldeído oxidase (AOX). AOX, localizado no fígado, desempenha um papel importante no metabolismo de drogas; Contudo, muitos medicamentos em potencial acabam falhando durante os testes em estágio final por causa de sua interação com AOX.
Para entender melhor a relação estrutura-metabolismo entre grupos funcionais e AOX, bem como para estabelecer diretrizes gerais para o metabolismo de drogas não citocromo P450, pesquisadores da Universidade de Perguia, na Itália, realizaram testes em 198 compostos com estruturas aza-aromáticas para ver quais eram oxidados por AOX. Além disso, eles testaram 75 suportes de amida para determinar quais foram hidrolisados. Eles descobriram que fatores eletrônicos, bem como impedimento estérico, afetaram a orientação da molécula no sítio ativo MoCo, que determinou se o composto foi metabolizado por AOX. Seu trabalho aparece no Proceedings of the National Academy of Sciences .
AOX é uma enzima localizada no fígado que tende a oxidar compostos aza-aromáticos como um metabólito da fase I. Estudos têm mostrado que AOX ativa o carbono não substituído orto ao nitrogênio no heterociclo aza. Por ser o carbono mais eletropositivo do anel aromático, a densidade de elétrons provavelmente desempenha um papel na ativação de AOX. Mas esses estudos, bem como outros que examinam o metabolismo AOX, foram baseados em um pequeno número de moléculas que não permite a dedução de um padrão geral para a relação estrutura-metabolismo.
No estudo atual, Lepri et al. testou 198 compostos aza-aromáticos para ver se eles foram oxidados por AOX. Cada um deles tinha estruturas aza-aromáticas típicas com variações nos substituintes retiradores e doadores de elétrons. Eles adquiriram ou fizeram este catálogo de compostos e então conduziram estudos de metabolismo in vitro usando citosol de fígado humano.
Cálculos DFT foram usados para elucidar os efeitos da densidade eletrônica para a atividade AOX. O local do metabolismo no composto aromático tendeu a corresponder ao carbono não substituído mais eletro-positivo, como esperado. Adicionalmente, estudos computacionais foram usados para conduzir a análise de docking dos compostos no sítio ativo de AOX.
Os autores encontraram algumas tendências para o local do metabolismo; Contudo, essas tendências são complicadas por vários fatores. O andaime de piridina foi o único que, como uma classe de andaime, não era suscetível ao metabolismo AOX. Os outros grupos dependiam fortemente da densidade de elétrons em carbonos particulares ou, como os autores encontraram com compostos como quinoxalinas e certos compostos bicíclicos, o impedimento estérico no sítio ativo impediu o metabolismo de AOX.
Lepri et al. também testou 73 compostos de amida para ver se AOX hidrolisou a ligação amida. Em geral, se houvesse um grupo de retirada de elétrons na posição orto na analina, então o AOX não o oxidou. Se houvesse um grupo doador de elétrons, então aconteceu. As versões meta e para dos grupos de doação e retirada de elétrons não foram suscetíveis ao metabolismo de AOX.
Os efeitos da exposição foram um componente importante para determinar se um composto foi metabolizado por AOX. Isso tem a ver com a orientação da molécula em direção ao centro MoCo no sítio ativo AOX. Certos grupos volumosos resultaram em nenhuma atividade onde uma era esperada com base em estudos computacionais. Adicionalmente, a hidrofobicidade também afetou a forma como o composto interagiu com o sítio ativo. Quando o carbono reativo é exposto ao centro de MoCo, então o composto é facilmente metabolizado. Mas, quando a porção não reativa do composto é orientada em direção ao centro de MoCo, então, é menos provável que o composto seja oxidado ou hidrolisado.
Os autores apontam que a partir desses experimentos "emerge que não é nada simples prever se um composto é um substrato de AOX ou não." A dificuldade está em entender a reatividade do carbono eletrofílico no composto, bem como como esse composto específico se orientará no sítio ativo da enzima. Contudo, este estudo fornece um ponto de partida para estudos adicionais e técnicas de modelagem mais sofisticadas.
© 2017 Phys.org