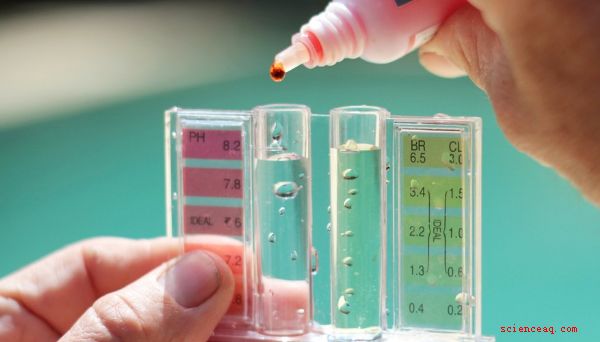
O pH de uma solução é uma medida da concentração de íons hidrogênio. O termo em si representa vagamente o "poder do hidrogênio" e é o logaritmo negativo da concentração real de íons hidrogênio. Isso significa que a concentração de íons hidrogênio diminui com o aumento do pH e que a diferença de uma unidade de pH significa uma variação de dez vezes na concentração de íons hidrogênio. O valor do pH pode variar de 0 a 14. Soluções com pH entre 0 e 7 são ácidas, enquanto aquelas com pH entre 7 e 14 são básicas. A água destilada pura deve ser neutra com um pH de 7, mas como absorve o dióxido de carbono da atmosfera, na verdade é levemente ácida com um pH de 5,8.
TL; DR (muito longo; não leu)
O pH da água destilada imediatamente após a destilação é 7, mas poucas horas após a destilação absorve o dióxido de carbono da atmosfera e se torna ácido com um pH de 5,8.
Ácidos e bases
< Faz sentido medir o pH em soluções de água; líquidos como óleo mineral ou aguarrás não têm pH. Na teoria de ácidos e bases de Bronsted-Lowry, um ácido é um composto que libera prótons livres na água e uma base é aquela que aceita prótons. Um próton não é senão o núcleo de um átomo de hidrogênio. Ácidos fortes, como o ácido clorídrico (HCl), diminuem drasticamente o pH de uma solução, enquanto bases fortes, como o hidróxido de sódio (NaOH), aumentam drasticamente. Ácidos e bases se neutralizam em solução e se combinam para formar um sal. Por exemplo, se você mistura HCl com NaOH em solução, obtém NaCl, que é sal de mesa.
Água destilada deve ter pH neutro
O processo de destilação envolve a fervura da água, permitindo a condensação do vapor em um tubo e coletando a condensação em um recipiente. Pode haver muitas substâncias dissolvidas na água, e algumas delas podem vaporizar junto com a água, mas sais e outros solutos sólidos são deixados para trás. Técnicas sofisticadas de destilação podem eliminar até os solutos voláteis, e se você empregar um desses, o condensado coletado deve estar livre de quaisquer solutos, e você esperaria que o pH fosse 7. Se você medir o pH imediatamente após a destilação, provavelmente é isso que você encontrará, mas logo muda.
A água pura é levemente ácida
O pH da água pura é de cerca de 5,8, o que a torna ácida. O motivo é que a água absorve o dióxido de carbono e continua a fazê-lo até entrar em equilíbrio com a atmosfera. Em solução, o dióxido de carbono reage com a água para produzir ácido carbônico, que, por sua vez, libera íons hidrônio na solução - o que equivale a liberar íons livres de hidrogênio. Demora cerca de duas horas para uma amostra de água destilada absorver todo o dióxido de carbono que puder da atmosfera e atingir seu pH final.