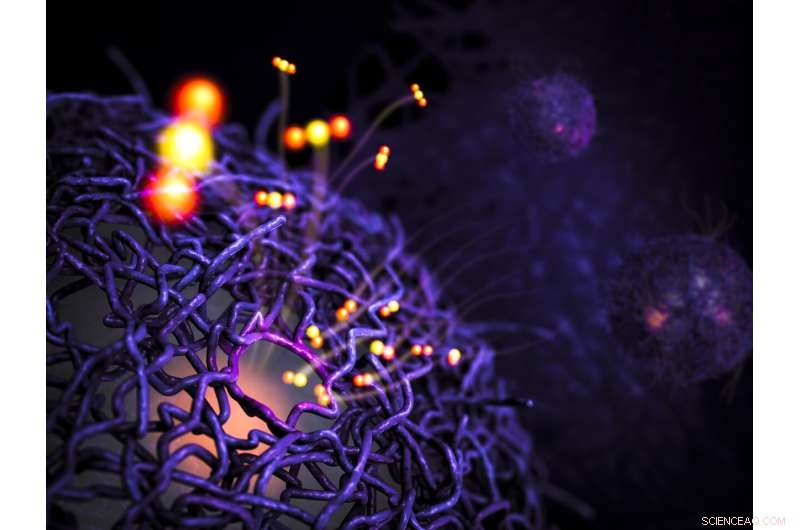
Os cientistas inventaram um catalisador semelhante a uma enzima feito de polímeros macios (roxo) e um núcleo duro de paládio (rosa). Quando aquecido, o paládio converte quimicamente moléculas de oxigênio e monóxido de carbono (amarelo e laranja) em dióxido de carbono (CO2). A reação para quando os polímeros estão saturados com dióxido de carbono, uma estratégia usada por enzimas vivas. A pesquisa está em andamento para desenvolver catalisadores que convertem gás natural em metanol em baixas temperaturas. Crédito:Gregory Stewart / SLAC National Accelerator Laboratory
Todos os organismos vivos dependem de enzimas - moléculas que aceleram as reações bioquímicas essenciais para a vida.
Os cientistas passaram décadas tentando criar enzimas artificiais capazes de produzir produtos químicos e combustíveis importantes em escala industrial, com desempenho rivalizando com seus equivalentes naturais.
Pesquisadores da Universidade de Stanford e do Laboratório Nacional de Aceleração SLAC desenvolveram um catalisador sintético que produz produtos químicos da mesma forma que as enzimas nos organismos vivos. Em um estudo publicado na edição de 5 de agosto da Catálise Natural , os pesquisadores afirmam que sua descoberta pode levar a catalisadores industriais capazes de produzir metanol usando menos energia e a um custo menor. O metanol tem uma variedade de aplicações, e há uma demanda crescente por seu uso como combustível com emissões menores do que a gasolina convencional.
"Nós nos inspiramos na natureza, "disse o autor sênior Matteo Cargnello, professor assistente de engenharia química em Stanford. "Queríamos imitar a função das enzimas naturais em laboratório usando catalisadores artificiais para fazer compostos úteis."
Para o experimento, os pesquisadores projetaram um catalisador feito de nanocristais de paládio, um metal precioso, incorporado em camadas de polímeros porosos adaptados com propriedades catalíticas especiais. A maioria das enzimas protéicas encontradas na natureza também contém vestígios de metais, como zinco e ferro, embutidos em seu núcleo.
Os pesquisadores foram capazes de observar traços de paládio em seus catalisadores com imagens microscópicas eletrônicas do co-autor Andrew Herzing, do Instituto Nacional de Padrões e Tecnologia.
Reação do modelo
"Nós nos concentramos em um modelo de reação química:converter monóxido de carbono tóxico e oxigênio em dióxido de carbono (CO2), "disse o estudante de doutorado Andrew Riscoe, autor principal do estudo. "Nosso objetivo era ver se o catalisador artificial funcionaria como uma enzima, acelerando a reação e controlando a forma como o CO2 é produzido."
Descobrir, Riscoe colocou o catalisador em um tubo de reator com um fluxo contínuo de monóxido de carbono e gás oxigênio. Quando o tubo foi aquecido a cerca de 150 graus Celsius (302 graus Fahrenheit), o catalisador começou a gerar o produto desejado, dióxido de carbono.
Os cientistas inventaram um catalisador semelhante a uma enzima feito de polímeros macios (roxo) e um núcleo duro de paládio (rosa). Quando aquecido, o paládio converte quimicamente moléculas de oxigênio e monóxido de carbono (amarelo e laranja) em dióxido de carbono (CO2). A reação para quando os polímeros estão saturados com dióxido de carbono, uma estratégia usada por enzimas vivas. A pesquisa está em andamento para desenvolver catalisadores que convertem gás natural em metanol em baixas temperaturas. Crédito:Gregory Stewart / SLAC National Accelerator Laboratory
Raios-X de alta energia do Stanford Synchrotron Radiation Lightsource (SSRL) no SLAC revelaram que o catalisador tinha características semelhantes às observadas nas enzimas:os nanocristais de paládio dentro do catalisador estavam continuamente reagindo com oxigênio e monóxido de carbono para produzir dióxido de carbono. E algumas das moléculas de dióxido de carbono recém-formadas ficaram presas nas camadas externas do polímero ao escapar dos nanocristais.
"Os raios X mostraram que, uma vez que as camadas de polímero foram preenchidas com CO2, a reação parou, "disse Cargnello, uma afiliada da Stanford Natural Gas Initiative (NGI). "Isso é importante, porque é a mesma estratégia usada pelas enzimas. Quando uma enzima produz muito de um produto, para de funcionar, porque o produto não é mais necessário. Mostramos que também podemos regular a produção de CO2 controlando a composição química das camadas de polímero. Esta abordagem pode impactar muitas áreas da catálise. "
A imagem de raios-X foi realizada pelos co-autores do estudo Alexey Boubnov, um estudante de pós-doutorado em Stanford, e os cientistas do SLAC Simon Bare e Adam Hoffman.
Fazendo metanol
Com o sucesso do experimento de dióxido de carbono, Cargnello e seus colegas voltaram sua atenção para a conversão de metano, o principal ingrediente do gás natural, em metanol, um produto químico amplamente utilizado em têxteis, plásticos e tintas. O metanol também foi apontado como um método mais barato, alternativa mais limpa para o combustível a gasolina.
"A capacidade de converter metano em metanol em baixas temperaturas é considerada um santo graal da catálise, "Cargnello disse." Nosso objetivo de longo prazo é construir um catalisador que se comporte como o metano monooxogenase, uma enzima natural que certos micróbios usam para metabolizar o metano. "
A maior parte do metanol hoje é produzida em um processo de duas etapas que envolve o aquecimento do gás natural a temperaturas de cerca de 1, 000 C (1, 800 F). Mas este processo de uso intensivo de energia emite uma grande quantidade de dióxido de carbono, um potente gás de efeito estufa que contribui para a mudança climática global.
"Um catalisador artificial que converte diretamente metano em metanol exigiria temperaturas muito mais baixas e emitiria muito menos CO2, "Riscoe explicou." Idealmente, também poderíamos controlar os produtos da reação projetando camadas de polímero que prendem o metanol antes de queimar. "
Enzimas futuras
"Nesse trabalho, demonstramos que podemos preparar materiais híbridos feitos de polímeros e nanocristais metálicos que possuem certas características típicas de atividade enzimática, "disse Cargnello, que também é afiliado ao SUNCAT Center for Interface Science and Catalysis de Stanford. "A parte empolgante é que podemos aplicar esses materiais a muitos sistemas, nos ajudando a entender melhor os detalhes do processo catalítico e nos levando um passo mais perto das enzimas artificiais. "