
Pela primeira vez, os cientistas detectaram a maquinaria celular que forma uma molécula vital em processo de evolução. Uma enzima chave que as plantas usam para fazer tirosina, um aminoácido necessário para a vida, foi pensado para ser conservado em todo o reino vegetal, mas os cientistas descobriram que sofreu uma mutação para outra forma de leguminosas. Em tomates cereja, a forma canônica da enzima domina, o amendoim pode mudar de golpe e algumas variedades de soja (grãos granulosos à direita) perderam a forma canônica. Crédito:Jez Lab
Porque as plantas não podem se levantar e fugir, eles tiveram que ser inteligentes em vez disso. Eles são os químicos do mundo vivo, produzindo centenas de milhares de pequenas moléculas que usam como protetores solares, para envenenar comedores de plantas, para cheirar o ar, para colorir flores, e para muitos outros negócios secretos vegetativos.
Historicamente, esses produtos químicos, chamados de "metabólitos secundários, "foram distinguidos de" metabólitos primários, "que são os blocos de construção das proteínas, gorduras, açúcares e DNA. Metabólitos secundários suavizam o modo de vida, mas os metabólitos primários são essenciais, e o fracasso em fazê-los correta e eficientemente é fatal.
Acredita-se que o metabolismo secundário tenha evoluído para ajudar os ancestrais das plantas a lidar com a vida em terra seca, em vez de nos oceanos mais hospitaleiros. A ideia é que os genes para enzimas nas linhas de montagem molecular do metabolismo primário foram duplicados. As duplicatas eram mais tolerantes a mutações que poderiam ter desestabilizado as vias primárias porque os originais ainda estavam em funcionamento. Com as restrições evolutivas assim relaxadas, a maquinaria sintética foi capaz de acumular mutações suficientes para fazer uma nova química.
Metabolismo primário, Contudo, é amplamente conservado, o que significa que ele permanece inalterado em muitos grupos diferentes de organismos porque foi ajustado para operar correta e eficientemente e porque seus produtos são necessários para a vida. Ou pelo menos é o que dizem os livros.
Mas agora uma equipe colaborativa de cientistas detectou o metabolismo primário em evolução. Em um estudo abrangente de uma linha de montagem de metabolismo primário em fábricas, eles descobriram uma enzima chave evoluindo de uma forma canônica possuída pela maioria das plantas, através de formas não canônicas em tomates, a uma forma de acionamento de interruptor encontrada em amendoim, e, finalmente, comprometendo-se com a nova forma em algumas variedades de soja.
Esta façanha, comparável a puxar a toalha de mesa debaixo da louça sem quebrar nenhuma delas, é descrito na edição de 26 de junho de Nature Chemical Biology . É o trabalho de uma colaboração entre o laboratório Maeda da Universidade de Wisconsin, que tem um interesse de longa data nesta via bioquímica, e o laboratório Jez na Washington University em St. Louis, que cristalizou a enzima da soja para revelar como a natureza mudou o funcionamento da proteína.
“O trabalho captura plantas em processo de construção de uma via que liga o metabolismo primário ao secundário, "disse Joseph Jez, o Howard Hughes Medical Institute Professor no Departamento de Biologia em Artes e Ciências. "Estamos finalmente vendo como a evolução cria a máquina para fazer novas moléculas."
Também pode ter importância prática porque as antigas e as novas vias tornam o aminoácido tirosina, que é um precursor de muitos metabólitos secundários com atividade biológica e farmacêutica - tudo, da vitamina E aos opioides. Mas o antigo caminho produz apenas pequenas quantidades desses compostos, em parte porque eles devem competir por átomos de carbono com o processo ganancioso de fazer lignina, os polímeros resistentes que permitem que as plantas se erguam.
A descoberta do novo caminho para a produção de tirosina é muito menos restrita do que a anterior. Isso levanta a possibilidade de que o fluxo de carbono possa ser direcionado para longe da lignina, aumentar a produção de drogas ou nutrientes a níveis que permitiriam que fossem produzidos em quantidades comerciais.
Uma história de duas enzimas
A tirosina é feita em uma linha de montagem chamada via do shiquimato, uma via metabólica de sete etapas que as plantas usam para produzir os três aminoácidos que possuem anéis aromáticos. Animais (incluindo pessoas) perdem a capacidade de erguer essa linha de montagem no passado evolucionário. Porque não podemos fazer esses aminoácidos por conta própria e eles são essenciais para a vida, em vez disso, devemos obtê-los comendo plantas ou fungos.
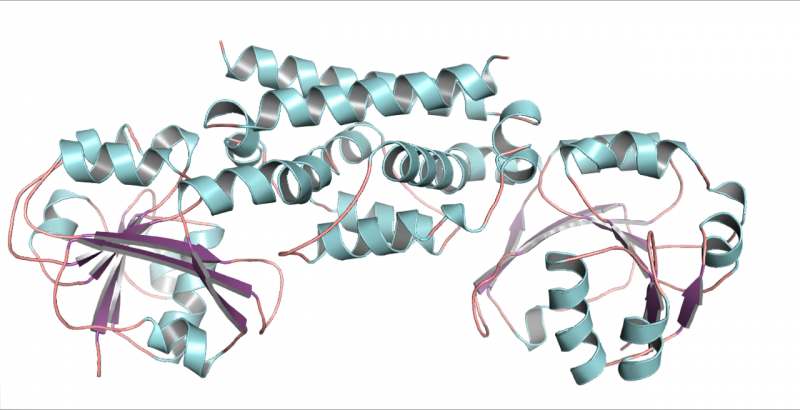
Uma estrutura tridimensional da enzima PDH da soja, uma leguminosa. Essa estrutura ajudou a mostrar que apenas uma mutação permitiu que as leguminosas desenvolvessem uma nova forma de produzir o aminoácido tirosina. Crédito:Craig Schenck
Esse anel aromático é importante, disse Jez, porque é uma estrutura distinta que pode absorver luz ou energia. Portanto, os aminoácidos aromáticos também são os precursores de muitos metabólitos secundários que captam a luz, transferir elétrons, ou flores coloridas. Além disso, os aminoácidos aromáticos também são precursores de substâncias químicas que envenenam outras plantas ou predadores de plantas e atraem polinizadores. Muitos medicamentos incluem um anel aromático, Jez comentou.
Na maioria das plantas, a via do shiquimato está no cloroplasto, a organela que faz o trabalho de converter a energia da luz solar em energia armazenada em ligações de carbono. Uma vez feito, Contudo, a tirosina pode ser exportada do citosol para incorporação ou conversão em outros compostos.
Na última etapa de um ramo da via, uma enzima chamada arogenato desidrogenase (ADH), catalisa uma reação que transforma o composto arogenado em tirosina. A enzima ADH é considerada "reguladora" porque é um gargalo na produção de tirosina. Deve competir pelo substrato de arogenato com o ramo da via do shiquimato que produz um aminoácido aromático diferente e é fortemente inibido pelo acúmulo de tirosina
A atividade de ADH é comum em plantas, mas, durante o estudo da via do shikimato, o laboratório de Maeda descobriu que as sequências de DNA que codificam o ADH em algumas plantas com flores eram significativamente diferentes das da maioria das plantas. Eles chamaram as enzimas produzidas por essas sequências de ADH não canônico. Então, em 2014, eles relataram que alguns legumes também produzem tirosina com uma enzima diferente, denominado pré-fenato desidrogenase (PDH).
O PDH difere do ADH de várias maneiras. É ativo fora do cloroplasto, ele atua no pré-fenato de substrato, em vez de no arogenato, por estar fora do cloroplasto, não precisa competir por seu substrato com outros ramos da via do shiquimato, e não é inibido por níveis crescentes de tirosina.
Por que existem duas linhas de montagem diferentes para a tirosina? Os cientistas acreditam que a enzima PDH evoluiu por meio de dois eventos de duplicação de genes e do acúmulo de mutações nas cópias "extras" do gene. O primeiro evento deu origem a ADHs não padronizados em algumas plantas com flores e o segundo ao PDH em um subconjunto de leguminosas. Mas por que isso aconteceu?
Essa não é uma pergunta que os cientistas podem responder, exceto em termos gerais, Jez disse. O que se destaca, Contudo, é que a via metabólica desenvolvida mais recentemente não é rigidamente regulamentada e pode produzir o produto em um ritmo frenético. Talvez os legumes precisassem desesperadamente de metabólitos secundários por algum motivo. É certamente suspeito que as leguminosas tenham uma ecologia bastante diferente das outras plantas, uma vez que vivem simbioticamente com bactérias fixadoras de nitrogênio.
Mexendo nos bits
Nesse ponto, os cientistas sabiam que a nova enzima, PDH, ligado a um substrato diferente da enzima original, ADH. Eles também sabiam que PDH, ao contrário do ADH, não se ligou à própria tirosina. Mas que mudanças na estrutura levaram a essas diferenças na atividade química?
Descobrir, Craig Schenck, um estudante de pós-graduação no laboratório Maeda, comparou as sequências de genes para a enzima ADH ou PDH em muitas plantas diferentes, cuidadosamente escolhidos para estar nos limites da transição de uma enzima para outra. Mas eles encontraram um problema. Havia diferenças suficientes no DNA que era difícil ver o que era relevante, Jez disse.
Encontrando Maeda em uma conferência, Jez se ofereceu para tentar cristalizar as novas enzimas para que sua estrutura pudesse ser reconstruída a partir de imagens de raios-X. Sua estudante de graduação Cynthia Holland foi capaz de cristalizar o PDH de soja e produzir imagens detalhadas de sua forma tridimensional.
"Depois de olhar para a estrutura, você pode ver que havia apenas duas diferenças em relação ao ADH típico encontrado na maioria das plantas e apenas uma das diferenças realmente mudava as coisas, "Disse Jez. Espantosamente essa diferença era um único aminoácido no sítio ativo da enzima. Nesse ponto, a asparagina havia substituído o ácido aspártico.
Schenck verificou novamente esse insight estrutural, lançando aquele aminoácido em formas mutantes da enzima. O mutante ADH revelou ter atividade PDH, e o mutante PDH tinha atividade ADH, exatamente como a equipe havia suspeitado.
"Essa diferença muda o substrato preferido da enzima e sua capacidade de ser inibida pelo feedback de tirosina, "Jez disse." E se você olhar para ele, é literalmente a diferença entre um átomo de nitrogênio ou um átomo de oxigênio. Nessas proteínas, que são compostos de quase trezentos aminoácidos ou quarenta e duzentos átomos, um átomo faz toda a diferença. Isso é simplesmente legal. "
O trabalho é importante porque demonstra que o metabolismo primário evolui. E porque mostra como a natureza rouba maquinários do metabolismo primário e os monta para formar novos metabólitos secundários. Eles fazem isso com muito mais sutileza do que os engenheiros genéticos ainda conseguem administrar.
"Quando queremos que uma planta faça uma nova molécula, "Jez disse, "adicionamos um gene e esperamos que ele se integre aos caminhos existentes. Ainda não sabemos como conectar prontamente a fiação entre o que inserimos e o que já está lá. Portanto, é interessante ver como a natureza planejou conectar a fiação e mudar as coisas sem quebrá-las. "