Cientistas associam a histona H1FOO específica do oócito à melhor geração de células iPS
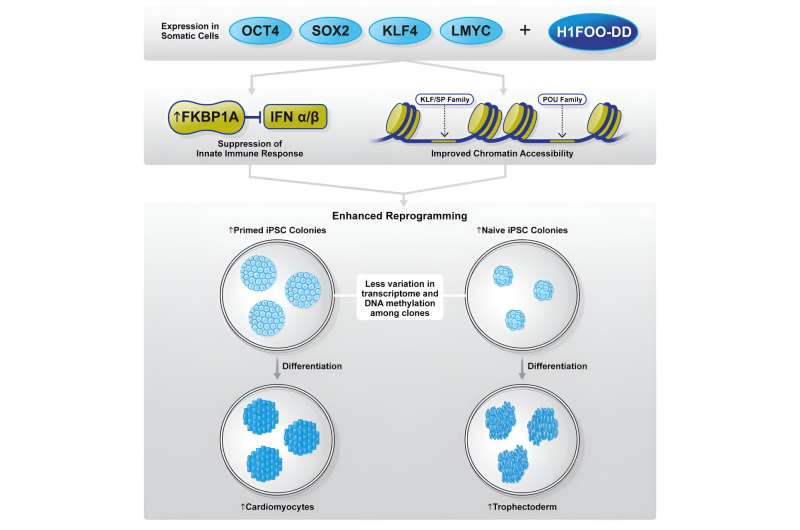 Crédito:Relatórios de células-tronco (2024). DOI:10.1016/j.stemcr.2024.04.005
Crédito:Relatórios de células-tronco (2024). DOI:10.1016/j.stemcr.2024.04.005
Uma equipe de pesquisa conjunta liderada pelo Dr. , H1FOO, no aumento da eficiência e homogeneidade da reprogramação para estados pluripotentes preparados e ingênuos. O estudo foi publicado em Stem Cell Reports .
