Novo estudo permite que cientistas testem terapias para doenças neurodegenerativas raras que afetam crianças pequenas
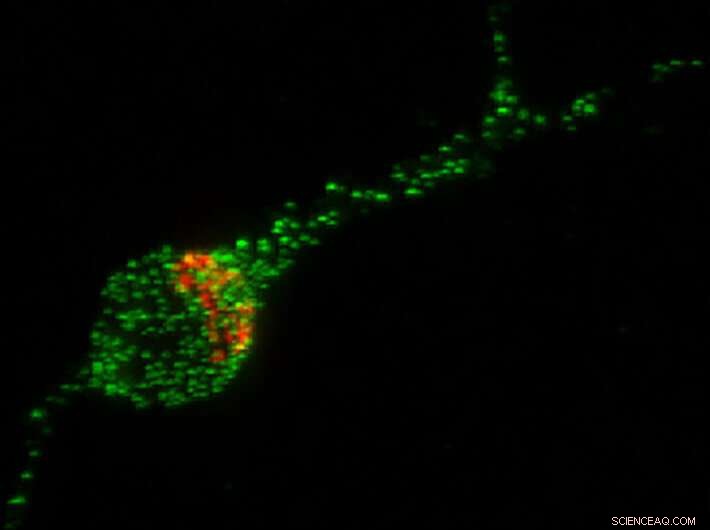
Nesta imagem de um neurônio derivado de células-tronco humanas, a proteína do gene Trk-fused (TFG) é mostrada em verde e o Aparelho de Golgi, a organela que ajuda a empacotar proteínas para transporte para o resto do corpo, é mostrado em vermelho. Crédito:Universidade de Wisconsin-Madison
Pela primeira vez, os cientistas poderão testar a terapêutica para um grupo de doenças neurodegenerativas raras que afetam bebês e crianças pequenas, graças a um novo modelo de pesquisa criado por cientistas da Universidade de Wisconsin-Madison. Seus resultados são publicados nos
Proceedings of the National Academy of Sciences .
As paraplegias espásticas hereditárias (HSPs) são um grupo de doenças neurodegenerativas causadas por mutações genéticas. Eles levam dezenas de milhares de crianças a desenvolver um aumento do tônus muscular em suas extremidades inferiores, causando fraqueza nas pernas e, finalmente, afetando sua capacidade de engatinhar ou andar.
"As crianças com seis meses de idade que têm essas mutações começam a mostrar sinais de doença", diz Anjon Audhya, professor do Departamento de Química Biomolecular da UW-Madison. "Entre dois e cinco anos de idade, essas crianças se tornam cadeirantes e, infelizmente, nunca poderão andar."
Audhya explica que muitos cientistas não pesquisaram as paraplegias espásticas porque não havia um bom modelo para estudar as origens da doença ou testar a terapêutica. Modelos anteriores de camundongos não funcionaram porque as vias neuronais que transportam informações relacionadas ao movimento por todo o corpo parecem ser muito diferentes daquelas em humanos, e os pesquisadores ainda não realizaram ensaios clínicos em humanos.
Audhya trabalhou com uma equipe interdisciplinar de pesquisadores da UW-Madison para estudar uma mutação específica que causa HSP em crianças pequenas. Eles então usaram o que aprenderam para criar um modelo melhor – em ratos.
A mutação que os pesquisadores escolheram funciona em uma proteína chamada gene Trk-fused, ou TFG. As proteínas TFG saudáveis trabalham dentro das células nervosas, ou neurônios, para transportar outras proteínas de uma parte da célula para outra. O trabalho de um neurônio é transportar mensagens na forma de sinais elétricos entre o cérebro e o resto do corpo.
As proteínas que dependem do TFG para seu transporte mantêm essas vias neuronais saudáveis, ajudando a gerenciar quais sinais elétricos o cérebro envia ao corpo e quais sinais inibir. Ao equilibrar os níveis certos de estimulação, os neurônios podem direcionar movimentos como contrair os músculos das pernas envolvidos na caminhada.
Em crianças pequenas com uma mutação no gene TFG, as proteínas neuronais não se movem com eficiência pelas células nervosas. Audhya diz que isso pode criar um desequilíbrio de estimulação elétrica que permite que uma abundância de sinais elétricos seja enviada para as extremidades inferiores, resultando em tônus muscular elevado. Com o tempo, o tônus muscular excessivo leva a uma perda da função motora.
"Você pode imaginar que se você esticar a perna com muita força e colocar toda a sua energia para flexionar esse músculo, é muito difícil movê-lo", diz Audhya, que também é o reitor associado sênior de pesquisa básica, biotecnologia e estudos de pós-graduação em Faculdade de Medicina e Saúde Pública da UW.
Procurando por um modelo viável, os pesquisadores recorreram aos ratos para ajudar essas crianças. A equipe usou a tecnologia de edição de genes CRISPR para criar em embriões de ratos as mutações que levam ao HSP. Isso lhes permitiu estudar como a doença progride desde o desenvolvimento inicial e monitorar a progressão dos sintomas após o nascimento.
Não apenas as vias neuronais dos ratos são mais próximas das dos humanos, mas os pesquisadores observaram que os sintomas se desenvolveram de forma semelhante em ratos aos observados em crianças com HSP. Também aconteceu em uma escala de tempo rápida o suficiente para que os cientistas pudessem testar facilmente a viabilidade de possíveis terapias.
"O exercício tem sido a única terapia que existe para esses pacientes, e isso é realmente insatisfatório", diz Audhya. "Acho que demos um grande salto em apenas ter um modelo onde você pode testar diferentes hipóteses. Isso é grande, da minha perspectiva."
Os detalhes intrincados envolvidos na química biomolecular podem parecer mundanos para alguns, mas a ciência básica como essa fascina Audhya. Não foi até que ele fez contato com pacientes que têm HSP, que ele entendeu completamente o impacto potencial que seu trabalho poderia ter.
"Estas são populações carentes. Uma empresa farmacêutica provavelmente não gastará grandes recursos para uma população afetada que é tão pequena. Em vez disso, eles vão se concentrar em doenças como Alzheimer e Parkinson", diz ele. "Então, eu senti que aqui está uma doença que é amplamente ignorada, subinvestida, e aqui está uma área em que podemos causar impacto".
Audhya disse que espera que este novo modelo inspire mais cientistas a estudar HSPs para melhorar a compreensão do desenvolvimento da doença e, eventualmente, melhorar o acesso a terapias que ajudarão as crianças que vivem com ela.
+ Explorar mais Mutações genéticas de pacientes com convulsão debilitante e distúrbio do movimento criadas em camundongos
