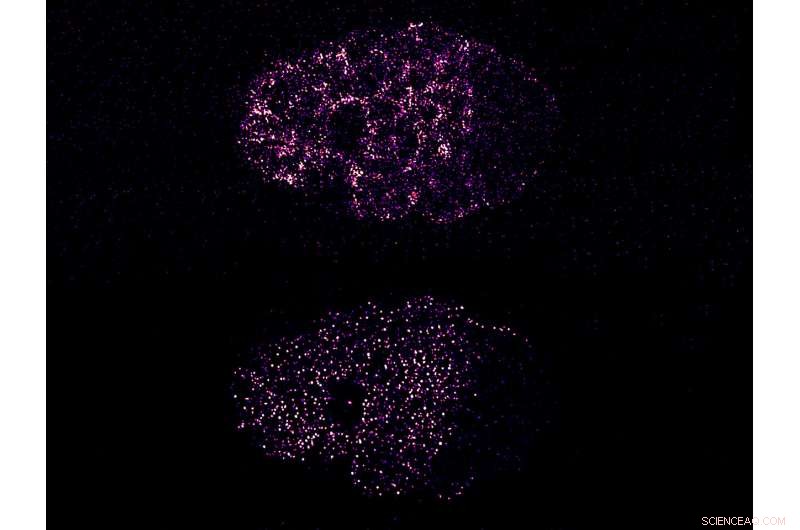
Figura:A contração conduz o agrupamento da proteína PAR para quebrar a simetria em um embrião de C. elegans. A imagem superior mostra a atividade contrátil da miosina cortical, que causa o agrupamento da proteína PAR-3 (imagem inferior). Tanto a miosina quanto o PAR-3 segregam no lado esquerdo do embrião, o pólo anterior. Isso quebra a distribuição simétrica anterior dessas proteínas e polariza a célula. Crédito:Instituto de Mecanobiologia, Cingapura
Uma equipe de pesquisadores do Instituto de Mecanobiologia, Cingapura (MBI) na Universidade Nacional de Cingapura, junto com colegas do Laboratório de Ciências da Vida Temasek e do Instituto de Biologia Molecular e Celular da A * STAR em Cingapura, descobriu um novo mecanismo para estabelecer a polaridade celular que depende do agrupamento de proteínas induzida por força de tensão. Este trabalho foi publicado em revista científica Nature Cell Biology em agosto de 2017.
Forças corticais induzem agrupamento de proteínas para polarização celular
As células biológicas são normalmente visualizadas como redondas (ou esféricas) em forma, com um núcleo centrado no meio, e outros componentes celulares espalhados por toda parte. Na realidade, cada tipo de célula exibe uma forma distinta, tamanho e composição. As representações de esferas simétricas são, em essência, uma simplificação excessiva que esconde o fato de que quase todas as células são assimétricas em sua composição, e que essa assimetria se desenvolve em etapas precisas e bem ordenadas.
Conhecida como polaridade celular, esta característica chave das células vê a separação dos componentes subcelulares em regiões distintas da célula. Se as células fossem simétricas, processos como a divisão e o movimento das células não ocorreriam corretamente, e os tecidos e órgãos seriam deformados e não funcionais. Apesar de ser parte integrante do desenvolvimento do organismo, os cientistas ainda não definiram totalmente os processos pelos quais as células se tornam polarizadas.
Uma maneira de visualizar a natureza assimétrica da composição celular é pensar sobre os componentes de um carro e como eles estão dispostos. Algumas partes do carro devem ser localizadas em um layout equilibrado, por exemplo, as rodas. Outros componentes precisam ser organizados em uma orientação específica para funcionar corretamente, ou seja, o banco do motorista deve estar localizado na frente dos bancos traseiros do passageiro. Finalmente, componentes como o motor podem estar localizados na parte dianteira ou traseira do carro, e, o que é mais importante, essa organização confere propriedades diferentes ao manuseio do carro. Do mesmo jeito, o arranjo dos componentes celulares pode ter efeitos drásticos na função celular.
Muitos dos estudos existentes sobre a polaridade celular foram realizados no verme nematóide C. elegans. No estágio de uma célula, o embrião se divide ao longo de um eixo frontal / posterior para gerar duas células-filhas de tamanhos diferentes, com uma célula maior na frente e uma célula menor atrás. Este eixo frontal / traseiro é estabelecido pelo movimento e segregação de um grupo de proteínas conhecidas como proteínas PAR (defeituosas de partição).
Essas proteínas PAR residem no córtex celular, uma camada dinâmica de filamentos de proteínas que fica logo dentro da membrana celular. Antes da polarização, as proteínas PAR são distribuídas por todo o córtex, onde eles se movem livremente. Durante a polarização, o córtex se contrai, e isso faz com que diferentes proteínas PAR se separem e se acumulem na parte frontal ou posterior da célula, quebrando assim sua organização anteriormente simétrica e estabelecendo a polaridade ao longo do eixo anterior / posterior. Contudo, o mecanismo pelo qual a atividade contrátil transporta e separa as proteínas PAR permanece obscuro.
Fluxo de tensão
A equipe de pesquisadores liderada pelo professor assistente Fumio Motegi, Investigador principal do MBI e do Laboratório de Ciências da Vida Temasek, procurou responder a esta pergunta observando o movimento de complexos de proteínas PAR marcados com fluorescência sob o microscópio em embriões vivos de C. elegans enquanto eles passavam por polarização. Usando técnicas avançadas de microscopia, eles descobriram que certas proteínas PAR montadas em clusters no início da polarização, e esses aglomerados aumentaram de tamanho à medida que a polarização progredia. Uma vez que a contração cortical parou, os clusters desmontados, com as proteínas se espalhando como um gradiente ao longo do eixo anterior / posterior.
Apesar dessas descobertas, os pesquisadores não observaram uma conexão direta entre as fibras contráteis e as proteínas PAR, e isso os levou a hipotetizar que um efeito indireto de contração era responsável pelo agrupamento. Ao interromper ou reforçar o córtex da actomoysina e observar o efeito na formação de aglomerados, eles descobriram que a principal força motriz do agrupamento PAR era a tensão cortical, que se desenvolveu à medida que o córtex se contraiu.
A partir disso, os pesquisadores foram capazes de propor um novo modelo que explica a segregação das proteínas PAR. Aqui, a contração do córtex da actomiosina leva a um aumento da tensão cortical, fazendo com que as proteínas PAR se agrupem em clusters. À medida que esses grandes aglomerados se movem lentamente, eles ficam presos no fluxo cortical geral e segregam em uma extremidade da célula, estabelecendo assim a polaridade. Esses grupos segregados de proteínas PAR atuam então como um arcabouço que medeia um acúmulo local de outras proteínas necessárias para o estabelecimento dos eixos dianteiro / traseiro ao longo do corpo.
O mecanismo descoberto neste estudo é um exemplo simples, mas elegante de como as células usam forças internas para mover e organizar seus componentes de proteína de forma precisa, maneira bem ordenada. Mais importante, o mecanismo acionado por força descrito permite que a célula estabeleça a polaridade sem desperdiçar energia, transportando ativamente proteínas ou componentes celulares contra um gradiente de concentração. Acredita-se que mecanismos semelhantes sejam usados para quebrar a simetria em outros organismos, incluindo humanos, e espera-se que esse novo conhecimento ajude os cientistas a entender como e por que a polaridade celular não é devidamente estabelecida em doenças como a fibrose cística e o câncer.