Os pesquisadores estendem o poder da edição de genes desenvolvendo uma nova classe de editores de base de DNA
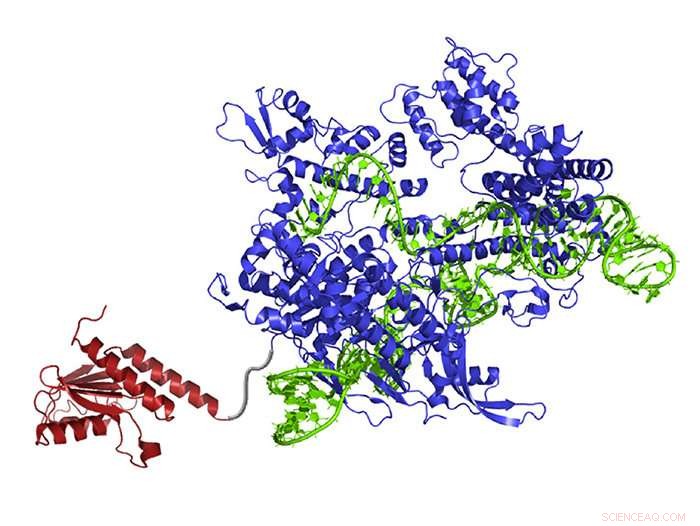 p Um editor de base de DNA recém-criado contém uma enzima de rearranjo de átomos (vermelha) que pode transformar adenina em inosina (lida e copiada como guanina), o RNA guia (verde) que direciona a molécula para o ponto certo, e Cas9 nickase (azul), que corta a fita oposta de DNA e induz a célula a trocar a base complementar. Crédito:Gaudelli et al./ Natureza 2017
p Um editor de base de DNA recém-criado contém uma enzima de rearranjo de átomos (vermelha) que pode transformar adenina em inosina (lida e copiada como guanina), o RNA guia (verde) que direciona a molécula para o ponto certo, e Cas9 nickase (azul), que corta a fita oposta de DNA e induz a célula a trocar a base complementar. Crédito:Gaudelli et al./ Natureza 2017
p Cientistas da Harvard University e do Broad Institute of MIT e Harvard desenvolveram uma nova classe de ferramenta de edição de genoma. Este novo "editor básico" pode reparar diretamente o tipo de alterações de uma única letra no genoma humano que respondem por aproximadamente metade das mutações pontuais associadas a doenças humanas. Essas mutações estão associadas a distúrbios que variam de cegueira genética a anemia falciforme, a distúrbios metabólicos a fibrose cística. p A equipe de pesquisa, liderado por David Liu, professor de química e biologia química na Universidade de Harvard, membro do instituto principal no Broad Institute, e um investigador do Howard Hughes Medical Institute (HHMI), desenvolveu uma máquina molecular que pode converter o par de bases de DNA A * T em G * C, sem cortar a dupla hélice, com alta eficiência e praticamente sem produtos indesejados. O desenvolvimento é uma adição importante ao crescente conjunto de ferramentas de edição de genoma.
p O novo sistema é descrito em um artigo publicado hoje em
Natureza . Além de Liu, o estudo foi liderado por Nicole Gaudelli, um pós-doutorado no laboratório de Liu; Alexis Komor, um ex-pós-doutorado no laboratório de Liu que agora é professor assistente na UCSD; a estudante de graduação Holly Rees; ex-alunos de pós-graduação Michael Packer e Ahmed Badran, e o ex-colega de pós-doutorado David Bryson.
p O novo sistema, apelidado de Editor de base de adenina, ou ABE, pode ser programado para ter como alvo um par de bases específico em um genoma usando um RNA guia e uma forma modificada de CRISPR-Cas9. Ele age reorganizando os átomos em uma adenina alvo (A) - uma das quatro bases que compõem o DNA - para se assemelhar à guanina (G), e, em seguida, enganar as células para que fixem a outra fita de DNA para completar a conversão do par de bases, tornando a mudança permanente. Como resultado, o que costumava ser um par de bases A * T torna-se um par de bases G * C.
p Não apenas o sistema é muito eficiente em comparação com outras técnicas de edição de genoma para corrigir mutações pontuais, mas praticamente não há subprodutos detectáveis, como inserções aleatórias, exclusões, translocações, ou outras conversões base a base.
p Fazer essa mudança específica é importante porque aproximadamente metade dos 32, 000 mutações pontuais associadas a doenças já identificadas pelos pesquisadores são uma mudança de G * C para A * T.
p "Desenvolvemos um novo editor de base - uma máquina molecular - que é programável, irreversível, eficiente, e a maneira limpa pode corrigir essas mutações no genoma das células vivas, "disse Liu, que também é o professor Richard Merkin e diretor do Instituto Merkin de Tecnologias Transformativas em Saúde da Broad. "Quando direcionado para determinados locais no DNA genômico humano, essa conversão reverte a mutação associada a uma doença específica. "
p ABE se junta a outros sistemas de edição de base pioneiros no laboratório de Liu, como BE3 e sua variante melhorada, BE4. Usando esses editores básicos, os pesquisadores agora podem corrigir todas as chamadas mutações de "transição" - C para T, T para C, A a G, ou G para A - que juntos respondem por quase dois terços de todas as mutações pontuais causadoras de doenças, incluindo muitos que causam doenças graves para as quais não há tratamento atual. É necessária pesquisa adicional, Liu observa, para permitir que ABE almeje o máximo possível do genoma, como Liu e seus alunos alcançaram anteriormente por meio de variantes de engenharia do BE3.
p O desenvolvimento do novo editor de base começou quando a equipe começou um esforço de um ano para desenvolver uma nova enzima que pudesse converter adenina em inosina (I), um nucleotídeo que se comporta de forma semelhante ao G durante a síntese de DNA ou RNA. O projeto, liderado por Gaudelli, no final das contas resultou em alto desempenho, ABEs de sétima geração.
p "O principal desafio para mim durante o desenvolvimento do ABE foi superar o obstáculo psicológico de se o ABE poderia ou não ir do conceito à realidade, uma vez que o componente principal do editor não existia naturalmente e teve que ser evoluído em nosso laboratório, "disse Gaudelli." Era importante manter a fé de que não poderíamos apenas sonhar com tal máquina molecular, mas também construí-lo. "
p Para demonstrar o potencial da ABE, Liu e colegas primeiro usaram ABE para corrigir diretamente uma mutação que causa hemocromatose hereditária (HHC) em células humanas.
p Eles também usaram ABE para instalar uma mutação em células humanas que suprime uma doença, recriando a chamada "mutação britânica" encontrada em indivíduos saudáveis que normalmente desenvolveriam doenças do sangue como a anemia falciforme, mas em vez disso têm uma mutação que faz com que os genes da hemoglobina fetal permaneçam ativos após o nascimento, protegendo-os das doenças do sangue.
p Embora o desenvolvimento do ABE seja um passo empolgante na edição de base, mais trabalho resta antes que a edição de base possa ser usada para tratar pacientes com doenças genéticas, incluindo testes de segurança, eficácia, e efeitos colaterais.
p "Criar uma máquina que faz a mudança genética de que você precisa para tratar uma doença é um passo importante à frente, mas é apenas uma parte do que é necessário para tratar um paciente, "disse Liu." Ainda temos que entregar essa máquina, temos que testar sua segurança, temos que avaliar seus efeitos benéficos em animais e pacientes e pesá-los contra quaisquer efeitos colaterais - precisamos fazer muito mais coisas. "
p "Mas ter a máquina é um bom começo."
