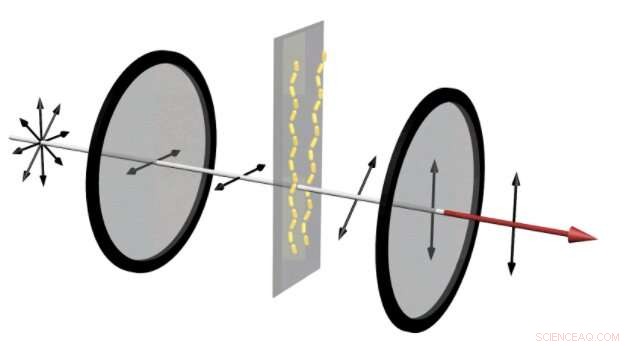
Em um dispositivo que pode revelar se as proteínas amiloides estão se montando em cadeias, luz não polarizada entra em um polarizador horizontal. Isso só permite que as ondas oscilando na direção horizontal passem. Então, se as proteínas amiloides montaram os nanobastões de ouro em cadeias, luz vermelha fica torcida, mudando o ângulo de sua polarização. Então, quando passa pelo polarizador vertical, a parte da luz que oscila na direção vertical passa. Isso resulta em um forte sinal vermelho que pode ser visto a olho nu. Crédito:Jun Lu, Jilin University e University of Michigan
Uma nova abordagem faz faróis semelhantes a cristal líquido a partir de proteínas amilóides prejudiciais presentes em doenças como o diabetes tipo II.
Em uma nova técnica de triagem de drogas que depende de nanobastões de ouro para torcer a luz, um brilho vermelho pode sinalizar o fracasso de um medicamento projetado para tratar doenças "amilóides", como diabetes tipo II e câncer de pâncreas.
A técnica foi desenvolvida por pesquisadores da Universidade de Michigan, Universidade Jilin na China, e a Universidade Federal de São Carlos no Brasil. Ele aproveita uma propriedade chamada "quiralidade, "que é encontrado em nanoestruturas, moléculas biológicas como proteínas, e ondas de luz. Um objeto quiral não pode ser sobreposto em sua imagem espelhada, como uma mão esquerda e direita, ou hélices que se torcem em direções diferentes.
Os pesquisadores foram capazes de tirar proveito da quiralidade de um marcador de proteína para essas doenças, chamados polipeptídeos de ilhotas amilóides. Essas proteínas se ligam em cadeias torcidas e se acumulam nos tecidos. As proteínas amilóides que formam fibras em forma de saca-rolhas também desempenham um papel nas doenças de Parkinson e Huntington.
Na nova abordagem, nanobastões de ouro são revestidos com proteínas prejudiciais, que formam longas fibras em forma de mola com três nanobastões por volta. Essas estruturas aparecem em vermelho brilhante quando vistas entre dois polarizadores de ângulos opostos, ou filtros de luz, porque sua torção, formas quirais podem transformar a polarização da luz.
"A forte torção da luz permite que os resultados do rastreamento de drogas sejam vistos a olho nu, em vez de usar instrumentos complicados, "disse Kun Liu, um professor de química na Universidade de Jilin e co-autor correspondente em um artigo recém-publicado em Ciência .

No dispositivo à esquerda, nanobastões de ouro permitem uma pequena quantidade de luz através dos dois polarizadores cruzados. Isso é semelhante ao sinal que mostra que uma droga projetada para prevenir a formação de placas amilóides está funcionando. Contudo, quando as proteínas amiloides montam os nanobastões de ouro em hélices, uma luz vermelha clara é visível através dos polarizadores, revelando que um medicamento falhou. Crédito:Jun Lu, Jilin University e University of Michigan
Os nanobastões - cada um com cerca de 50 nanômetros de comprimento e 20 nanômetros de largura - oferecem benefícios adicionais.
"As cadeias helicoidais periódicas aumentam a torção da luz em 4, 600 vezes, o que os torna visíveis em condições biológicas muito difíceis. E os nanobastões também aceleram o processo de formação de cadeias amilóides, o que é fundamental para a descoberta rápida de medicamentos, "disse Nicholas Kotov, co-autor correspondente do artigo e Professor Distinto de Ciências Químicas e Engenharia da Universidade Irving Langmuir na U-M.
Tipicamente, polipeptídeos amilóides levam alguns dias a uma semana para se ligarem. Isso retarda o teste de drogas potenciais. Os nanobastões aceleram o processo de polipeptídeos amilóides em um dia. Isso ocorre porque os bastonetes são revestidos com um surfactante químico chamado brometo de cetrimônio, semelhante ao cloreto de cetrimônio encontrado em alguns xampus e condicionadores. Quando as proteínas amilóides se ligam ao barril da barra de ouro, o surfactante os ajuda a formar uma forma enrolada que facilita a ligação a outras amilóides.
Quando os amilóides se conectam, suas barras de ouro formam uma hélice, torcendo a corda de proteína. E porque o ouro interage fortemente com a luz vermelha, essas hélices altamente organizadas torcem as ondas de luz vermelha com muita força.
Isso é o que leva à fácil detecção se um medicamento para prevenir as cadeias amilóides funcionou ou não. A configuração apresenta uma mistura realista de células, componentes do sangue, moléculas de drogas e proteínas amilóides que as drogas encontram no corpo entre dois polarizadores. O primeiro polarizador só permite a passagem de luz se oscilar na direção vertical. O segundo polarizador passa apenas ondas de luz que se movem na direção horizontal.
Se a luz não torcer entre os dois polarizadores, os dois polarizadores bloqueiam totalmente a luz. Isto é o que acontece quando uma droga tem sucesso:nenhuma cadeia amilóide se forma, portanto, apenas alguns nanobastões aleatórios estão torcendo a luz. Muito pouca luz passa pelos dois polarizadores. Contudo, se essas cadeias se formarem, eles torcem a luz vermelha. Um brilho vermelho se torna claramente visível - mostrando que o medicamento falhou.
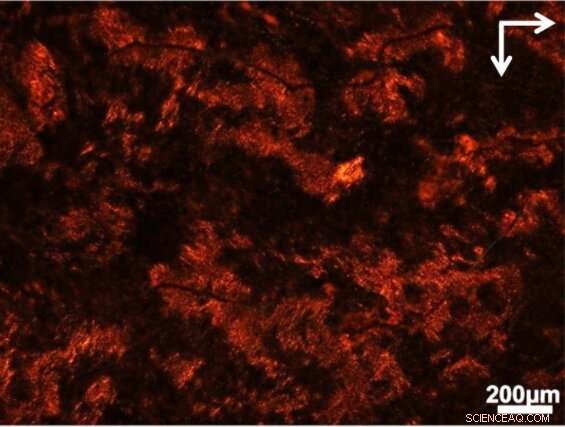
A visão através do polarizador mostra onde estruturas de torção de luz se formaram em uma sopa de células e materiais biológicos. Crédito:Jun Lu, Jilin University e University of Michigan
"Embora os experimentos tenham ajustado as melhores condições para a detecção de cadeias amilóides, as simulações de computador foram fundamentais para desvendar as complexas interações entre ouro, surfactantes e os fragmentos de proteínas, que precisam interagir simultaneamente para fazer a plataforma funcionar, “disse André de Moura, professora titular da Universidade Federal de São Carlos e coautora do artigo.
A equipe internacional também estabeleceu princípios de design unificados para fazer nanoestruturas torcidas que podem torcer significativamente a luz, um recurso que é crítico para muitos aplicativos.
A obra representa uma jornada de sete anos para Jun Lu, agora é pesquisador em engenharia química na U-M. No início do doutorado sob Liu na China, Lu começou tentando persuadir os polipeptídeos amiloides das ilhotas humanas a se automontarem, com hastes de ouro anexadas. Depois de cerca de um ano, ele e Liu haviam encontrado sinais fracos de que as assembleias estavam diminuindo a velocidade. Após um encontro fortuito no aeroporto com Kotov, a equipe começou a trabalhar no mecanismo de interações de luz e nos usos farmacêuticos desses conjuntos.
Lu trabalhou para tornar o efeito maior, dimensionar os nanobastões para complementar a distância entre os nanobastões. A equipe internacional explorou o aplicativo de rastreamento de drogas, e Lu desenvolveram simulações usando o poderoso supercomputador Great Lakes na Universidade de Michigan - enquanto seu colaborador na Universidade de São Paulo no Brasil, Kalil Bernardino, usou o supercomputador SDumont - para confirmar os mecanismos por trás das medições experimentais.
Embora o projeto fosse longo, Lu diz, "Cada esforço é bem recompensado. É como um sonho tornado realidade."
O artigo é intitulado "Melhoria da assimetria óptica em montagens quiroplasmáticas supramoleculares com ordem de longo alcance, "e será publicado online pela revista Ciência na quinta feira, 25 de fevereiro, 2021.