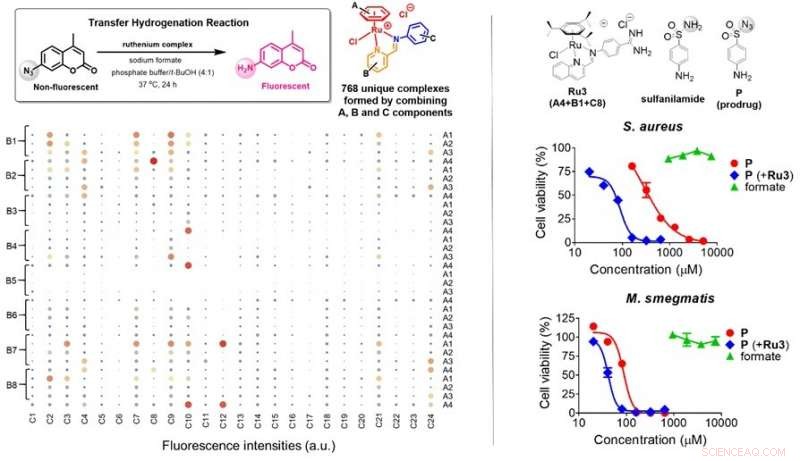
 p (Esquerda) Um total de 768 (4x8x24) complexos de rutênio únicos foram gerados por meio de reações de automontagem usando componentes moleculares A (4 tipos), B (8 tipos) e C (24 tipos) em soluções aquosas, em seguida, rastreados para atividades de hidrogenação de transferência na presença de formato. O tamanho dos círculos sombreados denota a eficácia dos complexos de rutênio na realização da hidrogenação de transferência na sonda, levando à ativação da fluorescência. Seis candidatos possíveis foram identificados. (Direita) As propriedades antibacterianas do pró-fármaco P (vermelho) em S. aureus e M. smegmatis foram ativadas na presença de Ru3 (azul), enquanto a suplementação de formato (verde) não teve efeito sobre o crescimento bacteriano. Ru3, montado usando A4, B1 e C8, foi capaz de utilizar formato presente em células de bactérias para ativar P. Crédito: Angewandte Chemie International Edition
p (Esquerda) Um total de 768 (4x8x24) complexos de rutênio únicos foram gerados por meio de reações de automontagem usando componentes moleculares A (4 tipos), B (8 tipos) e C (24 tipos) em soluções aquosas, em seguida, rastreados para atividades de hidrogenação de transferência na presença de formato. O tamanho dos círculos sombreados denota a eficácia dos complexos de rutênio na realização da hidrogenação de transferência na sonda, levando à ativação da fluorescência. Seis candidatos possíveis foram identificados. (Direita) As propriedades antibacterianas do pró-fármaco P (vermelho) em S. aureus e M. smegmatis foram ativadas na presença de Ru3 (azul), enquanto a suplementação de formato (verde) não teve efeito sobre o crescimento bacteriano. Ru3, montado usando A4, B1 e C8, foi capaz de utilizar formato presente em células de bactérias para ativar P. Crédito: Angewandte Chemie International Edition
p Pesquisadores da Universidade Nacional de Cingapura desenvolveram uma abordagem para direcionar seletivamente bactérias patogênicas, aproveitando um metabólito intracelular conhecido como formato, abundante nessas bactérias, como uma nova estratégia antimicrobiana. O formato é um metabólito essencial necessário para o crescimento em certas cepas patogênicas, mas só é encontrado em pequenas quantidades nas células de mamíferos. p A abundância e evolução do comportamento patogênico dos microrganismos bacterianos dão origem à tolerância e resistência aos antibióticos, que representam um perigo para a saúde pública global. Portanto, novas estratégias terapêuticas são necessárias para acompanhar essa ameaça crescente.
p A equipe de pesquisa liderada pelo Prof Ang Wee Han do Departamento de Química, A NUS propôs uma nova abordagem para direcionar bactérias por meio do aproveitamento do formato, um metabólito celular encontrado apenas em espécies bacterianas específicas, para ativar um pró-fármaco antibacteriano e inibir seletivamente o crescimento bacteriano. Os pesquisadores desenvolveram um sistema de enjaulamento molecular para drogas antibacterianas sulfonamidas, substituindo seu grupo de função amida essencial por azida (N
3
-
) Eles também encontraram um composto estável aquoso (complexo de organorutênio) que pode liberar essas drogas antibacterianas sob certas condições após a triagem através de 768 complexos de rutênio exclusivos. Quando usados juntos, os medicamentos antibacterianos são liberados na presença de formato endógeno encontrado nas células bacterianas. Esta estratégia explorou formato, um ingrediente necessário para o crescimento bacteriano, como arma para ativar pró-fármacos de sulfonamida a partir de complexos de rutênio desenvolvidos pelos pesquisadores.
p Prof Ang disse, "Este é o primeiro relatório que aproveita metabólitos celulares únicos para desencadear a ativação de pró-drogas em bactérias. Ele abre o caminho para uma nova abordagem de terapia antibacteriana direcionada, explorando as diferenças na ocorrência de metabólitos naturais entre as cepas patogênicas."
p O pró-fármaco de sulfonamida racionalmente projetado com fração de enjaulamento de azida foi eficientemente ativado pelos complexos de organorutênio em bactérias abundantes em formato com aumento de até 8 vezes na eficácia do fármaco, particularmente nas bactérias patogênicas, Staphylococcus aureus e Escherichia coli. Em contraste, elevação da eficácia em Mycobacterium smegmatis, que limitou a capacidade de geração de formato, aumentou apenas duas vezes. Isso validou a tese de que formato de metabólito intracelular pode ser direcionado para o desenvolvimento de novas estratégias terapêuticas antibacterianas.
p Prof Ang disse, "A resistência aos antibióticos é um dos desafios mais sérios que a humanidade enfrenta e, no entanto, o desenvolvimento de novos antibióticos não acompanhou essa ameaça crescente. O metaboloma bacteriano exclusivo oferece novas possibilidades para abordar esse problema. Esperamos que esta descoberta estimule novas pesquisas com objetivos distintos. metabólitos para o desenvolvimento de agentes antibacterianos melhores e mais seletivos. "
p A equipe de pesquisa está trabalhando para desenvolver outras estratégias de ativação de pró-drogas que podem aproveitar o formato bacteriano endógeno. Além disso, investigações sobre outros antibióticos clínicos, como trimetoprima e sulfametoxazol, também estão em andamento.
