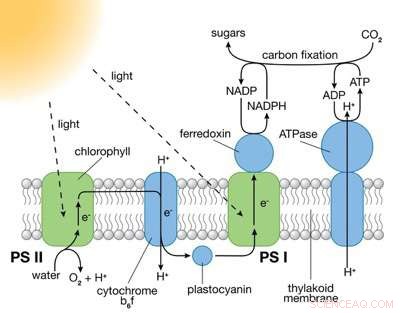
Os fotossistemas (PS) I e II são grandes complexos de proteínas que contêm moléculas de pigmento que absorvem luz, necessárias para a fotossíntese. PS II captura energia da luz solar para extrair elétrons das moléculas de água, dividir a água em íons de oxigênio e hidrogênio (H +) e produzir energia química na forma de ATP. PS I usa esses elétrons e H + para reduzir NADP + (uma molécula portadora de elétrons) a NADPH. A energia química contida no ATP e no NADPH é então usada na reação independente da luz da fotossíntese para converter o dióxido de carbono em açúcares. Crédito:Laboratório Nacional de Brookhaven
A fotossíntese em plantas verdes converte a energia solar em energia química armazenada, transformando dióxido de carbono atmosférico e água em moléculas de açúcar que alimentam o crescimento das plantas. Os cientistas têm tentado replicar artificialmente esse processo de conversão de energia, com o objetivo de produzir combustíveis ecologicamente corretos e sustentáveis, tais como hidrogênio e metanol. Mas imitando as principais funções do centro fotossintético, onde biomoléculas especializadas realizam fotossíntese, provou ser um desafio. A fotossíntese artificial requer a concepção de um sistema molecular que pode absorver luz, transporte e carga elétrica separada, e catalisar reações de produção de combustível - todos os processos complicados que devem operar em sincronia para alcançar alta eficiência de conversão de energia.
Agora, químicos do Laboratório Nacional Brookhaven e Virginia Tech do Departamento de Energia dos EUA (DOE) e da Virginia Tech projetaram dois fotocatalisadores (materiais que aceleram as reações químicas ao absorver luz) que incorporam componentes individuais especializados para a absorção de luz, separação de carga, ou catálise em uma única "supramolécula". Em ambos os sistemas moleculares, múltiplos centros de coleta de luz feitos de íons metálicos de rutênio (Ru) são conectados a um único centro catalítico feito de íons metálicos de ródio (Rh) por meio de uma molécula em ponte que promove a transferência de elétrons dos centros Ru para o catalisador Rh, onde o hidrogênio é produzido.
Eles compararam o desempenho de produção de hidrogênio e analisaram as propriedades físicas das supramoléculas, conforme descrito em um artigo publicado na edição online de 1º de junho de Jornal da American Chemical Society , para entender por que o fotocatalisador com seis em vez de três absorvedores de luz Ru produz mais hidrogênio e permanece estável por um longo período de tempo.
"O desenvolvimento de sistemas moleculares eficientes para a produção de hidrogênio é difícil porque os processos estão ocorrendo em taxas diferentes, "disse o autor principal Gerald Manbeck, um químico do grupo de fotossíntese artificial no Laboratório de Brookhaven. "Completar o turnover catalítico do hidrogênio antes das cargas separadas - o elétron excitado pela luz carregada negativamente e o" buraco "positivo deixado para trás depois que a molécula excitada absorve a energia da luz - ter a chance de recombinar e produzir calor de forma perdulária é um dos maiores desafios. "
Outra complicação é que dois elétrons são necessários para produzir cada molécula de hidrogênio. Para que a catálise aconteça, o sistema deve ser capaz de reter o primeiro elétron por tempo suficiente para que o segundo apareça. "Ao construir supramoléculas com vários absorvedores de luz que podem funcionar de forma independente, estamos aumentando a probabilidade de usar cada elétron de forma produtiva e melhorando a capacidade das moléculas de funcionar em condições de pouca luz, "disse Manbeck.
Manbeck começou a fazer as supramoléculas na Virginia Tech em 2012 com a falecida Karen Brewer, coautor e seu orientador de pós-doutorado. Ele descobriu que o sistema de quatro metais (tetrametálico) com três centros de absorção de luz Ru e um centro catalítico Rh produzia apenas 40 moléculas de hidrogênio para cada molécula de catalisador e parou de funcionar após cerca de quatro horas. Em comparação, o sistema de sete metais (heptametálico) com seis centros Ru e um centro Rh era mais de sete vezes mais eficiente, pedalando 300 vezes para produzir hidrogênio por 10 horas. Essa grande disparidade em eficiência e estabilidade era intrigante porque as supramoléculas contêm componentes muito semelhantes.
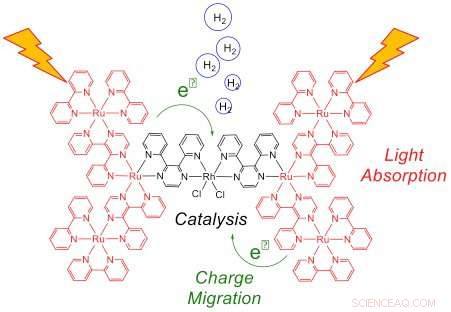
Esta representação do sistema heptametálico após a exposição à luz mostra a coleta de luz pelos seis centros Ru (vermelho) e transferência de elétrons para o catalisador Rh (preto), onde o hidrogênio é produzido. A transferência eficiente de elétrons para Rh é essencial para obter um alto desempenho catalítico. Crédito:Laboratório Nacional de Brookhaven
Manbeck ingressou na Brookhaven em 2013 e desde então realizou uma série de experimentos com o co-autor Etsuko Fujita, líder do grupo de fotossíntese artificial, para compreender as causas fundamentais da diferença de desempenho.
"A capacidade de formar o estado de carga separada é um indicador parcial de se uma supramolécula será um bom fotocatalisador, mas realizar uma separação de carga eficiente requer um ajuste fino da energética de cada componente, "disse Fujita." Para promover a catálise, o catalisador Rh deve ter energia baixa o suficiente para aceitar os elétrons dos absorvedores de luz Ru quando os absorvedores são expostos à luz. "
Por meio da voltametria cíclica, uma técnica eletroquímica que mostra os níveis de energia dentro de uma molécula, os cientistas descobriram que o catalisador Rh do sistema heptametálico é ligeiramente mais pobre em elétrons e, portanto, mais receptivo a receber elétrons do que sua contraparte no sistema tetrametálico. Este resultado sugere que a transferência de carga foi favorável no sistema heptametálico, mas não no sistema tetrametálico.
Eles verificaram sua hipótese com uma técnica resolvida no tempo chamada espectroscopia de absorção transiente de nanossegundos, em que uma molécula é promovida a um estado excitado por um pulso de laser intenso e a decadência do estado excitado é medida ao longo do tempo. Os espectros resultantes revelaram a presença de uma transferência de carga Ru-para-Rh apenas no sistema heptametálico.
"Os dados não apenas confirmaram nossa hipótese, mas também revelaram que a separação de cargas no estado excitado ocorre muito mais rapidamente do que havíamos imaginado, "disse Manbeck." Na verdade, a migração de carga acontece mais rápido do que a resolução de tempo de nosso instrumento, e provavelmente envolve curta duração, estados excitados de alta energia. ”Os pesquisadores planejam procurar um colaborador com instrumentação mais rápida que possa medir a taxa exata de separação de carga para ajudar a esclarecer o mecanismo.
Em um experimento de acompanhamento, os cientistas realizaram a medição de absorção transiente em condições operacionais fotocatalíticas, with a reagent used as the ultimate source of electrons to produce hydrogen (a scalable artificial photosynthesis of hydrogen fuel from water would require replacing the reagent with electrons released during water oxidation). The excited state generated by the laser pulse rapidly accepted an electron from the reagent. They discovered that the added electron resides on Rh in the heptametallic system only, further supporting the charge migration to Rh predicted by cyclic voltammetry.
"The high photocatalytic turnover of the heptametallic system and the principles governing charge separation that were uncovered in this work encourage further studies using multiple light-harvesting units linked to single catalytic sites, " said Manbeck.