
Carbonetos de metal bidimensionais desencadeiam uma reação que divide a água em oxigênio e valioso gás hidrogênio. Os pesquisadores de Berkeley descobriram uma nova receita fácil para cozinhar essas folhas nanométricas que é quase tão simples quanto fazer gelatina a partir de uma caixa. Crédito:gráfico Xining Zang, copyright Wiley
Um novo catalisador barato e eficaz desenvolvido por pesquisadores da Universidade da Califórnia, Berkeley, pode gerar combustível de hidrogênio a partir da água com a mesma eficiência da platina, atualmente o melhor - mas também o mais caro - catalisador de divisão de água que existe.
O catalisador, que é composto de folhas nanométricas de carboneto de metal, é fabricado usando um processo de automontagem que depende de um ingrediente surpreendente:gelatina, o material que dá a Jell-O sua agitação.
"Platinum é caro, portanto, seria desejável encontrar outros materiais alternativos para substituí-lo, "disse o autor sênior Liwei Lin, professor de engenharia mecânica na UC Berkeley. "Na verdade, estamos usando algo semelhante ao Jell-O que você pode comer como base, e misturá-lo com alguns dos abundantes elementos de terra para criar um novo material barato para importantes reações catalíticas. "
O trabalho aparece na edição impressa de 13 de dezembro da revista. Materiais avançados .
Um choque elétrico pode quebrar as fortes ligações que unem as moléculas de água, criando oxigênio e gás hidrogênio, o último dos quais é uma fonte extremamente valiosa de energia para alimentar células de combustível de hidrogênio. O gás hidrogênio também pode ser usado para ajudar a armazenar energia de fontes renováveis, porém intermitentes, como a energia solar e eólica, que produzem eletricidade em excesso quando o sol brilha ou quando o vento sopra, mas que ficam dormentes em dias chuvosos ou calmos.

Quando ampliado, os carbonetos de metal bidimensionais se assemelham a folhas de celofane. Crédito:foto de Xining Zang, copyright Wiley
Mas simplesmente colocar um eletrodo em um copo d'água é um método extremamente ineficiente de gerar gás hidrogênio. Nos últimos 20 anos, os cientistas têm procurado catalisadores que podem acelerar essa reação, tornando-o prático para uso em larga escala.
“A forma tradicional de usar gás de água para gerar hidrogênio ainda domina na indústria. este método produz dióxido de carbono como subproduto, "disse o primeiro autor Xining Zang, que conduziu a pesquisa como estudante de graduação em engenharia mecânica na UC Berkeley. "A geração de hidrogênio eletrocatalítico está crescendo na última década, seguindo a demanda global de redução de emissões. O desenvolvimento de um catalisador altamente eficiente e de baixo custo para eletrohidrólise trará profundas técnicas, benefício econômico e social. "
Para criar o catalisador, os pesquisadores seguiram uma receita quase tão simples quanto fazer gelatina de uma caixa. Eles misturaram gelatina e um íon metálico - ou molibdênio, tungstênio ou cobalto - com água, e depois deixe a mistura secar.
"Acreditamos que à medida que a gelatina seca, ele se auto-monta camada por camada, "Lin disse." O íon metálico é transportado pela gelatina, então, quando a gelatina se auto-monta, seu íon de metal também é organizado nessas camadas planas, e essas folhas planas são o que dão à Jell-O sua característica superfície semelhante a um espelho. "
O aquecimento da mistura a 600 graus Celsius aciona o íon metálico para reagir com os átomos de carbono na gelatina, formando grande, folhas nanométricas de carboneto de metal. A gelatina não reagida é queimada.
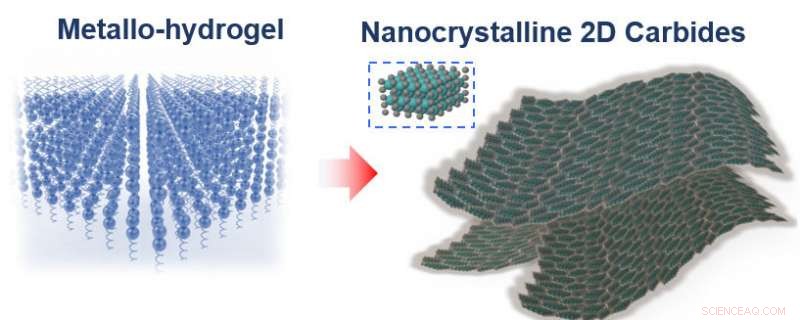
As moléculas da gelatina se auto-montam naturalmente em folhas planas, carregando os íons de metal com eles (esquerda). Aquecer a mistura a 600 graus Celsius queima a gelatina, deixando folhas nanométricas de carboneto de metal. Crédito:ilustração de Xining Zang, copyright Wiley
Os pesquisadores testaram a eficiência dos catalisadores colocando-os na água e passando uma corrente elétrica por eles. Quando empilhados uns contra os outros, carboneto de molibdênio dividiu a água com mais eficiência, seguido por carboneto de tungstênio e, em seguida, carboneto de cobalto, que não formou camadas tão finas quanto as outras duas. A mistura de íons de molibdênio com uma pequena quantidade de cobalto aumentou ainda mais o desempenho.
“É possível que outras formas de carboneto possam ter um desempenho ainda melhor, "Lin disse.
A forma bidimensional do catalisador é uma das razões de seu sucesso. Isso porque a água tem que estar em contato com a superfície do catalisador para fazer seu trabalho, e a grande área superficial das folhas significa que os carbonetos metálicos são extremamente eficientes para seu peso.
Porque a receita é tão simples, poderia ser facilmente ampliado para produzir grandes quantidades do catalisador, dizem os pesquisadores.
“Descobrimos que o desempenho está muito próximo do melhor catalisador feito de platina e carbono, que é o padrão ouro nesta área, "Lin disse." Isso significa que podemos substituir a muito cara platina por nosso material, que é feito em um processo de fabricação muito escalonável. "