
Um close-up de um pedaço de minério de cobre. Crédito:Coldmoon Photoproject / Shutterstock
Eles dizem que é melhor ter algo especial e perdido do que nunca ter tido. Quem teria pensado que esse sentimento é verdadeiro para os catalisadores de óxido de metal? De acordo com cientistas do Laboratório Nacional Lawrence Berkeley (Berkeley Lab) e Caltech, o cobre que já foi ligado ao oxigênio é melhor para converter dióxido de carbono em combustíveis renováveis do que o cobre que nunca foi ligado ao oxigênio.
Para seu estudo, agora publicado no jornal Catálise ACS , os cientistas realizaram espectroscopia de raios-X em protótipos de gerador de combustível solar para demonstrar que os catalisadores feitos de óxido de cobre são superiores aos catalisadores de origem puramente metálica quando se trata de produzir etileno, um gás de dois carbonos com uma vasta gama de aplicações industriais - mesmo depois de não haver átomos de oxigênio detectáveis restantes no catalisador.
"Muitos pesquisadores demonstraram que catalisadores de cobre derivados de óxido são melhores na fabricação de produtos combustíveis de CO 2 , Contudo, há um debate sobre por que isso ocorre, "disse o co-líder de pesquisa Walter Drisdell, um químico do Berkeley Lab e membro do Joint Center for Artificial Photosynthesis (JCAP). A missão do JCAP é desenvolver de forma eficiente, tecnologias movidas a energia solar que podem converter CO atmosférico 2 em combustíveis alternativos de petróleo. Drisdell e seus colegas dizem que sua descoberta é um avanço importante em direção a esse objetivo.
Ele explicou que sob condições operacionais para geração de combustível - o que envolve primeiro a conversão do CO 2 em monóxido de carbono, em seguida, construindo cadeias de hidrocarbonetos - o oxigênio ligado ao cobre é naturalmente esgotado no catalisador. Contudo, alguns pesquisadores acreditam que pequenas quantidades de oxigênio permanecem na estrutura metálica, e que esta é a fonte do aumento da eficiência.
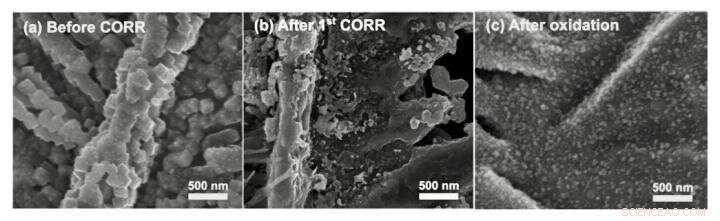
Essas imagens de microscopia eletrônica de varredura mostram a estrutura do catalisador de cobre em diferentes estágios. (a) O catalisador antes de executar quaisquer reações. As estruturas cúbicas na superfície são resultado do óxido. (b) Qual a aparência do catalisador após a execução da química de redução de CO; todo o oxigênio se foi. (c) O catalisador após adicionar intencionalmente oxigênio de volta ao metal como uma forma de recuperar o desempenho do catalisador. O óxido de cobre se formou em pequenas nanopartículas no topo da superfície lisa do metal de cobre. Crédito:Lee et al./ACS Catalysis
Para resolver o debate, a equipe trouxe um sistema de cromatografia gasosa (GC) para a linha de luz de raios-X para que pudessem detectar a produção de etileno em tempo real. "Nossos colaboradores da Caltech conduziram o GC desde Pasadena e o instalaram nas instalações de raios-X em Palo Alto, "disse Soo Hong Lee, um pesquisador de pós-doutorado no Berkeley Lab e co-autor principal do estudo. "Com isso, mostramos que não há correlação entre a quantidade de oxigênio ('óxido') no catalisador e a quantidade de etileno produzida. Então, pensamos que os catalisadores derivados de óxidos são bons, não porque eles têm oxigênio remanescente enquanto reduzem o monóxido de carbono, mas porque o processo de remoção do oxigênio cria uma estrutura metálica de cobre que é melhor na formação de etileno. "
A equipe mostrou ainda que, embora a eficiência dos catalisadores derivados de óxidos diminua com o tempo, ele pode ser regularmente "reativado", adicionando e removendo novamente o oxigênio durante um processo de manutenção simples. O próximo passo é projetar uma célula geradora de combustível que possa operar com instrumentos de espalhamento de raios-X, permitindo-lhes mapear diretamente a mudança da estrutura do catalisador enquanto converte o monóxido de carbono em etileno.
A equipe de pesquisa também incluiu Ian Sullivan e Chengxiang Xiang da Caltech, e David Larson, Guiji Liu, e Francesca Toma no Berkeley Lab. Este trabalho foi apoiado pelo Departamento de Energia dos EUA (DOE) Office of Science. JCAP é um DOE Energy Innovation Hub.