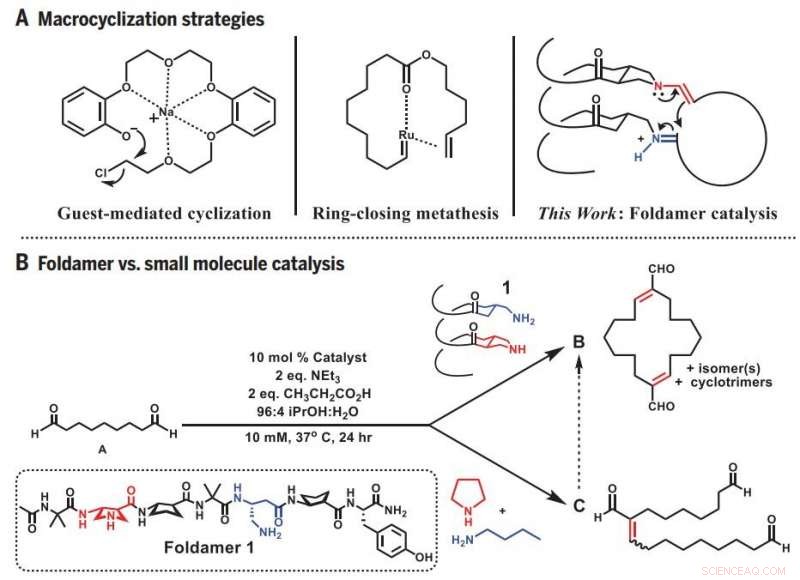
Estratégias de macrociclização. (A) Abordagens anteriores e abordagem de foldamer para macrociclização. (B) Reatividade divergente:Foldamer versus catálise de moléculas pequenas. eq., equivalente (s). Crédito: Ciência (2019) .DOI:10.1126 / science.aax7344
Inspirando-se na natureza, Químicos da Universidade de Wisconsin-Madison descobriram uma maneira eficiente de disputar por muito tempo, serpenteando moléculas para formar grandes anéis - anéis que formam a espinha dorsal de muitos produtos farmacêuticos, mas são difíceis de produzir em laboratório.
O trabalho pode representar um progresso preliminar para decifrar como as enzimas, afiado pela evolução, tão eficientemente produzir compostos naturais. Mais imediatamente, o novo método pode ajudar os pesquisadores a sintetizar drogas com grandes estruturas em anel, como os da hepatite. A pesquisa foi publicada em 19 de dezembro na revista Ciência .
A natureza prefere a desordem de um longo, molécula flexível na ordem de um anel rígido, o que torna notoriamente difícil para os químicos fazerem com que grandes anéis se formem em laboratório. "Se as moléculas lineares ficarem longas o suficiente, é como se as pontas não soubessem mais que estão conectadas, e eles são tão propensos a se ligar a outras moléculas quanto a se unir, "diz o professor de química da UW-Madison Sam Gellman, o autor sênior do relatório.
No entanto, as enzimas biológicas podem facilmente reunir essas extremidades e formar anéis de todos os tamanhos. Eles realizam essa façanha graças ao seu complexo, formas tridimensionais que atuam como uma fechadura especializada - a molécula linear se encaixa no lugar como uma chave exatamente da maneira certa para que ocorra uma reação organizada.
Para estudar como as enzimas funcionam e imitar suas habilidades, A equipe de Gellman tornou-se muito menor, moléculas tridimensionais semelhantes a proteínas, chamadas dobradeiras, que seu laboratório ajudou a desenvolver.
Como o dobrador tem uma forma tridimensional que pode se agarrar às extremidades da molécula precursora flexível, aumenta muito as chances de que os fins se encontrem. Ao mesmo tempo, o foldamer catalisa a reação certa que liga as pontas em um anel fechado. O resultado é uma síntese direta e previsível de um desafio, e útil, forma molecular.
"Como químicos, vemos como as enzimas são extraordinariamente eficazes em fazer reações que são difíceis de realizar em um frasco, mas não entendemos realmente como eles funcionam, "diz Gellman." Se aprendermos como esses pequenos catalisadores dobráveis funcionam, podemos ser capazes de construir catalisadores que sejam eficazes para muitas reações diferentes. Em última análise, talvez possamos abrir nosso caminho em direção a dobradores que têm atividade verdadeiramente semelhante à de uma enzima. "
O aluno de pós-graduação e autor principal Zebediah Girvin começou a pesquisa testando as habilidades de um curta, dobrador em forma de espiral. Girvin tentou usar o dobrador para dobrar uma molécula linear contendo nove átomos de carbono para que ela formasse um anel. Mas em vez de um anel do tamanho esperado, Girvin obteve uma com o dobro do tamanho - o resultado de duas moléculas precursoras primeiro se juntando e depois fechando o círculo.
"Esta é uma situação comum na ciência. Você tenta algo e não funciona da maneira que você esperava, "diz Gellman." O desafio é reconhecer quando o resultado surpreendente é tão interessante quanto o objetivo original, ou ainda mais interessante. "
Guiado por esta serendipidade, Girvin começou a testar o quão bem o dobrador poderia produzir os anéis maiores que parecia preferir criar. Ele descobriu que poderia fabricar facilmente anéis compostos de 12 a 22 átomos de carbono quando os locais reativos da dobra, onde ocorre o fechamento do anel, estavam alinhados uns com os outros de um lado. Essa orientação trouxe as duas extremidades de diversas moléculas lineares perto o suficiente para se fundir.
Como prova de conceito para a nova técnica, Girvin sintetizou o produto natural robustol a partir do zero. Derivado das folhas do carvalho sedoso australiano, robustol pesa com um anel de 22 átomos robusto.
A equipe de Gellman está muito animada com o potencial dos dobradores para catalisar outras reações úteis e possivelmente ajudar a desvendar mistérios de longa data sobre como as enzimas, virtuosos químicos da natureza, produzir as moléculas necessárias para a vida simplesmente organizando os blocos de construção de aminoácidos na forma certa. Embora essas respostas ainda estejam a anos de distância, a técnica de fechamento do anel que eles descobriram poderia ter um uso mais imediato na síntese de candidatos a drogas. O vaniprevir, medicamento para hepatite C, que é usado no Japão e em testes de estágio final nos EUA, contém apenas este tipo de anel grande.
O verdadeiro potencial das dobradeiras deriva de sua diversidade. Os químicos podem fazer uma variedade quase infinita de dobras no laboratório porque têm acesso a mais blocos de construção do que os encontrados nas proteínas naturais. Isso pode permitir que os químicos construam catalisadores mais úteis, o que levou Gellman a patentear certos dobradores e fundou a empresa Longevity Biotech para explorar seus usos terapêuticos.
Daqui para frente, essa riqueza de opções permitirá aos pesquisadores organizar esses catalisadores em formatos que provavelmente serão úteis de maneiras inesperadas. Só mais pesquisas dirão.
"Ainda não sabemos do que esses catalisadores são capazes, "diz Girvin." Levará anos para descobrir seu potencial, e é importante lançarmos uma rede ampla e manter a mente aberta sobre o que podemos realizar com essas novas ferramentas. "