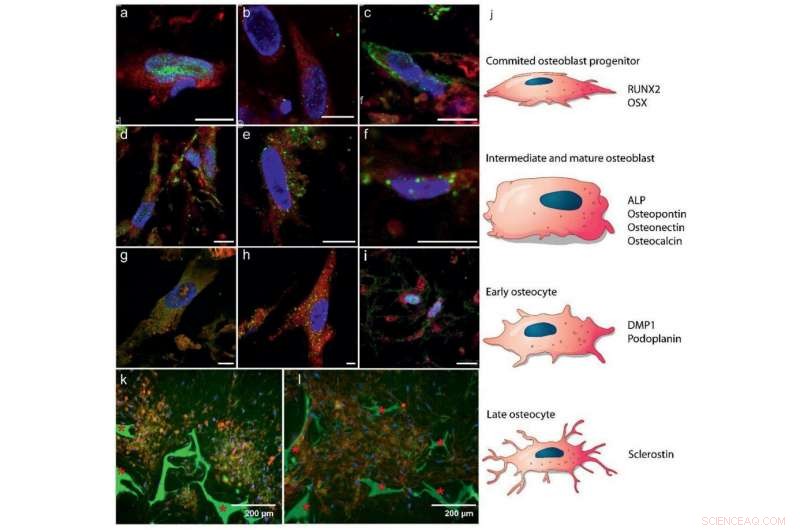
Diferenciação de hBMSCs em osteoblastos e osteócitos:a – i) Imagem imunohistoquímica de fluorescência mostrando marcadores para a – c) estágios iniciais da formação de osteoblastos, d – f) osteoblastos maduros, eg – i) desenvolvimento de osteócitos (5,55 mm de glicose). Código de cores:citoplasma de células vermelhas, azul - núcleos de células, verde:a) RUNX2 (dia 7), b) OSX (dia 7), c) ALP (dia 26), d) osteocalcina (dia 26), e) osteopontina (dia 26), f) osteonectina (dia 21), g) DMP1 (dia 28), h) podoplanina (dia 28), e i) esclerostina (dia 28). Barras de escala:10 µm. Veja a Figura S4, Informações de Apoio, para canais separados. j) Ilustração esquemática da diferenciação de MSCs em osteoblastos e osteócitos, indicando em qual estado a expressão da proteína é esperada em a – i. k, l) Imagens fluorescentes indicando domínios auto-organizados de osteócitos incorporados em uma matriz mineralizada após 8 semanas (glicose 25 mm), k) co-localização de osteócitos (esclerostina, vermelho) e mineral (calceína, verde), e l) colágeno (CNA35, vermelho) e mineral (calceína, verde) * Indica o andaime de fibroína de seda.
Imagine usar células-tronco da medula óssea para cultivar um pedaço de tecido ósseo no laboratório, depois disso, os médicos exploram quais drogas têm o efeito desejado em seus ossos. Desta maneira, um plano de tratamento feito sob medida seria feito para todos, com a melhor abordagem sendo clara de antemão:medicina personalizada no seu melhor.
Essa visão do futuro não é mais ficção científica, agora que os pesquisadores da Universidade de Tecnologia de Eindhoven e do centro médico da Universidade de Radboud perceberam a primeira parte:cultivar um pedaço de tecido ósseo natural a partir de células-tronco humanas. É o primeiro organoide de osso, uma versão simplificada do original, os pesquisadores relatam hoje no jornal Materiais Funcionais Avançados .
Imagem coerente
"Com isso, apresentamos, pela primeira vez, o quadro completo da formação óssea em estágio inicial, "diz Sandra Hofmann, professor associado em Bioengenharia óssea da TU / e. E isso é de grande importância:como nossos ossos são formados ainda é um grande mistério. O osso é um material muito complexo no qual inúmeras células e processos interagem, e compreende uma matriz engenhosa de colágeno e mineral para fornecer força. Muito se sabe sobre os componentes individuais, mas faltou uma imagem coerente até agora.
Três tipos de células desempenham o papel principal na formação óssea:osteoblastos (que constroem o tecido ósseo), osteoclastos (que retiram o osso) e osteócitos (que regulam a formação e a degradação do osso). "A maioria dos estudos até agora se concentrou em um desses tipos de células, mas isso não é uma boa representação do tecido real, ", diz Hofmann." Apresentamos aqui um pedaço de osso trançado (osso em estágio inicial) que se desenvolveu a partir de células-tronco e contém dois tipos dessas células:osteoblastos e osteócitos. Agora vemos que podemos fazer ossos semelhantes à vida exclusivamente com esses dois tipos de células. "
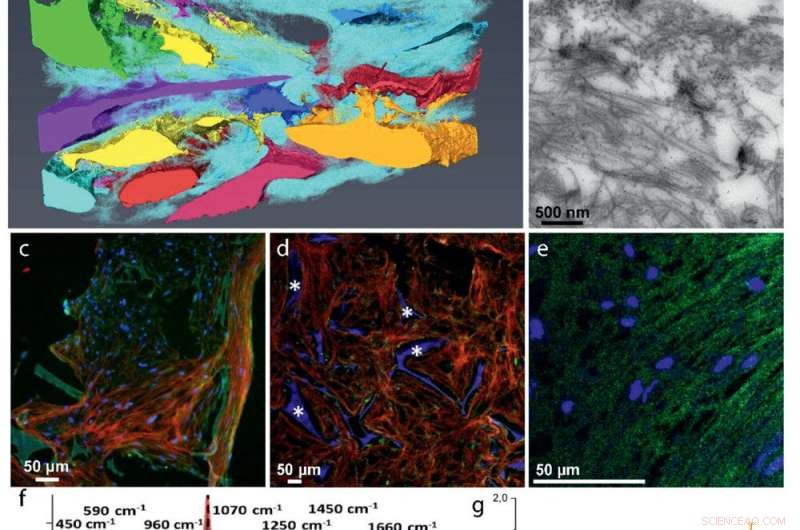
Desenvolvimento de ECM:a) A reconstrução 3D FIB / SEM mostra a incorporação das células na matriz de colágeno (ciano). As células discretas são representadas com cores diferentes. b) Imagem TEM de uma seção de 70 nm mostrando a distribuição aleatória de fibrilas de colágeno. O colágeno tipo I foi identificado por imunomarcação. c – e) Imuno-histoquímica fluorescente identificando proteínas não colágenas-chave na matriz colágena:c) Co-localização de osteocalcina (verde) e colágeno (vermelho). d) Distribuição da osteopontina (verde) na matriz de colágeno (vermelho). * Indica o andaime de fibroína de seda. e) Co-localização de DMP1 (verde) com a estrutura de colágeno (ver Figura S5, Informações de Apoio, para imagem de colágeno). f – g) Microespectrometria Raman de matrizes mineralizadas. f) Espectros Raman localizados de colágeno mineralizado de osso em desenvolvimento de peixe-zebra (vermelho), a co-cultura osteogênica 3D (azul), e osso humano de uma fêmea de 10 anos de idade (g cinza) relações minerais / matriz derivadas de Raman de 4 tecidos mineralizados de peixe-zebra (N =6, vermelho), Cultura osteogênica 3D (N =7, verde), Fêmea humana de 10 anos (N =1, cinza), e 48+ anos de idade do sexo masculino (N =7, Preto, retirado da ref. [36]). As barras indicam os desvios padrão da amostra. h) Apresentação do mapa de calor de uma seção transversal 3D FIB / SEM mostrando fibrilas de colágeno desorganizadas com diferentes graus de mineralização (Figura S10, Informações de Apoio). As setas indicam fibrilas de colágeno não mineralizadas (azul claro), seta indica fibrila de colágeno mineralizado (laranja). i) Imagem TEM mostrando fibrilas de colágeno mineralizadas individuais.
Ficando mais sábio com cutucões moleculares
"E talvez mais importante, nosso sistema se comporta como osso em estágio inicial, "diz Anat Akiva, professor assistente de Biologia Celular em Radboudumc. "Mostramos que ambos os tipos de células produzem as proteínas de que precisam para sua funcionalidade, e mostramos com o maior detalhe que a matriz é realmente a matriz óssea que vemos no tecido real. "
O fato de que uma representação simplificada da formação do osso em nível molecular agora é possível oferece possibilidades sem precedentes, de acordo com os pesquisadores. "Um osso consiste em 99% de colágeno e minerais, mas também há outro 1% de proteínas que são essenciais para o sucesso da formação óssea, "explica o professor Nico Sommerdijk de Radboudumc." Então, qual é o papel dessas proteínas? Como eles apoiam a formação óssea? Nunca antes fomos capazes de olhar para os marcos desse processo em um nível molecular. "
E com isso, eles imediatamente têm uma boa entrada para investigar a causa das doenças genéticas dos ossos, como a "doença dos ossos frágeis" e seus possíveis tratamentos. "Lembre-se de que a origem de muitas doenças está no nível molecular - assim como o tratamento, "diz Akiva." Na verdade, agora temos um sistema simples em um ambiente confiável no qual podemos vasculhar e ver como as células ósseas reagem aos estímulos que fornecemos. "