Crédito:Pacific Northwest National Laboratory
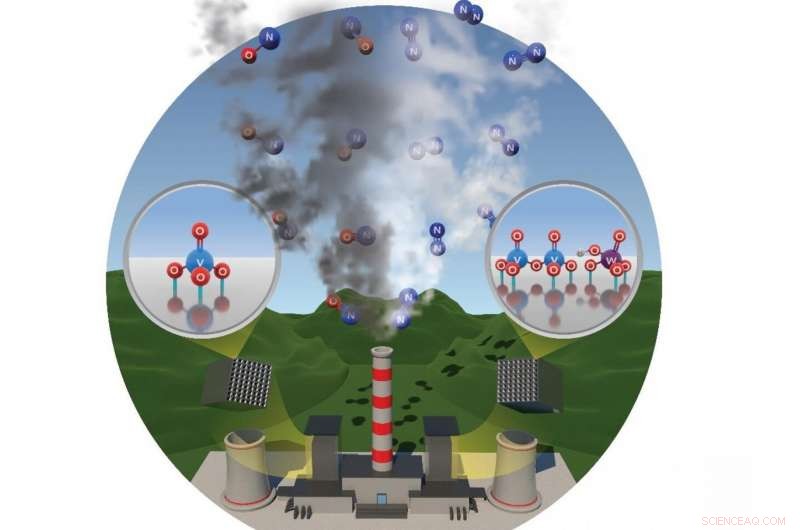
Óxidos de nitrogênio, também conhecido como NÃO x , se formam quando os combustíveis fósseis queimam em altas temperaturas. Quando emitido de fontes industriais, como usinas de carvão, esses poluentes reagem com outros compostos para produzir poluição atmosférica prejudicial. Para mitigar estes NÃO x emissões, engenheiros desenvolveram um processo chamado redução catalítica seletiva (SCR) onde NÃO x passa por um conversor, ou purificador de ar, que transforma o produto químico perigoso em gás nitrogênio inofensivo.
Embora SCR não seja novo, a química subjacente dos óxidos de metal usados no processo permanecia desconhecida - até agora. Uma equipe de pesquisa liderada pelo químico PNNL Jian Zhi Hu, junto com colaboradores de várias universidades, descreveu de forma decisiva como os óxidos de metal estão dispostos.
"O modo como uma reação funciona tem implicações quando tentamos projetar materiais ainda melhores, "disse Nicholas Jaegers, o primeiro autor do artigo e estudante de doutorado na Washington State University. "Se pudermos identificar uma tendência do que está funcionando especificamente em nível molecular, então podemos ser capazes de alterar o sistema para ter mais dos efeitos que queremos ou aplicar isso a outras reações com os mesmos requisitos de atividade. "Jaegers é um aluno do laboratório do Professor Yong Wang, o cientista sênior que orienta a pesquisa.
A separação
Como em muitos relacionamentos tóxicos, nitrogênio e oxigênio - os dois elementos benignos que compõem o NO x —São perigosos juntos, e, uma vez ligado, difícil de se separar. O catalisador certo facilita a separação, e sob as condições certas, ajuda os átomos a se separarem ainda mais rápido.
As unidades SCR projetadas para quebrar NO x em usinas de energia ou outras instalações de combustão estacionárias são feitas de uma estrutura de suporte de óxido de titânio com óxido de vanádio e óxido de tungstênio no topo. NÃO x não se divide sem um catalisador, como óxido de vanádio, mas a divisão é mais rápida e completa quando o óxido de tungstênio é adicionado.
Os cientistas especularam que o papel do tungstênio era estrutural e não uma parte direta do sítio ativo na reação, mas eles não podiam ter certeza sem saber o que estava acontecendo no nível molecular.
Até agora, os limites da medição das estruturas moleculares impediam a compreensão de como a reação funcionava. Muitas técnicas podem detectar a presença de certos elementos, suas concentrações, e seus estados químicos. Esses métodos, Contudo, degradam amostras experimentais ou carecem de precisão para fazer uma afirmação definitiva sobre se uma molécula existe sozinha ou dentro de um acoplamento ou grupo. A equipe superou essas limitações com uma combinação de ressonância magnética nuclear giratória de ângulo mágico de alta velocidade (MAS NMR), testes de reatividade, e modelagem computacional para fazer sua descoberta.
"Para encontrar esta evidência, MAS NMR é absolutamente necessário, "disse Karl Mueller, diretor de ciência e tecnologia da Diretoria de Ciências Físicas e Computacionais do PNNL. O instrumento, financiado pelo Departamento de Ciências Básicas de Energia do Departamento de Energia, permitiu que os cientistas tirassem conclusões decisivas sobre as estruturas moleculares responsáveis pela reação catalítica.
Procurando por um Sinal
O MAS NMR funciona girando uma amostra em um campo magnético forte em um ângulo específico e disparando ondas de rádio através dele para excitar e detectar as frequências ressonantes de spins nucleares associados aos átomos. Porque cada átomo tem uma frequência diferente, as ondas energizam apenas os elementos visados. Cada átomo envia uma resposta que revela sua localização e o que está ao seu redor. Com base nessa resposta - e em quão detalhada ela é - os cientistas podem entender a estrutura de um material.
MAS NMR é particularmente sensível às mudanças estruturais em materiais contendo vanádio, mas a equipe não sabia quais respostas esperar de diferentes arranjos de óxido de vanádio. Em estreita colaboração com a equipe de David Dixon da Universidade do Alabama, eles modelaram respostas de saída para vários arranjos de vanádio, em seguida, combinou os resultados modelados com os resultados de MAS NMR. Essa comparação permitiu aos pesquisadores identificar as estruturas da superfície.
A equipe descobriu que óxidos de vanádio únicos não ligados, também conhecidos como monômeros, foram relativamente lentos em permitir o NÃO x reação para prosseguir. Contudo, pares ou grupos de óxidos de vanádio - próximos no suporte de titânio - aumentaram drasticamente a eficiência da reação. This was precisely determined by Professor Israel Wachs' group from Lehigh University.
The team also learned the tungsten was necessary not for its reactive properties, but because it encouraged the vanadium oxides to arrange into the reactive clusters. Unlike isolated vanadium oxide monomers, vanadium clusters work better because they provide several active sites working together to make the reaction go faster. The study shows that the reaction needs two sites closer together to work.
With the structure in hand, the next step is to understand why the tungsten-promoted reaction is more stable. Para esse fim, the team is now studying how the reaction could be different in an aged versus fresh SCR unit and, entre outras coisas, how water might affect the reaction. Em tempo, these findings may influence how SCR units are made.
Results of the study appear in the journal Angewandte Chemie .