Formação de radical aril por clivagem de ligação de haleto de aril por um catalisador de carbeno N-heterocíclico
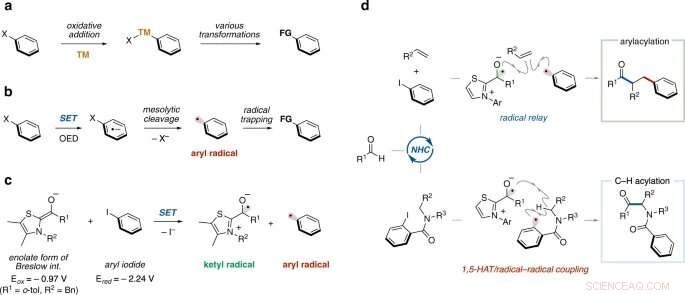 p a Adição oxidativa de haleto de arila ao metal de transição. TM, metal de transição. b Geração de radical arila induzida por doador de elétrons orgânicos (avanço recente). DEFINIR, transferência de um único elétron. OED, doador orgânico de elétrons. c Geração de radical arila através da catálise NHC (hipótese de trabalho). d Arilacilação de alqueno e C (sp
3
) –H acilação por catálise NHC (este trabalho). 1, 5-HAT, 1, Transferência de 5 átomos de hidrogênio.
p a Adição oxidativa de haleto de arila ao metal de transição. TM, metal de transição. b Geração de radical arila induzida por doador de elétrons orgânicos (avanço recente). DEFINIR, transferência de um único elétron. OED, doador orgânico de elétrons. c Geração de radical arila através da catálise NHC (hipótese de trabalho). d Arilacilação de alqueno e C (sp
3
) –H acilação por catálise NHC (este trabalho). 1, 5-HAT, 1, Transferência de 5 átomos de hidrogênio.
p Halogenetos de arila com um anel de benzeno diretamente ligado a um átomo de halogênio estão prontamente disponíveis e quimicamente estáveis, portanto, eles são usados como uma fonte de anéis de benzeno em síntese orgânica. Por exemplo, uma reação química que gera um radical arila altamente reativo a partir de um haleto de arila usando um composto tóxico de estanho é há muito conhecida como um método para fornecer um anel de benzeno. Nos últimos anos, foram desenvolvidas reações químicas nas quais um haleto de arila é reduzido usando um catalisador de metal ou um fotocatalisador seguido pela clivagem da ligação entre o anel de benzeno e o átomo de halogênio para gerar um radical arila. Contudo, uma vez que os métodos relatados anteriormente requerem sais de metal e / ou quantidades em excesso de um agente oxidante ou um agente redutor, reações químicas com menor impacto ambiental são desejáveis. p O grupo de pesquisa da Universidade de Kanazawa liderado pelo Prof. Ohmiya tem desenvolvido novas reações químicas usando catalisadores orgânicos livres de metal recentemente desenvolvidos para produzir vários produtos químicos úteis de uma maneira muito mais fácil do que com os métodos convencionais. No presente estudo, o grupo conseguiu gerar radicais aril a partir de iodetos de aril, um tipo de haleto de arila, sob condições amenas, sem a necessidade de luz ou sais metálicos, usando um catalisador carbeno N-heterocíclico e os radicais arila assim formados foram usados para sínteses orgânicas.
p Uma única transferência de elétrons de um intermediário enolato que consiste em um catalisador de carbeno heterocíclico N-tipo tiazólio e um aldeído para um iodeto de arila e a clivagem subsequente da ligação entre o anel de benzeno e o átomo de iodo geram um radical arila de uma maneira catalítica. Considerando o potencial de oxidação do intermediário enolato (Eox =-0,97 V) e o potencial de redução do iodeto de arila (Ered =-2,24 V), transferência de elétron único do intermediário enolato para o iodeto de arila, ou seja, redução de elétron único, é termodinamicamente desfavorável. Contudo, considera-se que a reação ocorreu devido a fatores cinéticos, pois as duas etapas da reação, i.e. 1) transferência de elétron único do intermediário enolato para o iodeto de arila e 2) clivagem da ligação entre o anel de benzeno e o átomo de iodo, proceda rapidamente. O radical aril gerado atua como uma fonte do anel de benzeno, a difuncionalização do alceno prossegue, e uma cetona substituída com anel de benzeno é obtida. Além disso, usando o radical aril gerado para a reação de abstração de hidrogênio intramolecular, a acilação desidrogenativa da amida prossegue, e pode ser obtido um composto de a-aminocetona. Substratos com vários grupos funcionais podem ser usados nessas reações de conversão molecular. Os derivados de produtos farmacêuticos também podem ser sintetizados pela acilação desidrogenativa de amidas.
p Os resultados deste estudo são o desenvolvimento de uma reação química que cliva a ligação entre o anel benzênico de um haleto de arila e o átomo de halogênio, usando um catalisador orgânico de baixo impacto no meio ambiente. levando à geração de um radical arila. Uma vez que os radicais de arila podem ser facilmente gerados a partir de haletos de arila que são amplamente usados em síntese orgânica, espera-se que seja uma tecnologia poderosa para sintetizar com precisão drogas médicas e agrícolas, bem como materiais químicos.
