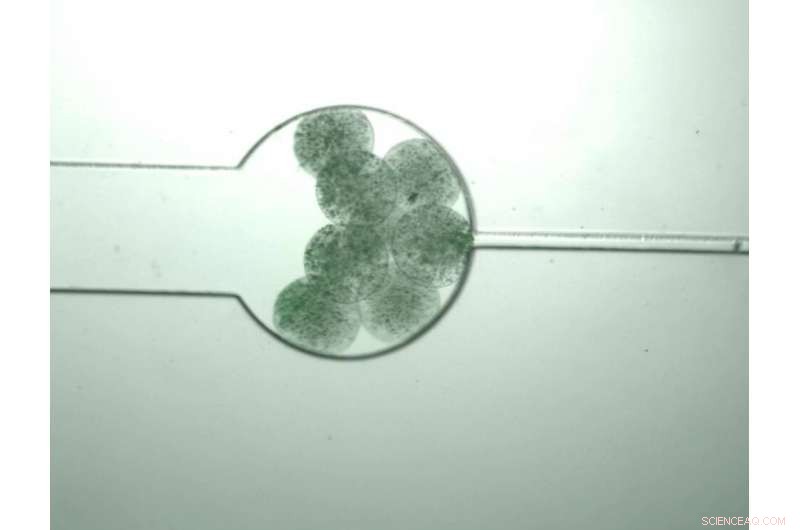
'Swarmbots, 'células vivas projetadas para produzir moléculas de monômero, crescer até sentirem que sua densidade populacional atingiu um certo nível, após o que eles se abriram, permitindo que os monômeros se misturem e se montem automaticamente em um polímero composto. Crédito:Zhuojun Dai
Os engenheiros biomédicos da Duke University demonstraram que uma classe de materiais compósitos entrelaçados chamados redes de polímero semi-interpenetrantes (sIPNs) podem ser produzidos por células vivas. A abordagem poderia tornar esses materiais versáteis mais compatíveis biologicamente para aplicações biomédicas, como sistemas de liberação de medicamentos com retardo de tempo.
A pesquisa aparece online no dia 8 de junho na revista. Nature Communications .
O conceito de sIPNs existe há mais de 100 anos e tem sido usado em peças automotivas, dispositivos médicos, compostos de moldagem e plásticos de engenharia. A ideia geral é que um ou mais polímeros sejam montados em torno de outro andaime de polímero de forma que fiquem interligados. Mesmo que os polímeros não sejam quimicamente ligados, eles não podem ser separados e formar um novo material com propriedades maiores do que a simples soma de suas partes.
Os métodos tradicionais de fabricação de SIPNs envolvem normalmente a produção das partes constituintes chamadas monômeros e sua mistura nas condições químicas corretas para controlar sua montagem em grandes redes em um processo chamado polimerização.
"Quando funcionar, é uma plataforma fantástica que pode incorporar diferentes funcionalidades na camada auto-montada para aplicações biomédicas ou ambientais, "disse Lingchong You, professor de engenharia biomédica na Duke. "Mas o processo geralmente não é tão biocompatível quanto você gostaria. Então, pensamos por que não usar células vivas para sintetizar a segunda camada para torná-la o mais biocompatível possível?"
No novo jornal, Zhuojun Dai, um ex-pós-doutorado no laboratório You que agora é professor associado do Instituto de Biologia Sintética de Shenzhen, usa uma plataforma que o laboratório vem desenvolvendo há vários anos chamada 'swarmbots' para fazer exatamente isso.
Os enxames são células vivas programadas para produzir moléculas biológicas dentro de suas paredes e explodir assim que sua população atingir uma determinada densidade. Nesse caso, eles são programados para produzir monômeros chamados polipeptídeos semelhantes a elastina (ELPs) fundidos a recursos funcionais chamados SpyTag e SpyCatcher. Essas duas estruturas moleculares formam um sistema de chave e fechadura, permitindo que as ELPs se automontem em uma cadeia de polímero quando misturadas. À medida que crescem, esses polímeros se enredam com as microcápsulas poliméricas contendo as células para formar sIPNs.
Cada monômero pode conter vários SpyTags ou SpyCatchers e também pode ser fundido a proteínas que geram uma leitura ou têm funções específicas. É como fazer uma cerca de arame com vários braceletes minúsculos que têm espaço para fechos e pingentes.
Os pesquisadores primeiro programam as células para preencher esse recurso acessável com uma proteína fluorescente para provar que o sistema pode travá-las no lugar. Depois dessa demonstração de sucesso, eles voltam sua atenção para a engenharia de um sistema de entrega de drogas útil com sua nova invenção.
"Você pode substituir o marcador fluorescente por qualquer coisa que tenha uma função que você deseja apresentar, "disse Você." Decidimos abordar os antibióticos porque é um dos outros focos do nosso laboratório. "
Antibióticos beta-lactâmicos, como a penicilina e seus derivados, são alguns dos antibióticos mais comumente usados no mundo. Eles também são usados em demasia e podem ter efeitos negativos, como destruir o microbioma natural que vive em nossas entranhas.
Para demonstrar uma maneira em que seus novos sIPNs construídos em células podem ser úteis, os pesquisadores preenchem o ponto acessável com beta-lactamase, que pode degradar os antibióticos beta-lactâmicos. Ao injetar os sIPNs recentemente funcionalizados em camundongos, os pesquisadores mostraram que a plataforma poderia liberar lentamente a molécula protetora de curta duração para ajudar os microbiomas intestinais dos camundongos a evitar os efeitos colaterais negativos dos antibióticos.
"Ninguém usou células vivas como fábrica para produzir monômeros em tempo real para sIPNs antes, "disse Você." A demonstração de prova de princípio mostra que, não só podemos fabricar esses tipos de materiais funcionais com células vivas, mas eles podem exibir funções medicamente relevantes. "