
Funcionalização de ligações éter. (A) Fármacos de moléculas pequenas contendo porções de éter cíclico. Ph, fenil; Ac, acetil; Beleza, benzoílo; glu, glicose. (B) Clivagem C-O catalisada por metal de transição via adição oxidativa. R, alquil; M, metal de transição; FG, grupo funcional; B2pin2, bis (pinacolato) diboro. (C) Inserção de carbeno em éteres ativados. (D) Derivados de boronato cíclico como candidatos a drogas ou reticulantes para materiais biomédicos. (E) Este trabalho:uma inserção direta de boro catalisada por Ni através de uma via de clivagem e rebote. Crédito:Ciência, 10.1126 / science.abg5526
A ligação carbono-oxigênio (C-O) em éteres alquílicos pode ser clivada usando métodos suaves para simplificar sínteses químicas elaborando robustos, precursores prontamente disponíveis. Em um novo relatório agora em Ciência , Hairong Lyu e uma equipe de pesquisa em química da University of Chicago e da University of Pittsburgh, Os EUA detalham como os dibromoboranos reagiram com éteres alquílicos na presença de um catalisador de níquel (Ni) e redutor de zinco para inserir boro na ligação C-O. A reatividade subsequente afetou a substituição de oxigênio por nitrogênio para agilizar a preparação de compostos bioativos de forma mais ampla. Usando estudos mecanísticos, a equipe revelou uma via de clivagem e recuperação via catálise tandem de zinco / níquel.
Metades de éter
Porções de éter são comumente encontradas em matéria-prima e produtos químicos finos; por exemplo, os éteres cíclicos são prevalentes em uma gama de moléculas biologicamente importantes, incluindo drogas, agroquímicos e produtos naturais. Os éteres também atuam como ligantes estruturais eficazes para proteger grupos na síntese orgânica devido à sua alta estabilidade química em relação aos ácidos, bases, redutores e oxidantes. Um método suave que edita diretamente uma porção substituindo o oxigênio ou inserindo um átomo interveniente na ligação C-O pode introduzir convenientemente um novo grupo funcional em um andaime existente em uma etapa estrategicamente importante. Os químicos podem usar éteres robustos como substitutos para grupos químicos mais sensíveis que podem ser instalados posteriormente. Lyu et al. foram inspirados por avanços recentes na química do borileno para funcionalizar ligações de éter inserindo uma espécie ativa de borileno.
Clivando ligações de alquil éter
Convencionalmente, ligações de éter alquílico podem ser clivadas sob condições severas e fortemente ácidas. Para estabelecer um método prático neste trabalho, Lyu et al. procurou evitar redutores fortes, catalisadores caros e condições de reação forçada. O estudo, portanto, começou com 2, 3-di-hidrobenzofurano como o subestado de éter modelo e dibromomesitilborano (MesBBr 2 ) como o reagente de boro. O grupo volumoso evitou a dimerização de espécies reduzidas de boro para aumentar a estabilidade do produto de inserção de boro para isolamento. O catalisador de níquel combinado com o pó de zinco foi mais eficaz. A equipe finalmente obteve o produto de inserção de boro desejado 2H-benzoxaborina (marcado com 3a) com 90% de rendimento em solução de tolueno a 60 graus Celsius. O caminho da reação foi totalmente diferente; eles usaram um complexo tetraédrico de Ni (II) estável ao ar abreviado (molécula Cat 1) e confirmaram sua estrutura usando cristalografia de raios-X para destacar sua superioridade em relação a outros pré-catalisadores de Ni ou outros metais. Na ausência de Cat1, eles notaram menos de 1 por cento de rendimento de 2H-benzoxaborina e um intermediário de brometo de alquila de abertura de anel (abreviado como 4a) para formar em alto rendimento. Outros complexos de níquel também deram o produto desejado, embora em rendimento muito menor. Lyu et al. observou eficiência semelhante usando um catalisador de níquel gerado in situ (abreviado como L1). Dado o papel crítico do catalisador de níquel, a equipe também examinou outros ligantes à base de nitrogênio. Os ligantes monodentados atuaram melhor do que os ligantes bidentados (marcados L1 a L7 e comparados com L8 a L12). Por exemplo, 3-metil piridina (L5) exibiu reatividade ligeiramente inferior, enquanto a maioria das outras monopiridinas (L2, L3, L4 e L6), bem como oxazolina (abreviado L7) foram comparativamente menos eficazes. Eles também usaram pó de zinco como um catalisador essencial e observaram a progressão da reação de inserção de boro em uma taxa de reação baixa em temperatura ambiente.
Borilação catalisada por níquel de éteres cíclicos. (A) Síntese de oxaborinanos via borilação direta de éteres cíclicos com cinco membros. Mim, metilo; Ar, arilo. (B) Síntese de oxaborepans via borilação direta de éteres cíclicos de seis membros. Ts, tosyl. (C) Síntese de oxaborolanos e azaborolidina via borilação direta de ciclooxabutanos e azetidina. (D) Síntese da oxazaborolidina via borilação direta de 4-fenil-morfolina. (E) Síntese de ácidos borínicos via borilação direta de éteres lineares. As reações foram conduzidas com 0,2 mmol de éter, 0,24 mmol MesBBr2, 0,01 mmol Cat 1, e 1 mmol de zinco em pó em 0,5 ml de tolueno a 60 ° C sob azoto durante 24 horas. Os rendimentos isolados após cromatografia em gel de sílica são dados; os números entre parênteses são rendimentos de ressonância magnética nuclear antes da purificação. * A reação foi realizada a 80 ° C. † A reação foi realizada a 100 ° C. ‡ 0,2 mmol de MesBBr2 foi usado. § A reação foi realizada a 130 ° C. ¶Ni (PMe3) 2Cl2 (0,01 mmol) foi usado como o catalisador, e a reacção decorreu a 130 ° C durante 18 horas. O tempo de reação foi de 36 horas. Crédito:Ciência, 10.1126 / science.abg5526 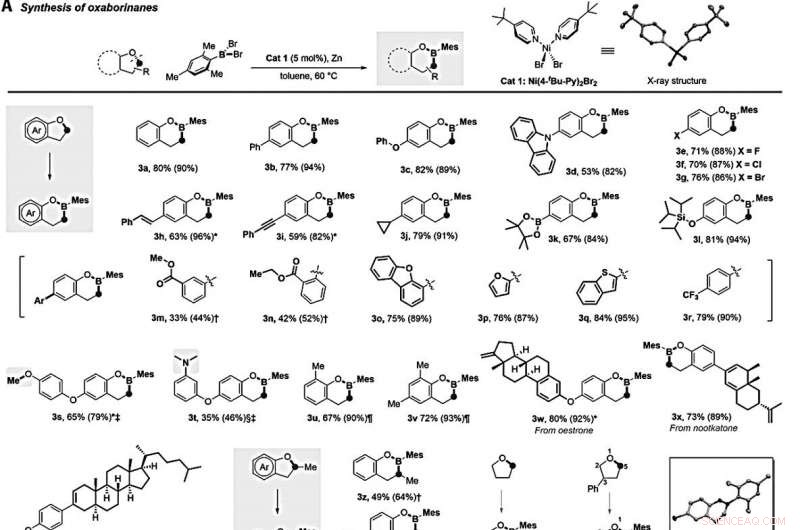
Lyu et al. examinou o escopo do éter para a reação de inserção de boro. Por exemplo, uma faixa de 2 substituídos, 3-dihidrobenzofuranos reagiram com MesBBr 2 (dibromomesitilborano) suavemente para formar os produtos de inserção de boro desejados com rendimentos bons a excelentes. Por exemplo, substratos contendo halogênios, incluindo flúor (F), cloro (Cl) e bromo (Br) foram submetidos a acoplamentos cruzados catalisados por níquel para formar 2H-benzoxaborinas (marcadas de 3e a 3g) com mais de 70 por cento de rendimento. Entre uma miríade de moléculas assim formadas, a equipe observou a tolerância de ambas as frações de boronato de pinacol e éter silílico durante esta reação. Outros experimentos de controle mostrarão como o cloreto de alquil primário é totalmente compatível, enquanto o brometo de alquil primário era parcialmente compatível sob as condições de reação. Adicionalmente, o fluoreto de alquil primário não foi tolerado devido às suas fortes interações de boro-fluoreto. Lyu et al. em seguida, substratos complexos derivados de produtos naturais de terpeno que sofreram suavemente a reação de inserção de boro e entregaram os produtos desejados em 3 vezes ou mais. Adicionalmente, o tetra-hidrofurano também deu o produto de inserção de monoboro esperado (rotulado como 3ab) com rendimento de 69 por cento. Quando a equipe usou o 3-fenil-tetra-hidrofurano assimétrico como parceiro de acoplamento, a inserção do boro ocorreu regiosseletivamente na posição menos volumosa para indicar a influência dos estéricos.
Inserção de boro em moléculas mais complexas.
Lyu et al. adicionalmente conduziu a inserção de boro em oxetanos mais tensos, também, para fornecer uma entrada para oxaborolanos de cinco membros (rotulados de 3ai a 3aj). A seletividade comprometida resultou em produtos colaterais lineares. Do ponto de vista da praticidade sintética, a equipe mostrou como a ligação B-Mes (boro-mesitil) poderia facilmente sofrer hidrólise em um único recipiente por meio da adição de água em metanol para fornecer os produtos de boronato de hidroxila correspondentes que são mais estáveis no ar. Os cientistas funcionalizaram boronatos cíclicos de prontamente disponíveis 2, 3-di-hidrobenzofuranos em uma etapa para desenvolver análogos de um medicamento antifúngico aprovado conhecido como tavaborol e crisaborol, um medicamento aprovado para tratar dermatite.
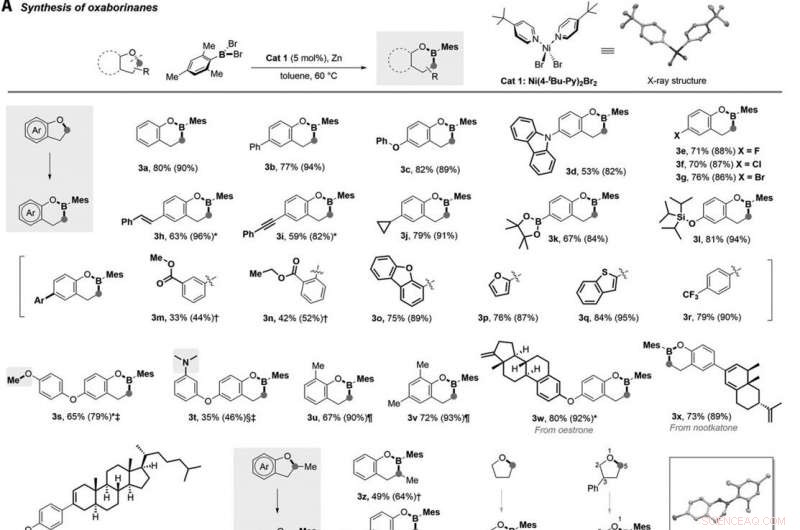
Elaboração sintética. (A) Acesso rápido a boronatos cíclicos por meio de hidrólise em um único recipiente. Os produtos de boronato (5a a 5c) são substancialmente mais estáveis em relação ao ar e à umidade. (B) Funcionalização adicional do produto de borylation através da derivatização da ligação C-B. Bn, benzil. (C) edição O-a-N para acessar pirrolidinas e piperidinas de tetra-hidrofuranos e tetra-hidropiranos, respectivamente. (D) Três abordagens para a expansão do anel de um carbono de éteres cíclicos. DIAD, azodicarboxilato de diisopropil. (E) Síntese simplificada do medicamento anti-hipertensivo nebivolol. Para protocolos de reação detalhados. Crédito:Ciência, 10.1126 / science.abg5526
Outras reações
A porção de boro nos produtos de inserção também pode ser convenientemente convertida em vários outros grupos funcionais. Por exemplo, a equipe poderia tratar o produto bruto (3a) 2H-benzoxaborina, com peróxido de hidrogênio para obter 1, 2-tirosol (6a) com excelente rendimento. O acoplamento Suzuki-Miyaura da molécula 3a com bromo-benzeno formou eficientemente o-fenetilfenol (marcado como 7a). O método também permitiu reações eficientes de expansão do anel de um carbono e proporcionou expansão do anel retentor de boro. Durante os experimentos, a natureza do grupo alquil na reação de acoplamento e o papel do catalisador de níquel foram fundamentais para entender as etapas subsequentes da formação da ligação carbono-boro.
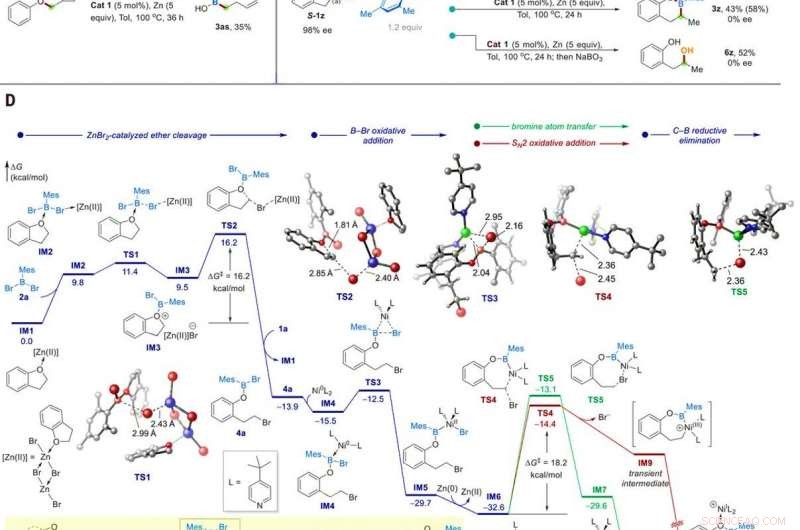
Estudos mecanísticos. (A) Identificação do intermediário da reação. (B) Experiência do relógio radical. (C) Experimentos de controle com um substrato de 98% ee. (D) Perfil de energia calculado da borilação catalítica do éter 1a. Os cálculos foram realizados no M06 / SDD-6311 + G (d, p) / SMD (tolueno) // B3LYP-D3 / SDD-6-31G (d) nível de teoria. A inserção mostra a catálise proposta em tandem de Zn / Ni. Crédito:Ciência, 10.1126 / science.abg5526
Panorama
Desta maneira, Hairong Lyu e colegas demonstraram um método para a inserção de boro em ligações de éter alquílico sob a catálise de níquel e zinco. Uma vez que os éteres estão prontamente disponíveis e são subestados robustos, o método de inserção de boro também pode agilizar a síntese de moléculas alvo complexas, minimizando as manipulações de grupos funcionais ou protegendo os usos de grupos. O modo de reação distinto revelado pelos estudos mecanísticos pode ter implicações nas reações de catálise em tandem de ácido de Lewis / metal de transição que estão além deste trabalho.
© 2021 Science X Network