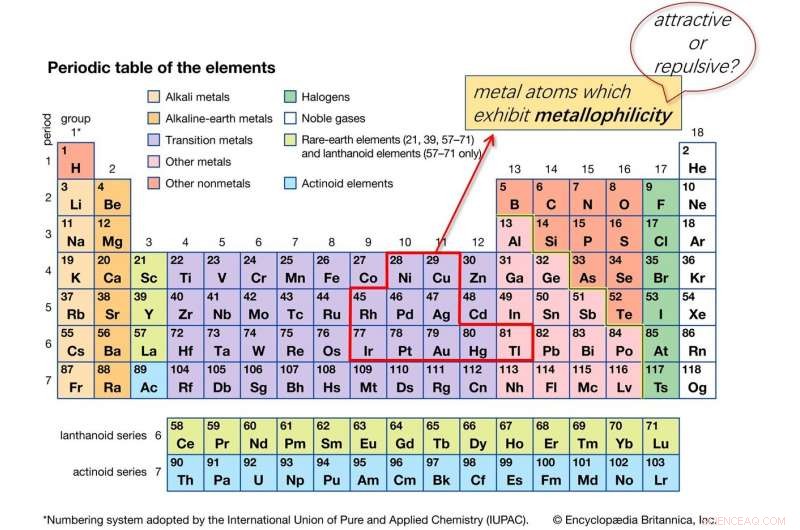
 p Tabela periódica mostrando elementos que podem exibir metalofilicidade. Crédito:Universidade de Hong Kong
p Tabela periódica mostrando elementos que podem exibir metalofilicidade. Crédito:Universidade de Hong Kong
p Uma equipe de pesquisa liderada pelo Professor Chi-Ming Che e Dr. Jun Yang, da Divisão de Pesquisa de Química e do Departamento de Química da Faculdade de Ciências da Universidade de Hong Kong, resolveu um problema fundamental de longa data no campo da interação metal-metal de concha fechada. Este trabalho foi publicado na revista
Proceedings of the National Academy of Sciences (PNAS) . p Interação de casca fechada Metal-Metal, também conhecido como metalofilicidade, tem um grande impacto em diversos campos da química, tais como química supramolecular e química organometálica. Os primeiros relatórios sobre metalofilicidade podem ser rastreados até a década de 1970. Muitos dos principais químicos teóricos em todo o mundo fizeram contribuições no campo, como Roald Hoffmann (Prêmio Nobel de Química de 1981), Pekka Pyykkӧ, etc. A metalofilicidade é importante na fabricação de automontagens por complexos de metais de transição, que demonstrou aplicações profundas em semicondutores orgânicos, bio-sensoriamento e materiais optoeletrônicos funcionais.
p
Indo além da sabedoria convencional
p O termo "metalofilicidade" originou-se da Europa e tem sido amplamente utilizado por químicos como um princípio orientador em estudos de design molecular e para racionalizar as propriedades espectroscópicas de complexos de metais de transição. Até agora, o consenso geral de metalofilicidade na comunidade acadêmica é "atraente, "que foi concebido para vir da hibridização orbital e / ou efeito relativístico do átomo de metal pesado, como ouro ou platina (metal da 3ª linha na tabela elemental). Junto com o professor Che e o Dr. Yang, O pós-doutorado Dr. Qingyun Wan e colegas questionaram a sabedoria convencional dos químicos de coordenação, concluindo que a metalofilicidade não é uma interação atrativa no complexo organometálico, mas é realmente repulsivo por natureza devido à forte repulsão M-M 'Pauli.
p Eles realizaram uma pesquisa combinada teórica e experimental sobre metalofilicidade e observaram forte repulsão M-M 'Pauli no complexo organometálico com configurações eletrônicas de concha fechada, que fornecerá uma nova perspectiva teórica sobre a possibilidade de fazer novos materiais supramoleculares com complexos baratos de metais de transição abundantes em terra, tais como paládio, prata ou níquel (metais de 1ª ou 2ª linha na tabela elementar). É também uma conquista crucial na compreensão fundamental das interações intermoleculares fracas.
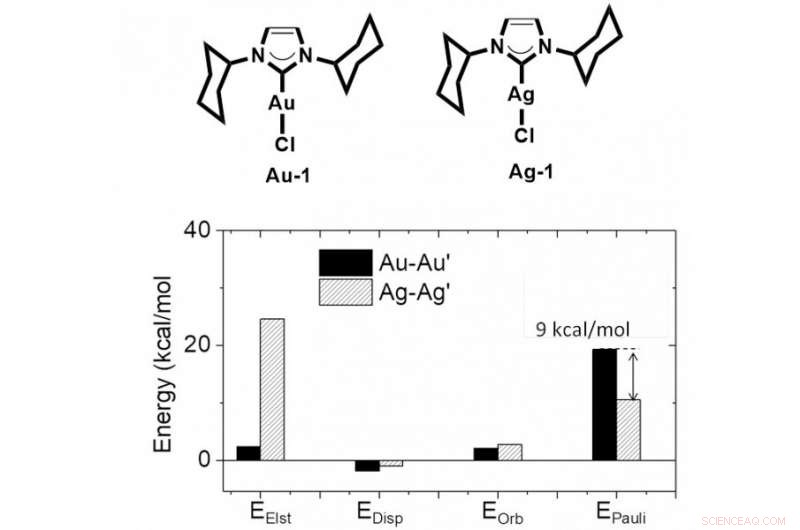 p Estrutura química do complexo Au (Elemento Ouro) e Ag (Elemento Prata), e os resultados do cálculo mostram uma repulsão Au-Au Pauli mais forte do que a repulsão Ag-Ag Pauli. Crédito:Universidade de Hong Kong
p Estrutura química do complexo Au (Elemento Ouro) e Ag (Elemento Prata), e os resultados do cálculo mostram uma repulsão Au-Au Pauli mais forte do que a repulsão Ag-Ag Pauli. Crédito:Universidade de Hong Kong
p
Histórico e conquistas
p No micromundo de pequenas moléculas, existem muitos tipos de interações. A metalofilicidade descreve a interação entre os átomos de metal como tendo configurações eletrônicas de concha fechada. No início dos anos 1970, os químicos observaram um fenômeno interessante:dois átomos de metal de concha fechada podem formar uma curta distância metal-metal. Uma "atração" especial foi proposta para existir entre dois átomos de metal, empurrando dois átomos de metal se aproximando. Muitos modelos teóricos foram criados para dar conta de tal apego, como o modelo de hibridização orbital ou efeito relativístico do metal pesado. Contudo, esses modelos teóricos têm conflitos com algumas observações de experimentos, como a distância Ag-Ag relativamente mais curta em complexos Ag em comparação com a distância Au-Au nos análogos de Au. Assim, este problema permaneceu controverso por muito tempo e sempre atormentou os químicos inorgânicos e teóricos.
p Os pesquisadores da HKU usaram métodos de cálculo de alto nível e técnicas experimentais para investigar um problema tão difícil, e provou que a metalofilicidade é de natureza repulsiva devido à forte repulsão M-M 'Pauli. Eles concluíram que a hibridização orbital e o efeito relativístico fortaleceriam a repulsão de Pauli metal-metal ao formar um contato metal-metal próximo. A dispersão intermolecular e a interação eletrostática irão contrabalançar a repulsão metal-metal, levando a uma curta distância metal-metal. Este modelo teórico poderia explicar bem por que a distância Ag-Ag é menor do que a distância Au-Au, devido à repulsão Ag-Ag Pauli mais fraca que é induzida por menos hibridização orbital no complexo Ag.
p Por uma estimativa conservadora, havia mais de 5, 000 artigos publicados na literatura relacionados à "metalofilicidade atrativa". A declaração de "metalofilicidade repulsiva" é proposta pela primeira vez pela equipe de pesquisa em sua recente publicação PNAS. Este trabalho também foi reconhecido pelo Professor Harry Gray em Caltech, que recebeu o Prêmio Wolf de Química em 2004, um dos prêmios mais honrosos da área.

