 p O cluster HPC "CARL" ajudou a decifrar o comportamento da molécula por meio de cálculos extensos. Crédito:Daniel Schmidt / Universidade de Oldenburg
p O cluster HPC "CARL" ajudou a decifrar o comportamento da molécula por meio de cálculos extensos. Crédito:Daniel Schmidt / Universidade de Oldenburg
p Como catalisadores moleculares - moléculas que, como enzimas, pode desencadear ou acelerar certas reações químicas - função, e que efeitos eles têm? Uma equipe de químicos da Universidade de Oldenburg chegou mais perto das respostas usando uma molécula modelo que funciona como uma nanobateria molecular. Consiste em vários centros de titânio ligados entre si por uma única camada de átomos de carbono e nitrogênio interconectados. A equipe de pesquisa de sete membros publicou recentemente suas descobertas, que combinam os resultados de três doutorados plurianuais. pesquisar projetos, no
ChemPhysChem . O jornal físico-química e física química apresentou a pesquisa básica de Oldenburg em sua capa. p Para obter uma melhor compreensão de como a molécula funciona, Os pesquisadores, liderado pelos primeiros autores Dr. Aleksandra Markovic e Luca Gerhards e o autor correspondente Prof. Dr. Gunther Wittstock, realizaram experimentos eletroquímicos e espectroscópicos e usaram o cluster de computação de alto desempenho da universidade para seus cálculos. Wittstock vê a publicação do artigo como uma "história de sucesso" para ambos os grupos de treinamento de pesquisa dentro dos quais o doutorado. projetos foram realizados e para o cluster de computação da universidade. "Sem a infraestrutura de computação de alto desempenho, não teríamos sido capazes de realizar os cálculos extensos necessários para decifrar o comportamento da molécula, "diz Wittstock." Isso sublinha a importância de tais clusters de computação para a pesquisa atual. "
p No papel, os autores apresentam os resultados de sua análise de uma estrutura molecular, o protótipo para o qual foi o resultado de uma reação química inesperada relatada pela primeira vez pelo Departamento de Química da Universidade de Oldenburg em 2006. É uma estrutura molecular altamente complexa na qual três centros de titânio (comumente referidos nas aulas do ensino médio como íons de titânio) estão conectados uns aos outros por um ligante de ponte consistindo de carbono e nitrogênio. Espera-se que tal composto seja capaz de aceitar e liberar vários elétrons por meio da troca de elétrons entre os centros de metal, entre outras razões.
A estrutura da molécula em estudo na Universidade de Oldenburg. O titânio é mostrado em vermelho, nitrogênio em azul, carbono na grea. O corpo básico da molécula é destacado, enquanto os átomos de hidrogênio estão ocultos para simplificação. Crédito:Imagens:Ruediger Beckhaus / Universidade de Oldenburg p Obter uma compreensão adequada desses processos é de interesse particular não apenas para a pesquisa básica, mas também para desencadear ou acelerar reações importantes nas quais mais de um elétron é transferido. Essas reações continuam sendo um grande desafio em sistemas técnicos, para o qual ainda não há solução satisfatória. “Muitos esforços estão atualmente focados neste objetivo, "diz Wittstock. Um exemplo é a tecnologia de células de combustível, que requer a transferência simultânea de quatro elétrons para uma molécula de oxigênio, a fim de atingir um fluxo de elétrons do hidrogênio para o oxigênio, ele explica. "Essas reações multieletrônicas também têm grande potencial para economizar materiais ou energia na produção química."
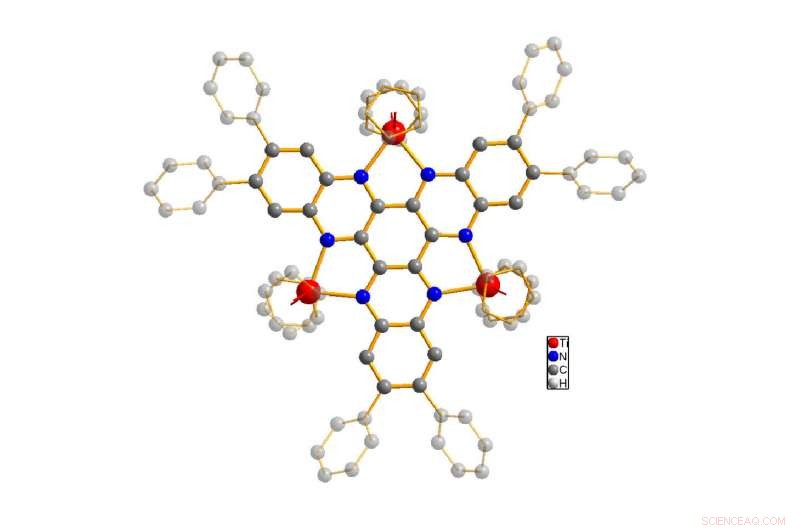 p A estrutura da molécula em estudo (titânio mostrado em vermelho, nitrogênio em azul, carbono em cinza). O corpo básico da molécula é destacado, enquanto os átomos de hidrogênio estão ocultos para simplificação. Crédito:Ruediger Beckhaus / Universidade de Oldenburg
p A estrutura da molécula em estudo (titânio mostrado em vermelho, nitrogênio em azul, carbono em cinza). O corpo básico da molécula é destacado, enquanto os átomos de hidrogênio estão ocultos para simplificação. Crédito:Ruediger Beckhaus / Universidade de Oldenburg
p O modelo de composto molecular que consiste no ligante em ponte e nos centros de titânio foi projetado especificamente para ajudar os cientistas a obter uma compreensão detalhada de como compostos com vários centros de metal são capazes de aceitar e liberar elétrons. Os cientistas animaram a molécula com a luz, ao qual as moléculas responderam de maneira diferente dependendo do número de elétrons aceitos e liberados. Infelizmente, a molécula feita em 2006 provou ser pouco solúvel na maioria dos solventes e, portanto, difícil de estudar. Usando síntese química, Dra. Pia Sander, um co-autor do artigo, adicionou motivos moleculares semelhantes a hélices ao composto para melhorar sua solubilidade. Isso forneceu a base para os experimentos de Markovic, que revelou que o composto do modelo poderia aceitar um total de três elétrons ou liberar seis elétrons - uma capacidade excepcionalmente alta para uma única molécula. Em cada uma dessas reações, não apenas a cor visível da molécula muda, mas a absorção de luz nas faixas espectrais que são invisíveis ao olho humano. Inicialmente, Contudo, as mudanças precisas na molécula com diferentes números de elétrons não puderam ser determinadas com base nessas faixas espectrais.
p Foi aí que Luca Gerhards e o cluster de computação da universidade entraram em ação. Embora as explicações comuns sejam baseadas na premissa de que em cada transição excitada pela luz apenas a energia de um único elétron muda, o co-autor Gerhards evitou essas suposições simplificadoras em suas equações químicas quânticas. Isso tornou os cálculos ainda mais complexos e manteve o cluster de computação de alto desempenho ocupado por meses. No fim, o resultado foi uma surpresa para todos os envolvidos:vários elétrons mudam seus níveis de energia simultaneamente quando a luz atinge a molécula em estudo. Além disso, esta carga não é armazenada no titânio, como seria de esperar, mas principalmente no ligante de ponte, a 'ligação' entre os centros de titânio.
p Como Wittstock explica, os centros de metal fornecem, assim, uma "estrutura" carregada positivamente para o armazenamento de elétrons, como em uma "nanobateria". A molécula modelo - e por extensão toda uma classe de compostos semelhantes - acabou sendo um "minissegmento de um material de armazenamento de energia". Embora seu potencial total não possa ser determinado nesta fase, Wittstock acredita que tais "quadros" com motivos de armazenamento de carga molecular podem se tornar um novo elemento de design em catalisadores moleculares complexos para reações de múltiplos elétrons.

