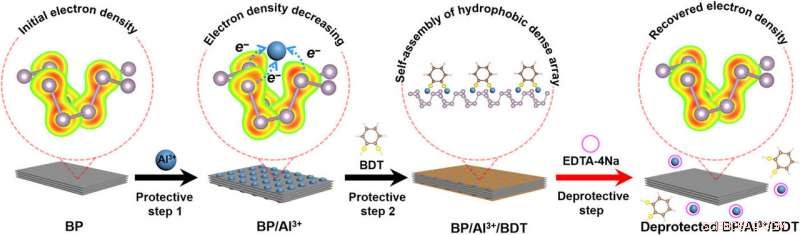
 p Ilustração esquemática da regulação da reatividade da BP via química protetora. Etapa de proteção 1:a ligação de íons Al3 + com pares de elétrons solitários na superfície dos átomos de P diminui a densidade de elétrons da superfície de BP, levando a uma reatividade química reduzida do BP. Etapa de proteção 2:A automontagem da matriz hidrofóbica densa na superfície do BP isola o BP do oxigênio / água circundante. Etapa desprotetora:Remoção de íons Al3 + e matriz densa hidrofóbica na superfície do BP por um agente quelante. O tratamento recupera a densidade eletrônica da BP, restaurando a reatividade original do BP desprotegido. BDT, 1, 2-benzenoditiol; EDTA-4Na, EDTA-tetrassódico. Crédito:Science Advances, doi:10.1126 / sciadv.abb4359.
p Ilustração esquemática da regulação da reatividade da BP via química protetora. Etapa de proteção 1:a ligação de íons Al3 + com pares de elétrons solitários na superfície dos átomos de P diminui a densidade de elétrons da superfície de BP, levando a uma reatividade química reduzida do BP. Etapa de proteção 2:A automontagem da matriz hidrofóbica densa na superfície do BP isola o BP do oxigênio / água circundante. Etapa desprotetora:Remoção de íons Al3 + e matriz densa hidrofóbica na superfície do BP por um agente quelante. O tratamento recupera a densidade eletrônica da BP, restaurando a reatividade original do BP desprotegido. BDT, 1, 2-benzenoditiol; EDTA-4Na, EDTA-tetrassódico. Crédito:Science Advances, doi:10.1126 / sciadv.abb4359.
p Os químicos podem regular racionalmente a reatividade de moléculas e grupos funcionais em processos de química orgânica sintética industrial e laboratorial. O conceito pode ser aplicado a nanomateriais inorgânicos, incluindo nanofolhas bidimensionais (2-D) de fósforo preto (BP). Por exemplo, os cientistas podem "desligar" a alta reatividade de fósforo preto de poucas camadas ou monocamada, quando o composto não está em uso, para retomar sua atividade mediante solicitação. Em um novo relatório agora publicado em
Avanços da Ciência , Xiao Liu e uma equipe de cientistas da física, biomateriais, A engenharia química e a química biológica na China desenvolveram um método de proteção baseado na química para regular a reatividade do fósforo preto. p Para iniciar a etapa de proteção, eles ligaram cátions de alumínio (Al
3+
) com pares de elétrons isolados do fósforo preto (BP) e diminuiu a densidade do elétron na superfície do fósforo preto. Eles concluíram o processo com uma camada resistente a oxigênio / água por meio da automontagem de hidrofóbico (ódio à água) 1, 2-benzenoditiol (BDT) no fósforo preto / alumínio (BP / Al
3+
) conjugado. A etapa de proteção produziu um composto estável com baixa reatividade. Usando um processo de tratamento quelante, Liu et al. subsequentemente alcançou a desproteção do BP / Al
3+
/ Complexo BDT para remover cátions de alumínio e BDT da superfície do fósforo preto. Desta maneira, eles recuperaram a densidade de elétrons do fósforo preto usando o processo de desproteção para restaurar a reatividade ao composto.
p
Ajustando as propriedades dos nanomateriais
p Liu et al. desenvolveu racionalmente um método de proteção baseado em química para controlar a reatividade do fósforo preto durante este trabalho. Na nanociência, os pesquisadores podem ajustar com precisão as propriedades dos nanomateriais para obter as características desejadas. Regular a reatividade dos nanomateriais é fundamental para aplicativos programáveis em várias etapas. Alguns nanomateriais podem ser protegidos para reduzir sua reatividade sob condições específicas e restaurar a atividade após uma desproteção bem-sucedida. Os pesquisadores, portanto, propuseram uma série de estratégias seletivas e eficientes para regular a reatividade de grupos funcionais em química orgânica.
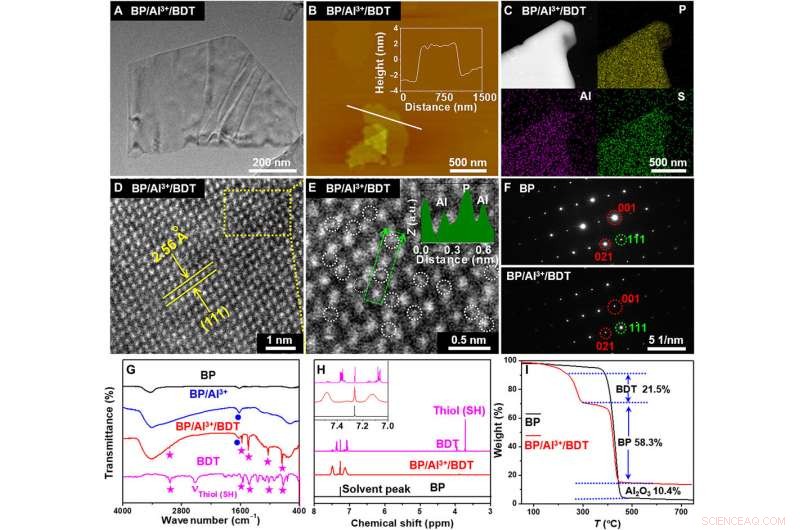 p Caracterização de BP / Al3 + / BDT. (A) Imagem TEM. (B) Imagem AFM (perfil de altura ao longo da linha branca). (C) Imagens de mapeamento elementar de espectroscopia de raios-x dispersiva de energia STEM (EDX). (D) Imagem de campo escuro anular de alto ângulo (HAADF). (E) Imagem HAADF ampliada tirada da área selecionada em (D). a.u .:unidades arbitrárias. (F) Padrão de difração de elétrons de área selecionada (SAED) de BP e BP / Al3 + / BDT. (G) espectros de FTIR de BP, BP / Al3 +, BP / Al3 + / BDT, e BDT. (H) Espectro de 1H NMR de BP, BP / Al3 + / BDT, e BDT. (I) Curvas termogravimétricas de BP e BP / Al3 + / BDT. ppm, partes por milhão. Crédito:Science Advances, doi:10.1126 / sciadv.abb4359.
p Caracterização de BP / Al3 + / BDT. (A) Imagem TEM. (B) Imagem AFM (perfil de altura ao longo da linha branca). (C) Imagens de mapeamento elementar de espectroscopia de raios-x dispersiva de energia STEM (EDX). (D) Imagem de campo escuro anular de alto ângulo (HAADF). (E) Imagem HAADF ampliada tirada da área selecionada em (D). a.u .:unidades arbitrárias. (F) Padrão de difração de elétrons de área selecionada (SAED) de BP e BP / Al3 + / BDT. (G) espectros de FTIR de BP, BP / Al3 +, BP / Al3 + / BDT, e BDT. (H) Espectro de 1H NMR de BP, BP / Al3 + / BDT, e BDT. (I) Curvas termogravimétricas de BP e BP / Al3 + / BDT. ppm, partes por milhão. Crédito:Science Advances, doi:10.1126 / sciadv.abb4359.
p Contudo, os processos protetores-desprotetores orgânicos bem estabelecidos existentes não podem ser aplicados a nanomateriais inorgânicos devido à falta de grupos funcionais semelhantes. Como resultado, uma abordagem eficiente e simples para controlar a reatividade de materiais inorgânicos ainda precisa ser desenvolvida. Para conseguir isso, a equipe começou a ligar o fósforo preto com cátions de alumínio (Al
3+
) para diminuir a densidade de elétrons de superfície e diminuir efetivamente sua reatividade. O processo de proteção produziu um arranjo do tipo hidrofóbico (ódio à água) 1, Molécula de 2-benezenditiol (BDT) na presença de fósforo preto e Al
3+
cátions para oferecer um complexo ultra-estável (BP / Al
3+
/ BDT). O composto foi estável em condições ambientais por até dois meses sem alterações. A equipe pode desproteger o complexo instável por meio do tratamento quelante.
p
Síntese e caracterização do BP / Al
3+
/ Composto BDT
p Liu et al. sintetizou e caracterizou (testou) o fósforo negro em massa (BP) seguindo um método desenvolvido anteriormente. A equipe obteve primeiro nanofolhas BP através da sonicação da forma em pó da molécula, em seguida, usando microscopia eletrônica de varredura e microscopia eletrônica de transmissão (TEM), eles observaram o tamanho da PA. O TEM de alta resolução também forneceu informações sobre a estrutura da nanofolha e a microscopia de força atômica revelou a espessura do BP com quatro a seis camadas individuais de fosforeno. Usando difração de raios-X e espectros Raman, a equipe determinou que as características do cristal de BP são semelhantes à sua forma volumosa. Na etapa de proteção da ligação catiônica à superfície do BP, Liu et al. BP misturado com cloreto de alumínio (AlCl
3 ) em uma solução de etanol. Eles então caracterizaram o apego bem-sucedido de Al
3+
cátions para a superfície do BP para fortalecer a proteção do BP, empregando espectroscopia de fotoelétrons de raios-X. A equipe observou a nanomorfologia do composto e estudou a conformação da superfície usando microscopia eletrônica de transmissão de varredura (STEM) e ainda verificou sua estrutura com espectroscopia de infravermelho com transformada de Fourier (FTIR) e ressonância magnética nuclear de próton (
1
HNMR).
p
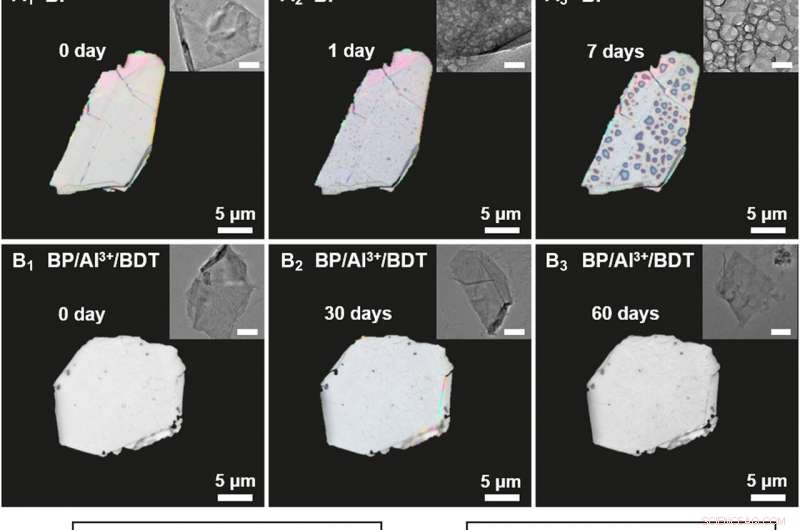 p Caracterização de BP e BP / Al3 + / BDT degradados em condições ambientais. Polarizando imagens de microscópio de (A) BP em massa (0, 1, e 7 dias) e (B) BP / Al3 + / BDT em massa (0, 30, e 60 dias). Inserções:imagens TEM correspondentes. Barras de escala, 200 nm. (C e D) Espectros HR-XPS de picos P 2p para BP e BP / Al3 + / BDT com exposição ambiente por várias durações. (E e F) Espectros de UV-vis de BP e BP / Al3 + / BDT dispersos em água por várias durações. Inserções:variação das razões de absorção UV-vis em 470 nm (A / A0) de BP (A0:valor original). Crédito:Science Advances, doi:10.1126 / sciadv.abb4359
Regulando a reatividade do BP / Al
3+
/ Composto BDT
p Caracterização de BP e BP / Al3 + / BDT degradados em condições ambientais. Polarizando imagens de microscópio de (A) BP em massa (0, 1, e 7 dias) e (B) BP / Al3 + / BDT em massa (0, 30, e 60 dias). Inserções:imagens TEM correspondentes. Barras de escala, 200 nm. (C e D) Espectros HR-XPS de picos P 2p para BP e BP / Al3 + / BDT com exposição ambiente por várias durações. (E e F) Espectros de UV-vis de BP e BP / Al3 + / BDT dispersos em água por várias durações. Inserções:variação das razões de absorção UV-vis em 470 nm (A / A0) de BP (A0:valor original). Crédito:Science Advances, doi:10.1126 / sciadv.abb4359
Regulando a reatividade do BP / Al
3+
/ Composto BDT
p Liu et al. investigou a reatividade do BP / Al
3+
/ BDT complexo, empregando uma variedade de técnicas ópticas em ciência dos materiais para compreender sua estrutura. As imagens correspondentes mostraram a evolução da estrutura cristalina e a estabilidade de longo prazo nas condições ambientais. A estabilidade do BP / Al
3+
/ O complexo BDT foi superior ao fósforo preto sozinho e os resultados destacaram a praticidade de incorporar o fósforo preto no composto. A equipe creditou a reatividade reduzida da estrutura complexa a dois fatores; primeiro, o cátion alumínio se ligando à superfície do fósforo preto tornou a reatividade química mais baixa. Segundo, a matriz densa hidrofóbica automontada na superfície do fósforo preto isolou a molécula do oxigênio e da água para evitar degradação posterior, melhorando a estabilidade do composto.
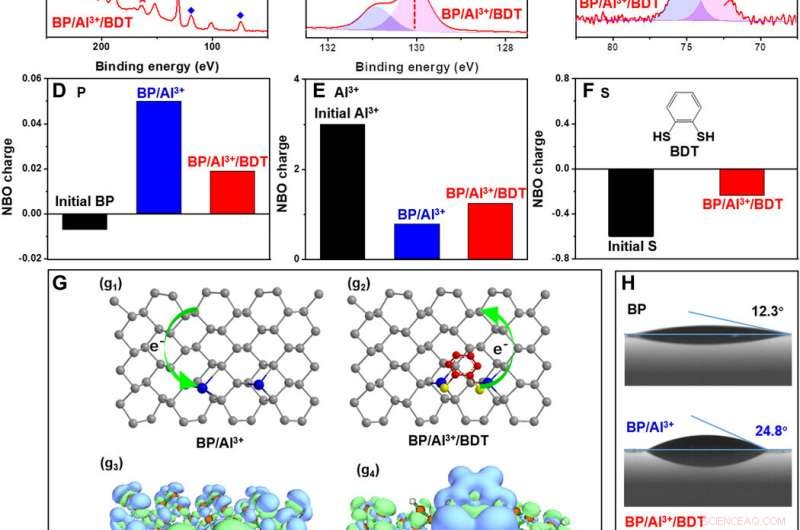 p Mecanismo de redução de reatividade em BP protegido. (A) Espectros XPS completos de BP, BP / Al3 +, e BP / Al3 + / BDT. (B e C) espectros HR-XPS de P 2p e Al 2p. (D a F) Carga NBO calculada do átomo P, Íon Al3 +, e átomo S. Modelo de estrutura de (G1) BP / Al3 + e (G2) BP / Al3 + / BDT. Mapeamento computacional da diferença de densidade eletrônica em (G3) BP / Al3 + e (G4) BP / Al3 + / BDT. As regiões verdes indicam aumento da densidade de elétrons, e as regiões azuis indicam densidade de elétrons diminuída. Os contornos são mostrados em 0.0001 a.u. nível. (H) Ângulos de contato de água de BP, BP / Al3 +, e BP / Al3 + / BDT. Crédito:Science Advances, doi:10.1126 / sciadv.abb4359.
p Mecanismo de redução de reatividade em BP protegido. (A) Espectros XPS completos de BP, BP / Al3 +, e BP / Al3 + / BDT. (B e C) espectros HR-XPS de P 2p e Al 2p. (D a F) Carga NBO calculada do átomo P, Íon Al3 +, e átomo S. Modelo de estrutura de (G1) BP / Al3 + e (G2) BP / Al3 + / BDT. Mapeamento computacional da diferença de densidade eletrônica em (G3) BP / Al3 + e (G4) BP / Al3 + / BDT. As regiões verdes indicam aumento da densidade de elétrons, e as regiões azuis indicam densidade de elétrons diminuída. Os contornos são mostrados em 0.0001 a.u. nível. (H) Ângulos de contato de água de BP, BP / Al3 +, e BP / Al3 + / BDT. Crédito:Science Advances, doi:10.1126 / sciadv.abb4359.
p
Desprotegendo o BP / Al
3+
/ Composto BDT
p A equipe de pesquisa desprotegeu o complexo ultraestável removendo o cátion alumínio da superfície do composto. Eles realizaram esta etapa com um quelante de íon metálico convencional - edetato de sódio (EDTA-4Na). Durante o processo, Liu et al. também removeu as moléculas BDT hidrofóbicas juntamente com cátions de alumínio, para obter a superfície hidrofílica resultante (amante da água) com potencial zeta negativo, semelhante em forma à molécula de fósforo preto original. O processo de regulação protetora-desprotetora permitiu aos cientistas controlar reversivelmente a reatividade do fósforo preto. Os resultados sugerem a capacidade de regular com eficiência a reatividade da molécula na prática.
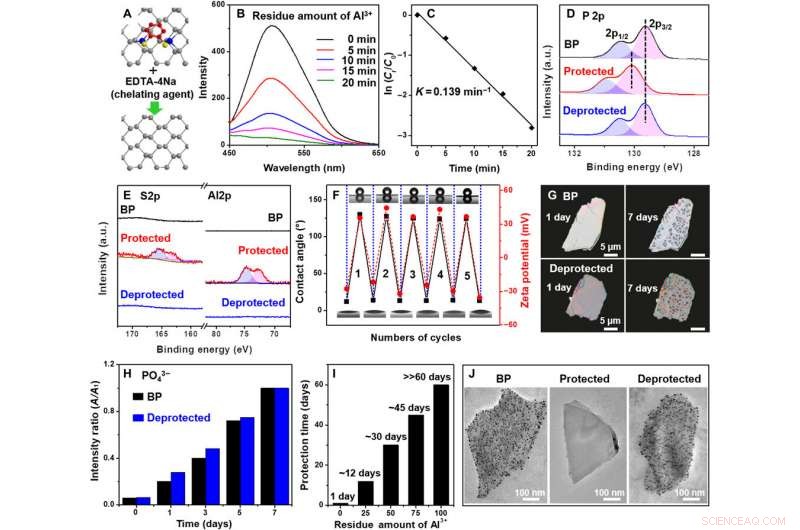 p Desproteção de BP / Al3 + / BDT. (A) Ilustração esquemática do íon Al3 + e remoção de BDT por EDTA-4Na. (B) Espectros de emissão de fotoluminescência (PL) de resíduo de Al3 + em BP / Al3 + / BDT após tratamento com EDTA-4Na. (C) Gráfico de ln (Ct / C0) em função do tempo de tratamento com EDTA-4Na. (D e E) espectros HR-XPS de P 2p, Al 2p, e S 2p para BP, BP / Al3 + / BDT, e BP / Al3 + / BDT desprotegido. (F) Gráficos de ângulos de contato com a água e potenciais zeta de BP medidos em cada ciclo protetor-desprotetor. (G) Imagens de microscópio de polarização de BP em massa (0 e 7 dias) e BP desprotegido em massa / Al3 + / BDT (0 e 7 dias). (H) Variação da concentração de PO43− em soluções de BP e BP / Al3 + / BDT desprotegidos com durações de exposição ambiente variáveis. (I) Estabilidade de BP / Al3 + / BDT desprotegido com uma quantidade residual variável de íon Al3 + na superfície de BP. (J) Imagens TEM de BP, BP / Al3 + / BDT, e BP / Al3 + / BDT desprotegido após tratamento com HAuCl4 (solução aquosa). Crédito:Science Advances, doi:10.1126 / sciadv.abb4359.
p Desproteção de BP / Al3 + / BDT. (A) Ilustração esquemática do íon Al3 + e remoção de BDT por EDTA-4Na. (B) Espectros de emissão de fotoluminescência (PL) de resíduo de Al3 + em BP / Al3 + / BDT após tratamento com EDTA-4Na. (C) Gráfico de ln (Ct / C0) em função do tempo de tratamento com EDTA-4Na. (D e E) espectros HR-XPS de P 2p, Al 2p, e S 2p para BP, BP / Al3 + / BDT, e BP / Al3 + / BDT desprotegido. (F) Gráficos de ângulos de contato com a água e potenciais zeta de BP medidos em cada ciclo protetor-desprotetor. (G) Imagens de microscópio de polarização de BP em massa (0 e 7 dias) e BP desprotegido em massa / Al3 + / BDT (0 e 7 dias). (H) Variação da concentração de PO43− em soluções de BP e BP / Al3 + / BDT desprotegidos com durações de exposição ambiente variáveis. (I) Estabilidade de BP / Al3 + / BDT desprotegido com uma quantidade residual variável de íon Al3 + na superfície de BP. (J) Imagens TEM de BP, BP / Al3 + / BDT, e BP / Al3 + / BDT desprotegido após tratamento com HAuCl4 (solução aquosa). Crédito:Science Advances, doi:10.1126 / sciadv.abb4359.
p
Panorama
p Desta maneira, Xiao Liu, e colegas desenvolveram uma nova abordagem baseada na química protetora para regular racionalmente a reatividade do fósforo preto (BP). Durante a etapa de proteção, eles ligaram cátions de alumínio (Al
3+
) ao único par de elétrons no BP para diminuir sua densidade de elétrons de superfície. Esta etapa de proteção aumentou a funcionalização do hidrofóbico (ódio à água) 1, 2-benezenditiol (BDT), na BP / Al
3+
superfície conjugada para formar uma camada hidrofóbica densa, o que reduziu bastante a reatividade do fósforo preto. A equipe então usou um quelador para remover os cátions de alumínio do fósforo preto para reverter a molécula de volta à sua alta densidade de elétrons original, superfície hidrofílica (que adora água). O BP desprotegido apresentou alta reatividade em seu estado original. O método forneceu uma abordagem ajustável para manipular a reatividade do BP, o que é difícil de conseguir por meio da funcionalização convencional. Esta estratégia de proteção pode ser explorada para regular a reatividade dos nanomateriais para criar nanoestruturas programáveis futurísticas para aplicações na ciência dos materiais. p © 2020 Science X Network




