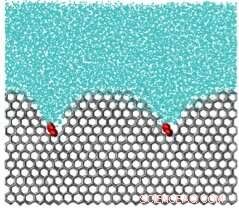
Uma simulação de uma molécula inibidora de gelo. A molécula, em vermelho, é como um peso na superfície do cristal de gelo, curvando-o e evitando o crescimento de cristais de gelo. Crédito:Universidade de Utah
As terapias celulares são uma grande promessa para revolucionar o tratamento de cânceres e doenças auto-imunes. Mas esta indústria multibilionária requer armazenamento de longo prazo de células em condições criogênicas superfrias, enquanto garante que eles continuarão a funcionar após o descongelamento. Contudo, essas temperaturas frias desencadeiam a formação e crescimento de gelo, que pode perfurar e separar as células. Pesquisa publicada no Jornal da American Chemical Society pelos químicos Pavithra Naullage e Valeria Molinero da Universidade de Utah fornecem a base para projetar polímeros eficientes que podem prevenir o crescimento de gelo que danifica as células.
Anticongelante da natureza
As estratégias atuais para criopreservar células e órgãos envolvem banhá-los com grandes quantidades de dimetilsulfóxido, um produto químico tóxico que atrapalha a formação de gelo, mas estressa as células, diminuindo suas chances de sobrevivência.
Natureza, Contudo, descobriu uma maneira de manter os organismos vivos em condições de frio extremo:proteínas anticongelantes. Peixe, insetos e outros organismos de sangue frio desenvolveram potentes glicoproteínas anticongelantes que se ligam aos cristais de gelo e os impedem de crescer e danificar as células.
A crescente área da terapêutica baseada em células exige o desenvolvimento de inibidores potentes de recristalização de gelo que podem competir em atividade com glicoproteínas anticongelantes naturais, mas não têm o custo e a toxicidade do dimetilsulfóxido. Essa demanda tem impulsionado a síntese de polímeros que mimetizam a ação das glicoproteínas anticongelantes. Mas o inibidor de recristalização de gelo sintético mais potente encontrado até hoje, álcool polivinílico (PVA), é ordens de magnitude menos potentes do que as glicoproteínas naturais.
"Os esforços para identificar inibidores mais fortes para o crescimento do gelo parecem ter estagnado, como ainda não há uma compreensão molecular dos fatores que limitam a eficiência de inibição da recristalização de gelo dos polímeros, "Molinero diz.
Uma variável de design de polímero oculta
Como as moléculas evitam que os cristais de gelo fiquem maiores? Moléculas que se ligam fortemente ao gelo fixam sua superfície - como pedras em um travesseiro - fazendo com que a frente do gelo desenvolva uma superfície curva ao redor das moléculas. Esta curvatura desestabiliza o cristal de gelo, detendo seu crescimento. As moléculas que permanecem presas ao gelo por muito mais tempo do que o tempo necessário para o crescimento dos cristais de gelo conseguem impedir o crescimento e a recristalização.
Molinero e Naullage usaram simulações moleculares em grande escala para elucidar as bases moleculares de como a flexibilidade, comprimento e funcionalização de polímeros controlam sua ligação ao gelo e sua eficiência para prevenir o crescimento de gelo. Seu estudo mostra que o tempo limite das moléculas na superfície do gelo é controlado pela força de sua ligação ao gelo juntamente com o comprimento do polímero e a velocidade com que se propagam na superfície do gelo.
"Descobrimos que a eficiência dos polímeros flexíveis em travar o crescimento do gelo é limitada pela propagação lenta de sua ligação ao gelo, "Molinero diz.
O estudo disseca os vários fatores que controlam a ligação de polímeros flexíveis ao gelo e que são responsáveis pela lacuna na potência do PVA e das glicoproteínas anticongelantes naturais. Em poucas palavras, cada bloco de glicoproteínas anticongelantes se liga mais fortemente ao gelo do que o PVA, e também são favorecidos por sua estrutura molecular secundária que separa os blocos de ligação e não ligação para permitir que eles se fixem mais rapidamente ao gelo para interromper seu crescimento.
"Para nosso conhecimento, este trabalho é o primeiro a identificar o tempo de propagação da ligação como uma variável-chave no projeto de polímeros flexíveis de ligação em gelo eficientes, "Naullage diz." Nosso estudo prepara o terreno para o design de novo de polímeros flexíveis que podem atender ou mesmo superar a eficiência das glicoproteínas anticongelantes e ter um impacto na pesquisa biomédica. "