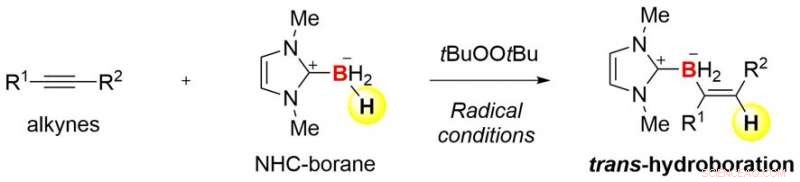
Visão geral da presente pesquisa Crédito:Kanazawa University
Uma combinação de organoboro e química radical gera trans-seletividade incomum na hidroboração de alcinos. O uso de carbenoboranos N-heterocíclicos é a chave para o sucesso dessa transformação química. Espera-se que este estudo abra as portas para o desenvolvimento de novos materiais contendo boro.
Compostos de organoboro têm sido amplamente usados para criar novas moléculas orgânicas desde o Prof. Suzuki, vencedor do Prêmio Nobel de Química em 2010, desenvolveram reações de acoplamento cruzado catalisadas por paládio com compostos de organoboro (acoplamento de Suzuki). Além disso, muitos compostos contendo boro são eles próprios materiais promissores. Eles podem ser usados como medicamentos e materiais orgânicos de eletro-luminescência devido à natureza eletrônica única do boro.
Borano (BH3) e seus derivados estabilizados por ligantes são os compostos de boro mais simples. Eles podem reagir com uma ligação tripla carbono-carbono (alcino, C-C) para produzir um produto de inserção (H-C =C-BH 2 ) Esta reação, chamado de hidroboração, é um método poderoso para preparar compostos de organoboro. Contudo, a reação normalmente fornece apenas um produto cis, o que significa que H e BH 2 são introduzidos no mesmo lado da ligação tripla. Isso é, é difícil sintetizar um produto de trans-hidroboração com a configuração geométrica oposta. Anteriormente, tem havido exemplos muito limitados de trans-hidroboração de alcinos.
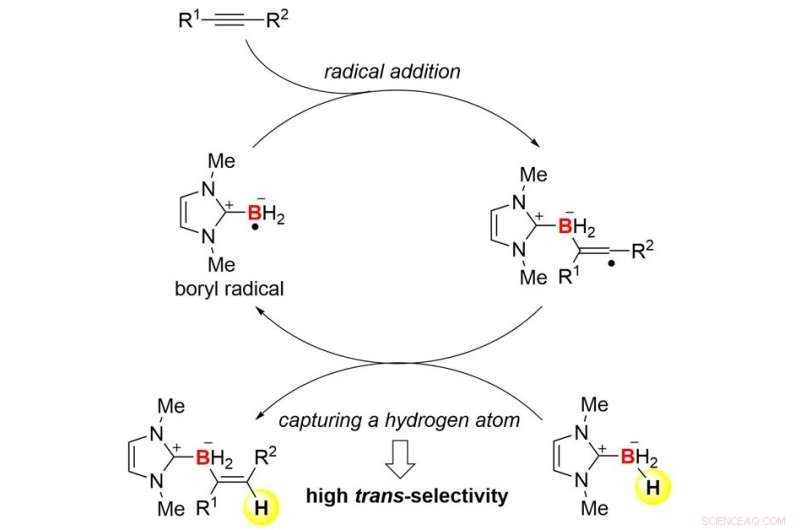
Esboço do mecanismo de reação. Crédito:Kanazawa University
A equipe de colaboração entre a Universidade de Kanazawa e a Universidade de Pittsburgh teve sucesso no desenvolvimento de reações de trans-hidroboração de alcinos com base na química radical (Figura 1). A equipe empregou carbenoboranos N-heterocíclicos (NHC-boranos) para combinar hidroboração com química radical. NHC-boranos podem ser manuseados facilmente devido à sua estabilidade, e eles são bons precursores de radicais boryl (radicais centrados em boro). De fato, um radical NHC-borila pode ser facilmente formado por termólise simples na presença de peróxido de di-terc-butila comercial barato. O radical pode se somar a um alcino para formar uma ligação carbono-boro (C-B) e um novo radical de carbono (Figura 2). A trans-seletividade na hidroboração é induzida cineticamente quando o radical de carbono altamente reativo captura um átomo de hidrogênio do NHC-borano de partida. Como resultado, o processo geral estabelece um ciclo de cadeia radical. Este mecanismo é bastante diferente daquele das reações de hidroboração conhecidas.
A partir de alcinos facilmente disponíveis, o presente protocolo fornece vários compostos alquenil borano estáveis em bancada que não são facilmente acessíveis por métodos conhecidos. Alguns deles podem ser convertidos em mímicos de retinoides, que são candidatos a drogas, por acoplamento Suzuki modificado (Figura 3).
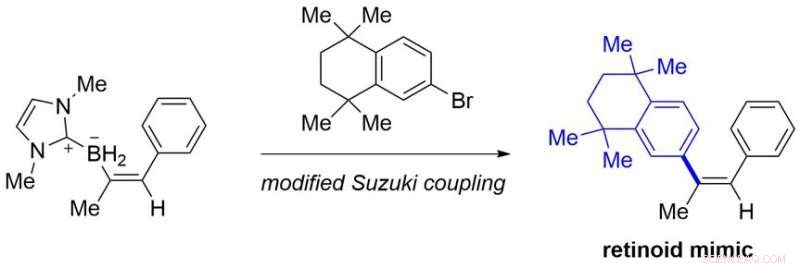
A aplicação de um produto sintetizado. Crédito:Kanazawa University
Os compostos organoboron sintetizados pelo presente método darão acesso a novos sistemas π contendo boro por meio de transformação química posterior. Portanto, este tipo de reação de transhidroboração facilitará os avanços na química medicinal e na ciência dos materiais. Do ponto de vista da química pura, este estudo expande o potencial dos radicais na química sintética. Resumidamente, ilustramos que os radicais são capazes de controlar as reações químicas com precisão, apesar de sua extrema reatividade.
Dennis Curran (Universidade de Pittsburgh), um colaborador neste estudo, diz, "Foi um prazer estar envolvido nesta colaboração, que foi liderado pela equipe Kanazawa. A nova reação que descobrimos é única, e estou entusiasmado com suas perspectivas de extensão nas direções tanto de pesquisa básica quanto de aplicações práticas. "