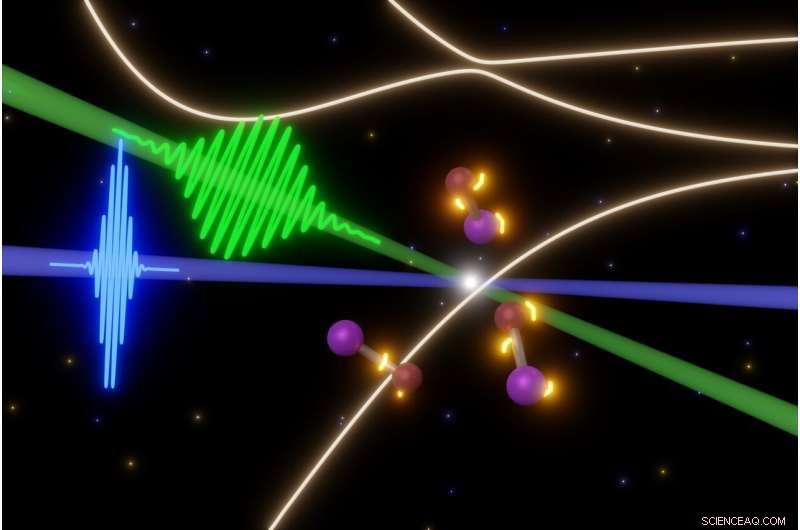
Os cientistas da UC Berkeley estão sondando as etapas fugazes em reações fotoquímicas rápidas com alguns dos pulsos de laser mais curtos possíveis hoje. Nesse caso, um pulso de femtossegundo de luz visível (verde) desencadeia a quebra de moléculas de monobrometo de iodo (centro), enquanto os pulsos de laser attosecond XUV (azul) capturam instantâneos das moléculas. Isso permite que eles façam um filme da evolução dos estados eletrônicos (luzes amarelas ao redor das moléculas) antes que as moléculas se separem. Crédito:Yuki Kobayashi, UC Berkeley
Em dias claros de verão, a luz do sol ao nosso redor está quebrando mal ao quebrar os laços. Ligações químicas.
A luz ultravioleta quebra as ligações entre os átomos no DNA das células da nossa pele, potencialmente causando câncer. A luz ultravioleta também quebra as ligações de oxigênio, eventualmente criando ozônio, e separa o hidrogênio de outras moléculas para deixar para trás radicais livres que podem danificar o tecido.
Universidade da Califórnia, Berkeley, químicos usando alguns dos pulsos de laser mais curtos disponíveis - um quintilionésimo de segundo - agora foram capazes de resolver o processo passo a passo que leva à explosão de uma ligação química, essencialmente fazer um filme do evento. Eles podem seguir os elétrons saltando indecisamente em vários estados da molécula antes que a ligação se quebre, e os átomos seguem seus caminhos separados.
A tecnica, relatado na semana passada no jornal Ciência , ajudará os químicos a compreender e potencialmente manipular as reações químicas estimuladas pela luz, as chamadas reações fotoquímicas. Químicos e biólogos, em particular, estão interessados em entender como grandes moléculas conseguem absorver a energia da luz sem quebrar nenhuma ligação, como acontece quando as moléculas do olho absorvem luz, nos dando visão, ou moléculas em plantas absorvem luz para fotossíntese.
"Pense em uma molécula, rodopsina, no olho, "disse o primeiro autor Yuki Kobayashi, um estudante de doutorado da UC Berkeley. "Quando a luz atinge a retina, rodopsina absorve a luz visível, e podemos ver as coisas porque a conformação da ligação da rodopsina muda. "
Na verdade, quando a energia da luz é absorvida, um vínculo nas torções da rodopsina, em vez de pausas, desencadeando outras reações que resultam na percepção da luz. A técnica Kobayashi e seus colegas da UC Berkeley, professores Stephen Leone e Daniel Neumark, desenvolvido poderia ser usado para estudar em detalhes como essa absorção de luz leva à torção depois que a molécula passa por um estado excitado chamado de cruzamento evitado ou interseção cônica.
Para evitar a quebra de uma ligação no DNA, "você deseja redirecionar a energia da dissociação para apenas ser vibracionalmente quente. Para a rodopsina, você deseja redirecionar a energia de vibração para uma isomerização cis-trans, uma reviravolta, "Kobayashi disse." Esses redirecionamentos de reações químicas estão acontecendo de forma onipresente ao nosso redor, mas não vimos o momento real deles antes. "

Yuki Kobayashi faz ajustes em um experimento no porão do Hildebrand Hall. Ele e os pesquisadores dos laboratórios de Stephen Leone e Daniel Neumark têm como alvo as moléculas em uma câmara de vácuo com lasers de femtossegundo e attossegundo para descobrir como as moléculas absorvem luz. Crédito:Foto da UC Berkeley, cortesia de Robert Sanders
Pulsos de laser rápidos
Lasers de atossegundo - um attossegundo é um bilionésimo de bilionésimo de segundo - existem há cerca de uma década e são usados por cientistas para sondar reações muito rápidas. Uma vez que a maioria das reações químicas ocorrem rapidamente, esses lasers de pulso rápido são a chave para "ver" como os elétrons que formam a ligação química se comportam quando a ligação se quebra e / ou reforma.
Leone, professor de química e física, é um experimentalista que também usa ferramentas teóricas e é um pioneiro no uso de lasers de attossegundo para sondar reações químicas. Ele tem seis desses raios-X e ultravioleta extremo (coletivamente, XUV) lasers em seu laboratório na UC Berkeley.
Trabalhando com uma das moléculas mais simples, monobrometo de iodo (IBr) - que é um átomo de iodo ligado a um átomo de bromo - a equipe da UC Berkeley atingiu as moléculas com um pulso de luz visível de 8 femtossegundos para excitar um de seus elétrons mais externos, em seguida, sondou-os com pulsos de laser de attossegundo.
Pulsar o laser de attossegundo XUV em intervalos cronometrados de 1,5 femtossegundo (um femtossegundo é 1, 000 attossegundos), muito parecido com o uso de uma luz estroboscópica, os pesquisadores puderam detectar as etapas que levam à quebra das moléculas. O laser XUV de alta energia foi capaz de explorar os estados de energia excitados em relação aos elétrons internos da molécula, que normalmente não participam de reações químicas.
"Você está fazendo um filme dos caminhos do elétron quando ele se aproxima do cruzamento e da probabilidade de ele seguir por um caminho ou por outro, "Leone disse." Essas ferramentas que estamos desenvolvendo permitem que você olhe para sólidos, gases e líquidos, mas você precisa de escalas de tempo mais curtas (fornecidas por um laser de attossegundo). De outra forma, você só vê o começo e o fim, e você não sabe o que mais aconteceu no meio. "
O experimento mostrou claramente que os elétrons externos do IBr, uma vez animado, de repente, vê uma variedade de estados ou lugares onde eles poderiam estar e explore muitos deles antes de decidir qual caminho seguir. Nesta molécula simples, Contudo, todos os caminhos levam ao elétron se fixando em iodo ou bromo e os dois átomos se separando.
Em moléculas maiores, que a equipe espera explorar em breve, elétrons excitados teriam mais opções, alguns onde a energia entra em uma torção, como com rodopsina, ou em vibração molecular sem que as moléculas se separem.
"Em biologia, Acontece que a evolução selecionou coisas que são extremamente eficazes em absorver a energia e não quebrar um vínculo, "Leone disse." Quando algo dá errado em sua química é quando você vê doenças surgindo. "