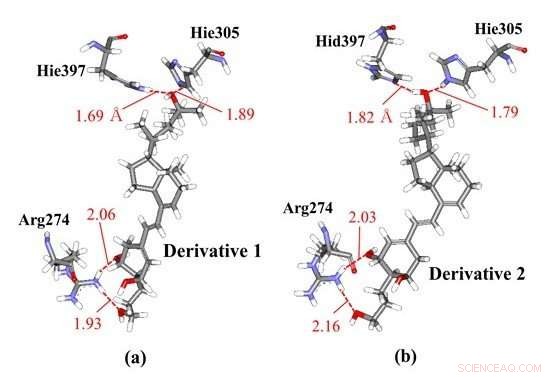
Interações de ligações de hidrogênio entre derivados de vitamina D e resíduos de aminoácidos em VDR; (a) derivada 1 e (b) derivada 2 que têm as mesmas estruturas químicas, mas quiralidades diferentes. Nossas simulações moleculares ab initio demonstraram que o derivado 1 interage com Hie397 e Hie305, enquanto o derivado 2 interage com diferentes resíduos de histidina protonada, como Hid397 e Hie305, indicando que a diferença na quiralidade dos derivados pode induzir alterações nos estados de protonação da histidina da proteína VDR. Crédito:Toyohashi University of Technology
Pesquisadores da Toyohashi University of Technology, em cooperação com pesquisadores da Teijin Pharma Ltd. e da Teikyo University, destacaram a possibilidade de que a quiralidade dos derivados da vitamina D pode afetar os estados de protonação dos resíduos de histidina na proteína do receptor da vitamina D por meio de simulações moleculares ab initio e análises biomédicas. Este achado enfatiza que os estados de protonação devem ser considerados mais precisamente em simulações moleculares, ao investigar interações específicas entre drogas candidatas e proteínas-alvo relacionadas à patogênese da doença.
A vitamina D desempenha muitos papéis importantes no aparecimento de doenças imunológicas, bem como a regulação dos níveis de cálcio no sangue. Essas ações fisiológicas causadas pela vitamina D ativa são desencadeadas pela interação específica da vitamina D ativa com o receptor de vitamina D (VDR); muitos tipos de derivados da vitamina D foram desenvolvidos como ligantes potentes contra o VDR. Foi relatado que a afinidade de ligação entre o VDR humano e os derivados da vitamina D depende significativamente da quiralidade do derivado.
Contudo, o motivo da dependência não foi esclarecido, o que o torna um gargalo no desenvolvimento de novos e potentes medicamentos contra doenças imunológicas, cujo início está relacionado à ativação do VDR.
Agora, pesquisadores do Departamento de Ciência da Computação e Engenharia da Toyohashi University of Technology e da Teijin Pharma Ltd. e da Teikyo University demonstraram a possibilidade da quiralidade do derivado da vitamina D afetar os estados de protonação dos resíduos de histidina na proteína VDR com base nos resultados avaliado por simulações moleculares de última geração e pelo computador K da RIKEN.
Os pesquisadores observaram as interações específicas entre o VDR e alguns derivados da vitamina D com diferentes quiralidades usando cálculos de orbitais moleculares de fragmentos ab initio (FMO). Os resultados do FMO revelam que dois resíduos de histidina no VDR contribuem significativamente para a ligação do VDR com os derivados e que os estados de protonação desses resíduos podem afetar as interações específicas. Portanto, os pesquisadores consideraram os outros possíveis estados de protonação desses resíduos de histidina e determinaram os estados mais estáveis usando os cálculos de FMO ab initio. Os resultados ilustrados, pela primeira vez, a possibilidade de que a diferença nas quiralidades dos derivados da vitamina D pode induzir mudanças nos estados de protonação dos resíduos de histidina no VDR que existe próximo ao derivado. Devido a esta mudança no estado de protonação, os derivados podem se ligar mais fortemente ao VDR e, portanto, produzir complexos mais estáveis com ele.
Esta descoberta fornece um aviso importante e essencial para as simulações moleculares para considerar os estados de protonação de resíduos de histidina em proteínas mais precisamente ao investigar as interações específicas entre proteínas e ligantes.
"Usamos simulações moleculares sofisticadas e o computador K para descobrir que os estados de protonação dos resíduos de histidina no VDR mudam significativamente com alterações na quiralidade do ligante, "explica o professor associado Noriyuki Kurita, "Uma vez que existem resíduos de histidina em muitas proteínas envolvidas na patogênese de doenças, devemos considerar seus estados de protonação mais precisamente via design de drogas in silico com base em simulações moleculares. "
O primeiro autor, estudante de graduação Yuta Terauchi, disse, "Nosso objetivo final é desenvolver drogas novas e potentes capazes de ativar o VDR com base em nossas simulações moleculares ab initio, bem como com base em estudos biomédicos realizados por nossos colaboradores. "
Os autores estão participando de um consórcio de design de drogas in silico - o consórcio de design de droga orbital molecular de fragmento (FMODD) - no qual vários pesquisadores de universidades, empresas farmacêuticas, and national institutes are investigating the specific interactions between disease-related proteins and many types of candidate drugs using ab initio molecular simulations based on the FMO method and the K computer. Similar molecular simulations are underway now for a huge number of vitamin D derivatives in order to propose novel ligands for VDR, which can act as candidate for potent drugs against immunological diseases, como o câncer.