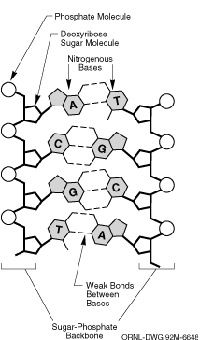
 Esta ilustração mostra quatro pares de bases de DNA. O Projeto Genoma Humano estudou 3,2 bilhões desses pares de bases! Sistema de Informação de Gerenciamento de Genoma, Oak Ridge National Laboratory
Esta ilustração mostra quatro pares de bases de DNA. O Projeto Genoma Humano estudou 3,2 bilhões desses pares de bases! Sistema de Informação de Gerenciamento de Genoma, Oak Ridge National Laboratory O espaço pode ser a fronteira final, mas a biologia humana é o desconhecido original, desafiando-nos a descobrir quem somos e de onde viemos. DNA , o bloco de construção da vida, contém o código genético que tanto informa quem somos. Este código é escrito com quatro letras, cada um representando um diferente base . As quatro bases são adenina (A), que emparelha com timina (T), e citosina (C), que emparelha com guanina (G).
Os cientistas sabem há muito tempo que essas quatro letras fornecem as receitas de proteínas, que realizam inúmeras funções corporais. Mas ainda há questões a serem respondidas, incluindo como os 3,2 bilhões de pares de bases contidos no genoma humano são ordenados. (O genoma humano é todo o feixe de DNA de uma pessoa dividido de forma desigual entre 23 pares de cromossomos.) Para esse fim, a Projeto Genoma Humano ( HGP ) foi lançado em 1990. Algumas das metas ambiciosas do projeto incluíam:
[fonte:Genome.gov]
Administrado pelo National Institutes of Health e pelo Departamento de Energia dos EUA, o projeto foi concluído antes do previsto em 2003. Um lote "final" de resultados foi publicado em 2006, mas os dados produzidos pelo HGP são continuamente examinados, analisados e ocasionalmente revisados. Teoricamente, com os principais objetivos alcançados, o projeto está concluído. Vejamos um pouco do que aprendemos.
Apenas alguns anos antes da conclusão do HGP, as previsões populares afirmavam que os humanos tinham até 100, 000 genes. Mas estimativas recentes de HGP reduziram esse número para uma faixa mais modesta de 20, 000 a 25, 000 [fonte:Informações sobre o projeto do genoma humano]. Além disso, o HGP ajudou a estreitar a gama de genes possíveis e a isolar certos candidatos como contribuintes para doenças específicas. Os cientistas também reavaliaram suposições anteriores, como a ideia de que os genes são independentes, pedaços discretos de DNA com funções definidas. Nem sempre é o caso. Agora sabemos que alguns genes multitarefa produzem mais de uma proteína; na verdade, o gene médio pode produzir três proteínas [fonte:Genome.gov]. Também, os genes parecem agarrar o código genético de outros segmentos de DNA.
Antes de olharmos de perto a hereditariedade e os genes, vamos parar para considerar o que os cientistas aprenderam sobre animais e outros genomas. Alguns desses projetos, como mapear o genoma do mouse, foram incluídos no Projeto Genoma Humano original e podem nos contar sobre nossa evolução e DNA.
Os cientistas mapearam muitos genomas de animais, entre eles o do chimpanzé, mouse, rato, mosca da fruta, lombriga e peixes-balão. Eles também mapearam alguns genomas de plantas e doenças. Esses mapas genômicos são úteis em parte porque os genomas animais podem ser comparados aos humanos. Pense em um programa de TV policial em que uma impressão translúcida mostrando o DNA de um suspeito está alinhada com a das evidências de DNA. Quando tudo estiver alinhado, há uma partida, e a polícia tem seu assassino. De forma similar, os cientistas podem procurar combinações entre o DNA humano e animal. Eles não esperam combinações perfeitas, mas examinando onde nossos genomas se alinham, pesquisadores podem ver o que temos em comum com os animais, o que nós não fazemos, e fazer determinações sobre ancestrais comuns e como evoluímos. Em casos de doenças que afetam os animais, como o câncer que assola a população de demônios da Tasmânia, uma melhor compreensão do DNA animal pode levar a tratamentos médicos importantes.
Mencionamos que um dos objetivos do HGP era sequenciar os genomas de cinco "organismos modelo". Este sequenciamento é uma parte importante de um campo conhecido como genômica comparativa . Em genômica comparada, o estudo de um animal com um genoma menos complexo, como um mouse, pode render informações importantes sobre genes que camundongos e humanos compartilham desde que estamos, na verdade, geneticamente muito semelhantes [fonte:HGP Information]. Assim como outras formas de testes em animais, examinar o genoma de outra espécie pode nos dizer mais sobre o nosso.
Um dos casos mais intrigantes de um animal cujo genoma foi mapeado é o do ornitorrinco. Esta criatura sempre foi considerada uma esquisitice porque é um dos poucos mamíferos que põe ovos e amamenta seus filhotes através de sua pele abdominal, ao invés de mamilos. O genoma do ornitorrinco, com seus 18, 500 genes, é importante porque remonta a uma época antiga, quando os mamíferos eram camadas de ovos [fonte:Hood]. A evolução provavelmente afastou os humanos dos ancestrais que compartilhamos com o ornitorrinco há cerca de 170 milhões de anos. Hoje, esta maravilha evolucionária tem características de mamíferos, pássaros e répteis [fonte:Hood]. Eles também têm 10 cromossomos sexuais, em comparação com nossos dois miseráveis.
Fora do genoma humano (e, claro, do ornitorrinco), talvez nenhum projeto de mapeamento genético seja tão atraente quanto aquele focado em desvendar o código genético de vários tipos de câncer. O sequenciamento de genomas de câncer permite que cientistas e médicos descubram mutações genéticas que contribuem para o câncer, potencialmente levando a melhores métodos de detecção e tratamentos.
O primeiro genoma de câncer completo sequenciado foi o da leucemia mieloide aguda, uma forma grave de câncer que começa na medula óssea. The Cancer Genome Atlas, uma organização que espera sequenciar muitos tipos de câncer, liderou o mapeamento usando sequenciamento maciçamente paralelo , que compara DNA normal e de câncer e procura mutações [fonte:Kushnerov].
Se o sequenciamento do genoma do câncer provar a hipótese de que cada ocorrência de câncer produz mutações únicas em uma pessoa específica, os futuros médicos poderão personalizar os tratamentos para cada paciente. Com muitos tratamentos disponíveis para algumas condições, geralmente é um processo de tentativa e erro para ver o que funciona melhor para uma pessoa em vez de outra [fonte:Aetna]. Em alguns casos, essa prática pode fazer mais mal do que bem ou privar médicos e pacientes do valioso tempo necessário para conter o avanço de uma doença.
Agora que o Projeto Genoma Humano acabou, é hora de os cientistas examinarem as informações produzidas e realizarem pesquisas relacionadas. Muito do foco pós-HGP recaiu sobre os genes, estimulando novas discussões sobre como funciona a hereditariedade e fazendo com que os cientistas vejam o DNA de maneira diferente, deixando de lado o foco tradicional nos genes como os atores dominantes no DNA. Alguns pesquisadores estão agora olhando para cerca de 99 por cento do DNA que não são genes, me perguntando se esses pedaços anteriormente negligenciados do genoma têm papéis significativos a desempenhar.
O HGP e os esforços de pesquisa subsequentes mudaram a visão consensual dos genes e do DNA não codificador, lançando-os como parte de uma imagem cada vez mais complexa dos genes, DNA e outros componentes do genoma. Por exemplo, epigenético marcas , as proteínas e outras moléculas ligadas ao DNA, estão recebendo mais atenção, especialmente por seu aparente papel na hereditariedade. Parece que essas marcas também podem transmitir traços, assim como genes, e marcas epigenéticas mal colocadas ou danificadas podem aumentar o risco de alguém desenvolver câncer e outros distúrbios [fonte:Zimmer]. Um estudo de US $ 190 milhões do National Institutes of Health espera mapear todas as marcas epigenéticas no DNA.
Além de mudar a forma como pensamos sobre os genes, o Projeto Genoma Humano gerou muitos outros projetos. Por exemplo, em 2002, o International HapMap Project começou a mapear SNPs entre vários grupos étnicos. De pessoa para pessoa, o código genético difere em cerca de 10 milhões de pontos (de 3,2 bilhões de pares de bases de DNA) [fonte:Aetna]. Essas diferenças são chamadas SNPs - polimorfismos de nucleotídeo único . Mas, apesar desses SNPs, os seres humanos diferem uns dos outros em cerca de 0,1 por cento, o suficiente para garantir que dois seres humanos não sejam geneticamente idênticos, até, as vezes, gêmeos idênticos. Compreender os SNPs pode nos ajudar a entender melhor a variação genética entre indivíduos e grupos étnicos; produzir melhores testes genéticos para predisposição a doenças; e contribuir para o desenvolvimento de tratamentos médicos mais personalizados.
Projetos futuros e áreas de pesquisa relacionadas ao HGP são aparentemente infinitas. Muitos milhões de dólares estão sendo investidos em projetos como o Encode, um esforço extremamente ambicioso para determinar o papel de cada pedaço de DNA no genoma humano. (Codificar significa Encyclopedia of DNA Elements.) Mas, embora as informações geradas pelo HGP e projetos relacionados provavelmente levem a importantes avanços médicos e tratamentos de doenças, a relação entre pesquisa e terapias práticas não é realmente uma simples causa e efeito. Apenas um novo medicamento pode levar 10 anos de tempo de desenvolvimento.
No futuro, fique atento a esses campos de pesquisa em expansão, muitos dos quais têm uma grande dívida com o trabalho do HGP:
Apesar de todas essas descobertas empolgantes e daquelas que nos esperam, podemos nunca compreender totalmente o funcionamento interno do DNA. A definição do gene que muda rapidamente pode ser uma prova disso. Um pesquisador disse ao New York Times que a biologia humana pode ser "irredutivelmente complexa" [fonte:Angier]. Nós, humanos, podemos fazer e compreender coisas notáveis - lançar espaçonaves, construir computadores incrivelmente rápidos, criar lindas obras de arte - mas nossos 3,2 bilhões de pedaços de DNA podem ser demais para nossas mentes compreenderem no final. No curso do progresso humano, foi muito mais fácil entender as coisas que fazemos, ao invés do que nos torna.
Para obter mais informações sobre o Projeto Genoma Humano e outros tópicos relacionados, como epigenética, visite os links na próxima página.
Fontes