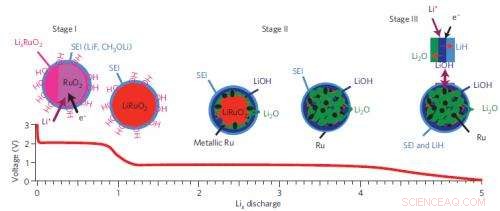
Um resumo da via de reação de três estágios do sistema de bateria de óxido de rutênio-lítio.
As baterias de íons de lítio alimentam quase todos os dispositivos eletrônicos portáteis que usamos todos os dias, incluindo smartphones, máquinas fotográficas, brinquedos, e até carros elétricos. Pesquisadores de todo o mundo estão trabalhando para encontrar materiais que levem à segurança, barato, de longa duração, e poderosas baterias de íon-lítio.
Trabalhando em várias instalações de fontes de luz do Departamento de Energia dos EUA e nas universidades Cambridge e Stony Brook, um grupo de pesquisadores estudou recentemente uma classe de eletrodos de bateria de íon-lítio que têm capacidades muito maiores do que os materiais usados nas baterias atuais. Os pesquisadores queriam determinar por que esses materiais muitas vezes podem armazenar mais carga do que a teoria prevê.
Os autores escolheram o óxido de rutênio (RuO2) como sistema modelo para estudar esses chamados "materiais de conversão, "nomeados porque sofrem grandes mudanças estruturais ao reagir com os íons de lítio, formando reversivelmente nanopartículas de metal e sais (aqui Ru e Li2O). Essas reações são muito diferentes daquelas que ocorrem em eletrodos convencionais, que armazenam carga permitindo que íons de lítio se aninhem em espaços dentro da estrutura cristalina.
"Nossa investigação identificou a fonte da capacidade adicional encontrada para RuO2, e também rendeu um protocolo para estudar a 'camada de passivação' que se forma nos eletrodos da bateria, que protege o eletrólito de sofrer novas reações de decomposição em ciclos de carga-descarga subsequentes, "disse o pesquisador correspondente do estudo, Clare Gray, professor dos departamentos de química das universidades Cambridge e Stony Brook. "Compreender as estruturas dessas camadas de passivação é a chave para fazer baterias que duram o suficiente para uso em aplicações como transporte e armazenamento de rede elétrica."
Na Fonte de Luz Síncrotron Nacional do Laboratório Nacional de Brookhaven, a equipe estudou suas amostras usando a estrutura de absorção de raio-x próxima à borda (XANES) e a estrutura fina de absorção de raio-x estendida (EXAFS). Na Fonte Avançada de Fótons do Laboratório Nacional de Argonne, eles usaram duas técnicas adicionais, difração de raios-x de alta resolução (XRD) e análise de função de distribuição de par de espalhamento (PDF), para extrair informações sobre as mudanças estruturais eletrônicas e de longo / curto alcance do eletrodo RuO2 em tempo real conforme a bateria era descarregada e carregada. Usando esses métodos, a equipe mostrou que RuO2 foi reduzido a nanopartículas de Ru e Li2O por meio da formação de fases intermediárias, LixRuO2.
Uma vez que isso não explica a origem do mecanismo de armazenamento de carga adicional, o grupo usou outra técnica, ressonância magnética nuclear de estado sólido (NMR) de alta resolução. Este método envolve submeter uma amostra a um campo magnético e medir a resposta dos núcleos dentro da amostra. Pode fornecer informações específicas sobre as composições químicas e estruturas locais, e é particularmente útil para estudar compostos que contêm apenas elementos "leves", como hidrogênio (H), Li, e oxigênio (O), que são difíceis de detectar usando o XRD. Os dados de NMR mostraram que o principal contribuinte para a capacidade é a formação de LiOH, que se converte reversivelmente em Li2O e LiH. Contribuintes menores para a capacidade vêm do armazenamento de Li nas superfícies das nanopartículas de Ru, formando uma liga LixRu, e a decomposição do eletrólito. O último, Contudo, em última análise, faz com que a capacidade diminua e resultará na morte da bateria após vários ciclos de carga.