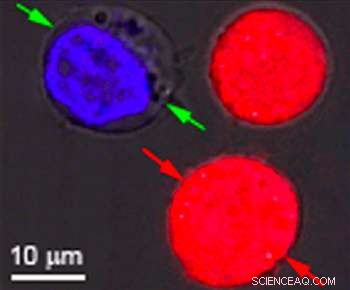
 p Células idênticas coradas de vermelho e azul foram o alvo da pesquisa na Rice University para mostrar o efeito das nanobolhas plasmônicas. As bolhas se formam em torno de nanopartículas de ouro aquecidas que têm como alvo células específicas, como células cancerosas. Quando as partículas são ocas, formam-se bolhas grandes o suficiente para matar a célula quando estouram. Quando as partículas são sólidas, as bolhas são menores e podem abrir um buraco temporário na parede celular, permitindo o fluxo de drogas ou outro material. Ambos os efeitos podem ser alcançados simultaneamente com um único pulso de laser. Crédito:Plasmonic Nanobubble Lab / Rice University
p Células idênticas coradas de vermelho e azul foram o alvo da pesquisa na Rice University para mostrar o efeito das nanobolhas plasmônicas. As bolhas se formam em torno de nanopartículas de ouro aquecidas que têm como alvo células específicas, como células cancerosas. Quando as partículas são ocas, formam-se bolhas grandes o suficiente para matar a célula quando estouram. Quando as partículas são sólidas, as bolhas são menores e podem abrir um buraco temporário na parede celular, permitindo o fluxo de drogas ou outro material. Ambos os efeitos podem ser alcançados simultaneamente com um único pulso de laser. Crédito:Plasmonic Nanobubble Lab / Rice University
p (Phys.org) - Pesquisadores da Rice University descobriram uma maneira de matar algumas células doentes e tratar outras na mesma amostra ao mesmo tempo. O processo ativado por um pulso de luz laser deixa as células saudáveis vizinhas intocadas. p O uso exclusivo para nanobolhas plasmônicas sintonizáveis desenvolvido no laboratório Rice de Dmitri Lapotko mostra a promessa de substituir vários processos difíceis agora usados para tratar pacientes com câncer, entre outros, com um rápido, simples, procedimento multifuncional.
p A pesquisa é o foco de um artigo publicado online esta semana pela revista American Chemical Society.
ACS Nano e foi realizado na Rice por Lapotko, o cientista pesquisador e autor principal Ekaterina Lukianova-Hleb e o estudante de graduação Martin Matonga, com a assistência do Centro de Terapia Celular e Genética do Baylor College of Medicine (BCM), Hospital Infantil do Texas e Centro de Câncer MD Anderson da Universidade do Texas.
p Nanobolhas plasmônicas de 10, 000 vezes menor que um fio de cabelo humano causa pequenas explosões. As bolhas se formam em torno de nanopartículas de ouro plasmônico que aquecem quando excitadas por uma fonte de energia externa - neste caso, um curto pulso de laser - e vaporiza uma fina camada de líquido perto da superfície da partícula. A bolha de vapor se expande e desmorona rapidamente. Lapotko e seus colegas já haviam descoberto que as nanobolhas plasmônicas matam as células cancerosas literalmente explodindo-as sem causar danos a vizinhos saudáveis, um processo que mostrou muito mais precisão e seletividade em comparação com aqueles mediados apenas por nanopartículas de ouro, ele disse.
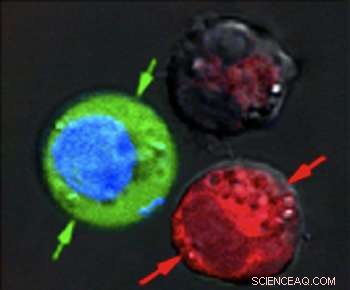 p Após o pulso de laser, células manchadas de vermelho mostram evidências de danos massivos de nanobolhas explodindo, enquanto as células coradas de azul permaneceram intactas, mas com corante fluorescente verde puxado de fora. Crédito:Plasmonic Nanobubble Lab / Rice University
p Após o pulso de laser, células manchadas de vermelho mostram evidências de danos massivos de nanobolhas explodindo, enquanto as células coradas de azul permaneceram intactas, mas com corante fluorescente verde puxado de fora. Crédito:Plasmonic Nanobubble Lab / Rice University
p O novo projeto leva essa habilidade notável alguns passos adiante. Uma série de experimentos provou que um único pulso de laser cria grandes nano-bolhas plasmônicas em torno de nanoconchas ocas de ouro, e essas grandes nanobolhas destroem seletivamente as células indesejadas. O mesmo pulso de laser cria nanobolhas menores em torno de nanoesferas de ouro sólido que perfuram uma pequena, poro temporário na parede de uma célula e criar um nanojato de entrada que rapidamente "injeta" drogas ou genes em outras células.
p Em seus experimentos, Lapotko e sua equipe colocaram nanoconchas ocas de 60 nanômetros de largura em células cancerígenas modelo e as tingiram de vermelho. Em um lote separado, eles colocaram nanoesferas de 60 nanômetros de largura no mesmo tipo de células e as tingiram de azul.
p Depois de suspender as células juntas em um corante fluorescente verde, eles dispararam um único pulso de laser largo na amostra combinada, lavou a mancha verde e verificou as células ao microscópio. As células vermelhas com as nanoconchas ocas foram destruídas por grandes nanobolhas plasmônicas. As células azuis estavam intactas, mas o líquido esverdeado de fora foi puxado para dentro das células, onde nanobolhas plasmônicas menores ao redor das nanopartículas de ouro maciço abriam temporariamente as paredes.
p Porque tudo isso acontece em uma fração de segundo, até 10 bilhões de células por minuto poderiam ser processadas seletivamente em um sistema de fluxo como o que está sendo desenvolvido na Rice, disse Lapotko, um membro do corpo docente em bioquímica e biologia celular e em física e astronomia. Isso tem potencial para avançar na terapia celular e genética e no transplante de medula óssea, ele disse.
p A maioria das terapias celulares e genéticas de combate a doenças requerem processamento "ex vivo" - fora do corpo - de enxertos de células humanas para eliminar células indesejadas (como cancerosas) e modificar geneticamente outras células para aumentar sua eficiência terapêutica, Disse Lapotko. "O processamento da célula atual costuma ser lento, caro e trabalhoso e sofre de altas perdas de células e baixa seletividade. Idealmente, tanto a eliminação quanto a transfecção (a introdução de materiais nas células) devem ser altamente eficientes, seletivo, rápido e seguro. "
p A tecnologia de nanobolhas plasmônicas promete "um método de fazer várias coisas a uma população de células ao mesmo tempo, "disse Malcolm Brenner, professora de medicina e pediatria da BCM e diretora do Centro de terapia celular e gênica da BCM, que colabora com a equipe do Rice. "Por exemplo, se eu quiser colocar algo em uma célula-tronco para fazê-la se transformar em outro tipo de célula, e, ao mesmo tempo, mata as células circundantes que têm o potencial de causar danos quando voltam a um paciente - ou a outro paciente - essas nanobolhas plasmônicas muito ajustáveis têm o potencial de fazer isso. "
p O objetivo de longo prazo de um esforço colaborativo entre Rice, BCM, O Texas Children's Hospital e o MD Anderson devem melhorar o resultado para pacientes com doenças cujo tratamento requer processamento celular ex vivo, Disse Lapotko.
p A Lapotko planeja construir um protótipo da tecnologia com o objetivo de testar com células humanas em um futuro próximo. “Gostaríamos que esta fosse uma plataforma universal para a terapia celular e genética e para o transplante de células-tronco, " ele disse.

