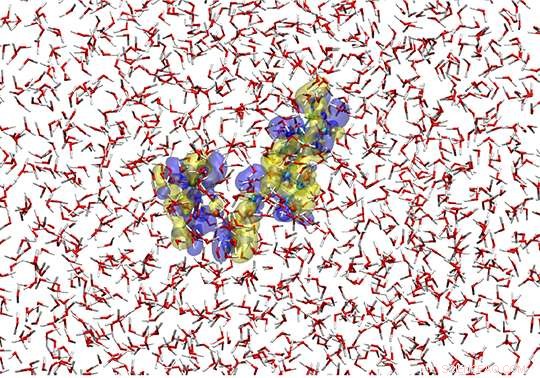
Um instantâneo da simulação quântica / clássica híbrida para ATP 4- colocado em solvente de água. Aqui, o soluto de ATP é descrito por um método de química quântica e as moléculas de água do solvente são representadas com um campo de força clássico. As superfícies transparentes azuis e amarelas mostram, respectivamente, as superfícies de isovalores do aumento e diminuição da densidade de elétrons em 3,0x10 -4 au em relação à distribuição média de elétrons de ATP 4- na solução. Assim, o estado eletrônico do soluto (ATP 4- ), bem como a propriedade molecular do solvente circundante são fielmente representados na simulação. Crédito:Hideaki Takahashi
Na hidrólise de ATP, a água é usada para separar o trifosfato de adenosina (ATP) para criar o difosfato de adenosina (ADP) para obter energia. A energia de hidrólise do ATP (AHE) é então usada nas atividades das células vivas.
Muitas tentativas foram feitas para explicar a origem molecular do AHE. Na década de 1960, AHE foi pensado para estar contido exclusivamente na estrutura molecular do ATP, e cálculos de química quântica foram conduzidos sem nenhum sucesso quantitativo.
No final da década de 1990, mais investigações em AHE foram conduzidas usando cálculos de mecânica quântica em água que foi tratada como um meio dielétrico contínuo. Contudo, o papel do solvente de água como um conjunto estruturado de pequenas moléculas na energética de AHE permaneceu obscuro.
Agora, pesquisadores no Japão têm, pela primeira vez, conseguiu desvendar o mecanismo microscópico de liberação de AHE na água, usando a abordagem computacional de última geração.
No estudo liderado por Hideaki Takahashi na Tohoku University, os efeitos das propriedades moleculares do solvente, bem como os estados eletrônicos dos solutos, foram totalmente considerados. Essas simulações em grande escala foram possibilitadas por técnicas computacionais híbridas quânticas e clássicas implementadas em computadores maciçamente paralelos. Isso se refere ao uso de um grande número de processadores executando simultaneamente um conjunto de cálculos coordenados.
Além disso, a simulação foi seguida por cálculos de energia livre usando um método de alta precisão e alta velocidade desenvolvido por Nobuyuki Matubayasi na Universidade de Osaka.
Com este estudo, a equipe de pesquisa explicou por que as energias livres de hidrólise do ATP e do pirofosfato são principalmente de -10 kcal / mol e são insensíveis às cargas totais desses solutos. Eles também descobriram que a constância do AHE é o resultado da excelente compensação entre a estabilização do estado eletrônico e a desestabilização na energia livre de hidratação dos solutos.
Isso é significativo porque constitui uma nova questão fundamental a ser descrita em livros-texto de biologia padrão.