Na ciência, você pode fazer experimentos com compostos hidratados e anidros. A principal diferença entre compostos hídricos e compostos anidros é a presença de moléculas de água. Um composto hidratado contém moléculas de água, mas um composto anidro não contém.
Propriedades do composto hidratado
Um composto hidratado (um hidrato) é um composto químico com água em sua estrutura. Por exemplo, sais hidratados têm água dentro de seus cristais. Os hidratos se formam naturalmente quando os compostos iônicos são expostos ao ar e se ligam às moléculas de água. Especificamente, a ligação é formada entre o cátion da molécula e a molécula de água. A água que resta é geralmente conhecida como água de hidratação ou água de cristalização. A maioria dos hidratos é estável à temperatura ambiente. No entanto, alguns involuntariamente rendem água na atmosfera. Esses hidratos são conhecidos como eflorescentes.
Propriedades do composto anidro
Um composto anidro (um anidrato) é um composto sem água em sua estrutura. Depois que a água é removida de um hidrato, ela se torna um anidrato. As moléculas de água são removidas por sucção ou aquecimento do composto a uma temperatura alta. Por exemplo, um sal anidro teve a água expulsa de seus cristais. Um composto anidro de um hidrato é geralmente altamente solúvel em água e, quando dissolvido em água, terá uma cor semelhante à do hidrato original, mesmo que tenha mudado de cor, transformando o hidrato em composto anidro.
Exemplos de Hidratos
Exemplos de hidratos são gesso (comumente usado na fabricação de papelão, cimento e gesso de Paris), Bórax (usado em muitos produtos cosméticos, de limpeza e de lavanderia) e sal epsom (usado como remédio natural e esfoliante). Os hidratos são frequentemente usados em produtos de cuidados com a pele para infundir umidade no corpo. O mundo contém muitos hidratos gasosos, sólidos cristalinos nos quais as moléculas de gás estão envolvidas em estruturas feitas de moléculas de água. Estes se formam a partir de temperaturas muito baixas e alta pressão. Eles são misturados com sedimentos e são encontrados principalmente nas profundezas do oceano e nas regiões do Ártico.
Exemplos de anidratos
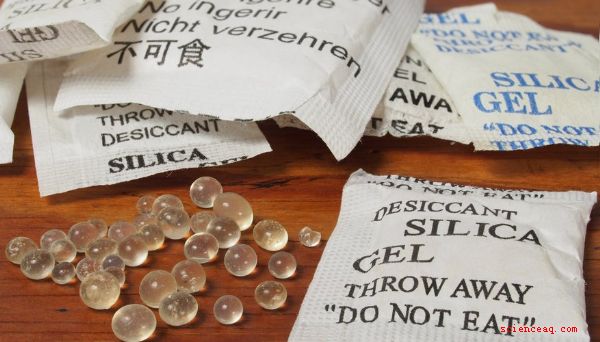
Os anidratos, também conhecidos como dessecantes, removem a água e são frequentemente usados em agentes de secagem, como papel produtos. O gel de sílica é um dos anidratos mais usados. Um pacote de gel de sílica é mantido dentro de bolsas acabadas e outros produtos para absorver a água, mantendo a área circundante seca e impedindo o crescimento de fungos. Os anidratos também podem reter a umidade dos alimentos e produtos de tabaco quando estão na forma umectante.