
O estudante de pós-graduação da Rice University, Kang-Jie (Harry) Bian, monta moléculas sensíveis à luz para um experimento no laboratório do químico Julian West. Bian é o principal autor de um estudo inspirado em processos naturais para permitir a difuncionalização modular de moléculas de alceno para o design de medicamentos e materiais. Crédito:Universidade Rice
Inspirado pelo fígado e ativado pela luz, um processo químico desenvolvido nos laboratórios da Rice University e na China mostra-se promissor para o design de medicamentos e o desenvolvimento de materiais exclusivos.
Pesquisadores liderados pelo químico de arroz Julian West e Xi-Sheng Wang da Universidade de Ciência e Tecnologia da China, Hefei, estão relatando seu processo catalítico bem-sucedido para adicionar simultaneamente dois grupos funcionais distintos a alcenos únicos, moléculas orgânicas extraídas de produtos petroquímicos que contêm pelo menos uma ligação dupla carbono-carbono combinada com átomos de hidrogênio.
Melhor ainda, dizem eles, é que esses alcenos são "desativados" - ou seja, eles não têm átomos reativos perto da ligação dupla - e até agora, provaram ser difíceis de melhorar.
A via química detalhada no
Journal of the American Chemical Society poderia simplificar a criação de uma biblioteca de precursores para a indústria farmacêutica e aprimorar a fabricação de polímeros.
West, cujo laboratório projeta processos químicos sintéticos, disse que a inspiração inicial veio de uma enzima, o citocromo P450, que o fígado usa para eliminar moléculas potencialmente nocivas.
"Essas enzimas são uma espécie de serras circulares que trituram as moléculas antes que possam causar problemas", disse ele. "Eles fazem isso por meio de um mecanismo interessante chamado rebote radical".
West disse que o P450 encontra ligações carbono-hidrogênio e remove o hidrogênio, deixando um radical centrado no carbono que inclui um elétron desemparelhado.
"Esse elétron realmente quer encontrar um parceiro, então o P450 devolverá imediatamente um átomo de oxigênio (o 'rebote'), oxidando a molécula", disse ele. "No corpo, isso ajuda a desativar essas moléculas para que você possa se livrar delas.
"Esse tipo de recuperação é poderoso", disse West. "E Harry (o autor principal Kang-Jie Bian, um estudante de pós-graduação da Rice) se perguntou se poderíamos fazer algo parecido para transferir fragmentos diferentes para esse radical."
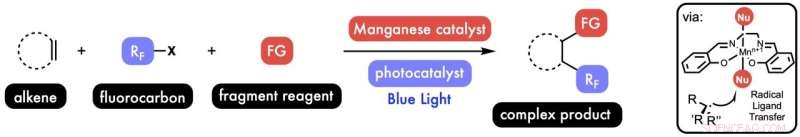
Os químicos da Rice University desenvolveram um método para adicionar dois fragmentos a uma molécula de alceno em um único processo. A descoberta pode simplificar o design de medicamentos e materiais. Crédito:West Research Group/Rice University
A solução deles foi permitir o que eles chamam de transferência radical de ligantes, um método geral que usa manganês para catalisar o "rebote radical".
West disse que enquanto o P450 usa o elemento próximo, o ferro, para catalisar a reação biológica, experimentos anteriores no laboratório Rice e em outros lugares mostraram que o manganês tinha potencial.
"O manganês ajudou o processo a ser mais seletivo e um pouco mais ativo, além de muito mais barato e fácil", explicou. "Ele pode transferir vários átomos diferentes - como cloro, nitrogênio e enxofre - apenas mudando o ingrediente comercial que você adiciona à reação".
Essa reação foi responsável por uma funcionalização. Por que não ir para dois?
West disse que Bian também teve a ideia de adicionar um fotocatalisador à mistura. "Quando você acende a luz sobre ele, ele fica excitado e você pode fazer coisas que seriam impossíveis no estado fundamental, como ativar pequenas moléculas de fluorocarbono para fazer fragmentos radicais que possuem ligações carbono-flúor, que são importantes para a ciência farmacêutica e de materiais. " ele disse. "Agora podemos anexá-los à nossa molécula de interesse."
O resultado final é um processo suave e modular para adicionar dois grupos funcionais a um único alceno em uma única etapa.
"Primeiro temos a ligação dupla carbono-carbono de uma molécula de interesse, o alceno", disse West, resumindo. “Então adicionamos esse valioso fluorocarbono e, em seguida, o catalisador de manganês sobe e faz essa transferência de ligante radical para adicionar um átomo de cloro, nitrogênio ou enxofre”.
Ele observou que a colaboração entre Rice e o laboratório de Wang foi um resultado natural da mudança de Bian para Rice de Hefei, onde obteve seu mestrado. “Nós realmente nos concentramos no aspecto de manganês deste trabalho, e o grupo de Wang trouxe não apenas experiência em fotocatálise, mas também desenvolveu e testou fragmentos de carbono-flúor, e mostrou que funcionaria muito bem neste sistema”, disse West.
Ele disse que, juntamente com as ciências farmacêuticas e de materiais, a biologia química também pode se beneficiar do processo, especialmente por sua afinidade com o pClick, um método descoberto pelo químico da Rice, Han Xiao, para anexar drogas ou outras substâncias a anticorpos.
Os co-autores são o estudante de graduação da Rice David Nemoto Jr. e o estudante de pós-graduação Shih-Chieh Kao, e Yan He e Yan Li de Hefei. Wang é professor em Hefei. West é o jovem investigador Norman Hackerman-Welch e professor assistente de química.
+ Explorar mais Tem pressa para desenvolver drogas? Aqui está seu bate-papo

