Elucidando os alvos moleculares do ácido eicosapentaenóico:um remédio natural para a dor crônica
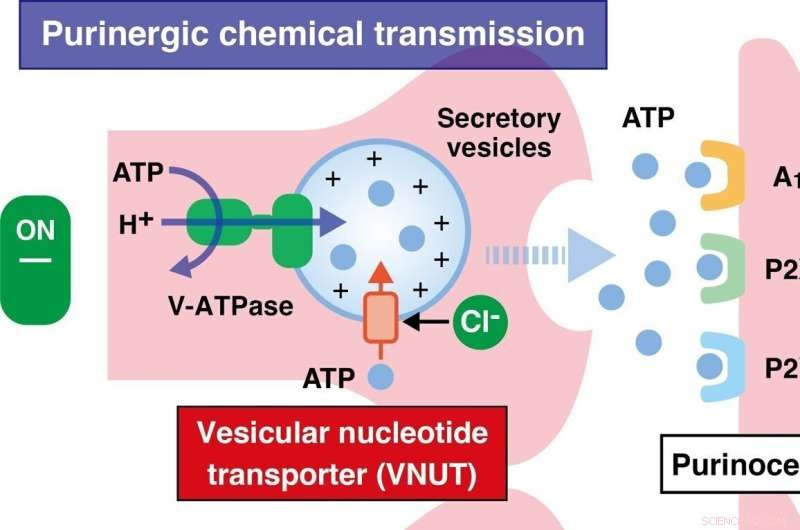
Novo estudo identifica o transportador de nucleotídeo vesicular como um novo alvo do ácido eicosapentaenóico (EPA) e destaca o mecanismo subjacente ao efeito analgésico do EPA. O EPA atenua potentemente a dor neuropática e inflamatória e a resistência à insulina, com menos efeitos colaterais. Crédito:Takaaki Miyaji da Universidade de Okayama
O ácido eicosapentaenóico (EPA) é um nutriente essencial pertencente ao grupo ômega-3 dos ácidos graxos poliinsaturados (PUFAs). Como o corpo humano não pode sintetizar PUFAs, suplementos dietéticos contendo EPA são necessários para funções fisiológicas normais. Encontrado abundantemente em fontes naturais como peixe, óleo de cânhamo e óleo de linhaça, o EPA é conhecido por exibir atividades anti-inflamatórias, neuroprotetoras e protetoras cardiovasculares.
Além disso, estudos recentes demonstraram seus efeitos terapêuticos na redução do risco de mortalidade após o infarto do miocárdio, melhorando a resistência à insulina, reduzindo os níveis de lipídios no sangue e inibindo a agregação plaquetária. Os PUFAs ômega-3 também demonstraram diminuir as respostas inflamatórias após a infecção por COVID-19. Apesar do amplo espectro de seus efeitos terapêuticos, o(s) alvo(s) molecular(es) e o mecanismo subjacente da ação do EPA permanecem indefinidos.
O professor de pesquisa Takaaki Miyaji, da Universidade de Okayama, no Japão, e sua equipe de pesquisadores descobriram um novo alvo molecular do EPA em seu recente trabalho publicado na revista
Proceedings of the National Academy of Sciences .
Explicando a lógica por trás de seu estudo, o professor de pesquisa Miyaji, autor correspondente deste artigo, diz que "alvos moleculares convencionais, como inibidores de COX-2, podem explicar os efeitos anti-inflamatórios e analgésicos da dor inflamatória, mas não da dor neuropática, do EPA No entanto, como o EPA atenua significativamente a dor inflamatória e neuropática, existe uma forte possibilidade de que exista outro importante alvo molecular do EPA relacionado à neuropatia." Mergulhando mais fundo, a equipe procurou entender o mecanismo de ação do EPA no alívio da dor inflamatória e neuropática.
Durante distúrbios neurológicos, metabólicos e imunológicos, a transmissão química "purinérgica" (uma forma de sinalização extracelular mediada por derivados de purina), leva à ligação de transportadores de energia como trifosfato de adenosina (ATP) a "purinoreceptores", que induz e exacerba neuropatia e percepção da dor inflamatória. Essa ligação é mediada por um transportador vesicular de nucleotídeos (VNUT), que se torna a molécula chave no início da sinalização purinérgica. Os pesquisadores levantaram a hipótese de que o EPA tem como alvo o VNUT, bloqueando assim a transmissão química purinérgica e reduzindo a percepção da dor.
O professor de pesquisa Miyaji e sua equipe testaram essa hipótese tanto in vitro, usando VNUT derivado de humanos, quanto in vivo, usando um modelo de camundongo deficiente em VNUT.
Eles descobriram que o EPA compete com íons de cloro que normalmente ativam o VNUT e inibem a liberação de ATP mediada pelo VNUT. Além disso, observaram esse efeito apenas com EPA e seus metabólitos, e não com ácido docosahexaenóico, outro ácido graxo ômega-3, sugerindo assim que a estrutura de ácidos graxos ômega-3 com cadeias laterais é necessária para a inibição de VNUT.
Além disso, eles induziram dor neuropática em camundongos do tipo selvagem e deficientes em VNUT usando agentes quimioterápicos que são usados no tratamento do câncer. Notavelmente, o EPA acentuou a dor em animais do tipo selvagem, mas não em camundongos deficientes em VNUT, corroborando assim sua descoberta anterior sobre o efeito inibitório do EPA no VNUT. Da mesma forma, a resistência à insulina induzida pela dor neuropática mostrou ser reduzida pelo tratamento com EPA em camundongos de tipo selvagem, mas não em camundongos deficientes em VNUT.
"Descobrimos que baixas concentrações de EPA inibiram completa e reversivelmente a liberação de ATP dos neurônios, sem inibir a liberação de outros neurotransmissores. Comparado com outras drogas, o EPA demonstrou um efeito analgésico maior e menos efeitos colaterais", explica o professor de pesquisa Miyaji.
Além da dor neuropática e resistência à insulina associada, os efeitos analgésicos do EPA podem ser estendidos à dor crônica associada a várias outras condições, como quimioterapia, diabetes, reumatismo, gota, ligadura do nervo ciático e inflamação. Além disso, a transmissão química purinérgica também está associada a uma variedade de condições, incluindo doença de Alzheimer e depressão, para as quais o EPA pode ser explorado como uma estratégia terapêutica.
Além disso, os opióides e outros medicamentos para alívio da dor podem ter efeitos colaterais a longo prazo e resultar em vícios. Na ausência de tratamentos medicamentosos ideais com menos efeitos colaterais, a dor crônica leva a uma diminuição da qualidade de vida, além de aumentar o ônus econômico do tratamento. Com esta descoberta, o 'EPA à base de nutrientes' e seus metabólitos podem ser indicados no tratamento da dor crônica, ao mesmo tempo em que mantém os efeitos colaterais afastados.
Elaborando as implicações de longo prazo de sua pesquisa, o professor de pesquisa Miyaji acrescenta que seus "resultados podem ajudar a desenvolver novas estratégias de tratamento e prevenção baseadas em nutrientes, visando a transmissão química purinérgica para doenças inflamatórias, neurológicas e metabólicas, sem os efeitos colaterais adversos de medicamentos convencionais para aliviar a dor."
+ Explorar mais Potencial medicamento para o tratamento da dor crônica com poucos efeitos colaterais
