Pesquisadores descobrem um novo método para testar medicamentos à base de proteínas
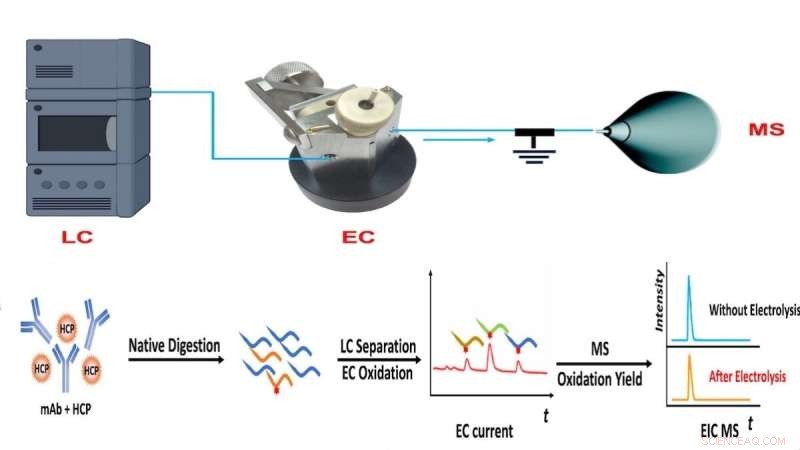
Fluxo de trabalho do método CMS da equipe do NJIT, combinando cromatografia líquida (LC), oxidação eletroquímica (EC) e medição quantitativa baseada em espectrometria de massa (MS) da abundância de proteínas. Crédito:NJIT
Pesquisadores do Instituto de Tecnologia de Nova Jersey (NJIT) revelaram uma nova técnica de laboratório que eles dizem representar uma "mudança de paradigma" em como os laboratórios farmacêuticos testam e produzem novos medicamentos à base de proteínas, como anticorpos monoclonais terapêuticos sendo desenvolvidos para tratar uma variedade de doenças, de câncer a doenças infecciosas.
Pesquisadores dizem que sua abordagem baseada em eletroquímica, descrita na revista
Analytical Chemistry , poderia permitir que testes de segurança e qualidade de bioterapêuticos promissores fossem feitos em uma fração do tempo exigido pelos métodos convencionais, que normalmente exigem a produção demorada e cara de certos biomateriais usados para testes de amostras.
O estudo foi realizado em colaboração com pesquisadores da Merck, Johnson &Johnson e da Universidade de Ohio.
"Este método que desenvolvemos no NJIT tem o potencial de ter um grande impacto na proteômica quantitativa e representa uma mudança de paradigma na indústria farmacêutica em termos de monitoramento de produtos biofarmacêuticos e impurezas de processo para controle de qualidade", disse Hao Chen, pesquisador do artigo. autor correspondente e professor do Departamento de Química e Ciências Ambientais do NJIT.
"Com este estudo, agora demonstramos uma abordagem que pode quantificar produtos farmacêuticos e processar impurezas com muito mais rapidez e precisão do que era possível... Esperamos que se torne muito útil para facilitar o desenvolvimento de proteínas terapêuticas e vacinas para tratamento e prevenção de diferentes doenças no futuro."
Tradicionalmente, esses testes, ou quantificação de proteínas, envolvem a preparação demorada de peptídeos marcados com isótopos sintéticos que são usados como padrões internos para medir as concentrações de proteínas totais em uma amostra – ajudando os pesquisadores a monitorar ativamente a eficácia e a segurança dos componentes proteicos terapêuticos ao longo do desenvolvimento do medicamento processo.
Para superar essa limitação, o laboratório de Chen desenvolveu uma abordagem de espectrometria de massa coulométrica (CMS) para quantificação absoluta de proteínas sem o uso de padrões. Em vez disso, o método aplica espectrometria de massa de cromatografia líquida e uma célula de fluxo eletroquímica para quantificar e detectar rapidamente alterações nas proteínas ou peptídeos alvo com base em assinaturas eletroquímicas.
"Em vez de esperar semanas para obter padrões ou reagentes em abordagens tradicionais, pode-se realizar experimentos de quantificação de CMS imediatamente. Assim, isso facilitaria o rastreamento de impurezas de drogas descobertas durante o processo e garantiria sua eliminação efetiva com otimização e controle do processo", disse Chen.
"Tal aparelho nos permite separar peptídeos após a digestão de proteínas com cromatografia líquida, monitorar a oxidação de peptídeos na célula de fluxo eletroquímico para produzir uma corrente elétrica e medir o rendimento de oxidação com espectrometria de massa", explicou o primeiro autor do artigo e NJIT Ph.D. . estudante Yongling Ai. "A combinação de sinais de corrente elétrica juntamente com o rendimento de oxidação fornece informações suficientes para a quantificação absoluta de peptídeos e proteínas."
Em seu estudo, a equipe demonstrou seu método CMS obtendo a quantificação absoluta de várias proteínas (β-lactoglobulina B, α-lactalbumina e anidrase carbônica) em uma mistura em uma corrida, sem usar nenhum padrão.
Notavelmente, a equipe também apresentou as capacidades do método para detectar a desamidação de proteínas – um evento de degradação comum em proteínas terapêuticas resultantes de estresses físicos ou químicos durante todo o processo de fabricação e armazenamento.
A equipe quantificou com sucesso vários produtos de degradação de proteínas, incluindo um intermediário-chave da degradação de proteínas - a formação de succinimida - que nunca foi feito antes com quantificação absoluta devido à falta de padrões, de acordo com os autores do estudo.
"A falta de padrões é causada pelos desafios em sua síntese de novo", disse Chen. "Ser capaz de quantificar com precisão os produtos e intermediários de desamidação pode fornecer uma melhor compreensão da degradação de proteínas terapêuticas e potencialmente criar uma nova maneira de investigar patologias de doenças e processos de envelhecimento".
Agora, o laboratório de Chen planeja aplicar seu novo método para quantificação em larga escala de milhares de proteínas em uma corrida. Eles também planejam melhorar a sensibilidade de suas análises de CMS para permitir a quantificação de níveis muito baixos de proteínas em amostras biológicas complexas, o que poderia beneficiar os esforços de pesquisa que vão desde diagnóstico clínico e descoberta de medicamentos até medicina de precisão para a qual a identificação e quantificação de amostras em nível molecular é necessário.
"Como as proteínas desempenham uma vasta gama de funções dentro dos organismos, é difícil exagerar a importância da quantificação absoluta de proteínas", disse Chen. "O CMS deve acelerar os processos de diagnóstico de doenças, descoberta e desenvolvimento de medicamentos, e agora abre uma nova porta para biólogos e bioquímicos explorarem quantidades de proteínas no corpo humano que podem servir a funções biológicas importantes ou papéis como biomarcadores de doenças e alvos de medicamentos. "
+ Explorar mais Pesquisadores desenvolvem maneira mais fácil e rápida de quantificar, explorar proteínas terapêuticas
