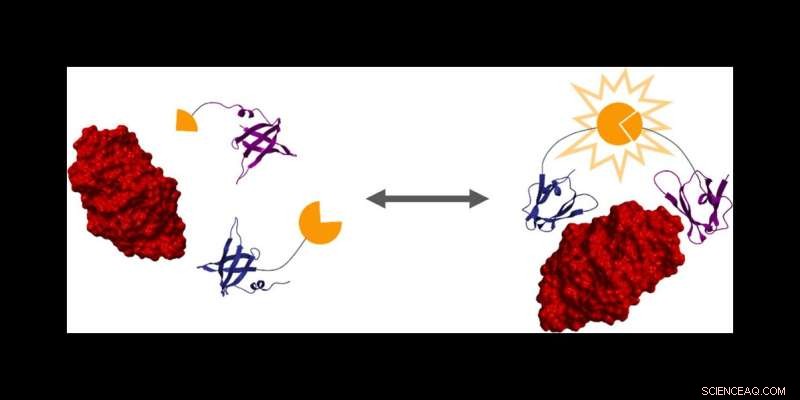
Duas proteínas ligantes (azul e roxa) são projetadas para ligar uma proteína alvo específica (vermelha), como a lisozima. Somente na presença da proteína alvo as duas metades da enzima luciferase dividida (amarela) se unem para criar um sinal bioluminescente. Ao analisar essa interação, os pesquisadores estão desenvolvendo modelos matemáticos que podem prever e controlar a diferenciação. Crédito:Nikki McArthur e Carlos Cruz-Teran
As células estão constantemente tomando decisões que levam à diferenciação. Por exemplo, as células de um embrião tomam uma série de decisões que determinam se elas se tornarão neurônios em alguns casos e células musculares em outros. Como as células tomam essas decisões?
Pesquisadores da Texas A&M University e da North Carolina State University estão determinando como as células facilitam os processos de tomada de decisão. Através deste trabalho, eles esperam medir com precisão as concentrações de proteínas específicas de sinalização vital dentro dos tecidos celulares. Além disso, eles usarão as medições para desenvolver modelos matemáticos que possam prever e controlar a diferenciação celular.
Este estudo foi publicado recentemente no
ACS Omega .
"Queremos entender as decisões de diferenciação, para que possamos aproveitá-las", disse o Dr. Gregory Reeves, professor associado do Departamento de Engenharia Química Artie McFerrin da Texas A&M. "Somos ferramentas de engenharia para entender a diferenciação celular e descrever os processos por meio de equações. Para realizar essas tarefas, precisamos entender as concentrações das proteínas nos tecidos vivos."
No entanto, determinar as concentrações das principais proteínas de sinalização pode ser extremamente difícil. Para combater esse problema, Reeves colaborou com pesquisadores da North Carolina State University que usaram uma estrutura experimental e analítica para desenvolver ensaios de mistura e leitura. Os ensaios de mistura e leitura significam que os reagentes críticos são colocados em combinação com uma célula lisada, permitindo a detecção de luminescência se a proteína alvo estiver presente.
Os pesquisadores então usaram uma técnica de engenharia de proteínas para criar duas proteínas que se ligam fortemente a uma proteína-alvo – neste caso, a lisozima. Esses dois aglutinantes de proteínas são fundidos a duas metades da luciferase, uma enzima que cria bioluminescência, como você veria em um vaga-lume.
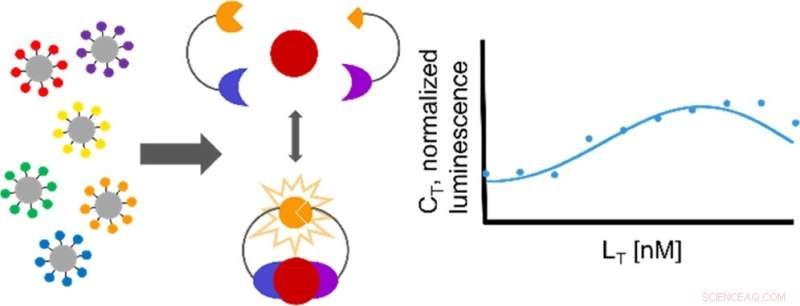
Resumo gráfico. Crédito:ACS Omega (2022). DOI:10.1021/acsomega.2c02319
"Quando a proteína alvo é ligada pelos dois ligantes de proteína projetados, ela une as duas metades da luciferase para criar bioluminescência, que podemos usar para fazer medições", disse Reeves.
Pesquisadores do laboratório de Reeves analisaram um modelo matemático desse método para prever quanta bioluminescência resulta dos eventos de ligação, permitindo-lhes determinar a sensibilidade do ensaio. Isso, por sua vez, ajudará os pesquisadores a obter uma compreensão mais profunda de como e por que as células tomam decisões de diferenciação.
Os impactos mais amplos deste estudo incluem o uso desta técnica para detectar a presença de proteínas-alvo, como anticorpos ou marcadores de câncer regulados positivamente, em um lisado celular.
"Outras aplicações, que usaremos em meu laboratório, incluem permitir-nos medir de forma limpa algumas proteínas que não puderam ser medidas anteriormente em tecidos vivos", disse Reeves.
Os pesquisadores também esperam aplicar esses métodos a outras classes de moléculas difíceis de detectar em tecidos vivos, como o mRNA.
Este trabalho é em colaboração com o autor principal Nikki McArthur, juntamente com o Dr. Balaji Rao, Dr. Carlos Cruz-Teran e Apoorva Thatavarty do Departamento de Engenharia Química e Biomolecular da North Carolina State University.
+ Explorar mais Proteína controlada por luz e temperatura pode informar as vias de sinal celular

