Polipeptídeo de colágeno recombinante como um biomaterial de enxerto ósseo versátil
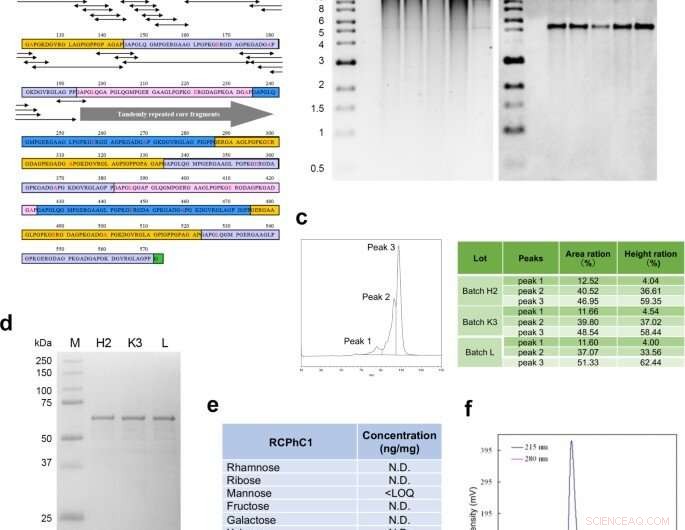 p Desenho molecular e síntese do polipeptídeo recombinante RCPhC1. (a) A sequência de peptídeo de RCPhC1 mostra que Gly-Xaa-Yaa se repete com substituições de aminoácidos (vermelho). Todos os fragmentos de peptídeo (sequências penta mínimas) contendo as substituições de aminoácidos (setas de cabeça dupla) foram combinados com sequências de colágeno humano. (b) Estabilidade do DNA genômico no banco de células de trabalho. Após cada uma das quatro fragmentações consecutivas, O DNA genômico foi isolado (pistas 1–4) e comparado com o DNA genômico original (pistas 5). O painel direito, Southern blot hibridizado com a sonda do promotor AOX1. (c) A reprodutibilidade foi analisada por cromatografia líquida. O perfil de fase reversa mostrou três picos, que foram identificados de forma consistente em três lotes diferentes (H2, K3, e eu). (d) A reprodutibilidade também foi avaliada por SDA-PAGE. A única banda de três lotes diferentes também sugeriu a ausência de modificação pós-tradução. (e) A ausência de glicosilação pós-tradução. (f) A cromatografia de permeação em gel confirmou a alta pureza de RCPhC1. Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
p Desenho molecular e síntese do polipeptídeo recombinante RCPhC1. (a) A sequência de peptídeo de RCPhC1 mostra que Gly-Xaa-Yaa se repete com substituições de aminoácidos (vermelho). Todos os fragmentos de peptídeo (sequências penta mínimas) contendo as substituições de aminoácidos (setas de cabeça dupla) foram combinados com sequências de colágeno humano. (b) Estabilidade do DNA genômico no banco de células de trabalho. Após cada uma das quatro fragmentações consecutivas, O DNA genômico foi isolado (pistas 1–4) e comparado com o DNA genômico original (pistas 5). O painel direito, Southern blot hibridizado com a sonda do promotor AOX1. (c) A reprodutibilidade foi analisada por cromatografia líquida. O perfil de fase reversa mostrou três picos, que foram identificados de forma consistente em três lotes diferentes (H2, K3, e eu). (d) A reprodutibilidade também foi avaliada por SDA-PAGE. A única banda de três lotes diferentes também sugeriu a ausência de modificação pós-tradução. (e) A ausência de glicosilação pós-tradução. (f) A cromatografia de permeação em gel confirmou a alta pureza de RCPhC1. Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
p O padrão ouro atual para cirurgia de enxerto ósseo inclui autoenxertos e aloenxertos, embora exista uma demanda crescente para desenvolver biomateriais sintéticos para biointegração aprimorada na engenharia de tecido ósseo. Em um novo relatório agora publicado em
Materiais de comunicação da natureza , Hideo Fushimi e uma equipe de pesquisa em biociências e engenharia, e biotecnologia reconstrutiva no Japão e nos EUA, desenvolveu um material de suporte biodegradável usando proteínas ou polipeptídeos recombinantes como fonte de materiais de enxerto à base de hidrogel. A equipe usou a cadeia alfa 1 do colágeno tipo I humano (abreviado RCPhC1) como uma fonte para desenvolver o polipeptídeo recombinante e demonstrou a flexibilidade do material para projetar as características ideais para enxertos ósseos. A equipe também desenvolveu enxertos ósseos RCPhC1 usando um sistema altamente escalonável, protocolo de produção simplificado para a geração robusta de tecido ósseo maduro no laboratório. O enxerto ósseo foi completamente reabsorvido após a regeneração do tecido em um modelo animal pré-clínico para integração biológica efetiva. p
Engenharia de tecido ósseo com biomimética, enxertos ósseos sintéticos
p Nesse trabalho, Fushimi et al. desenvolveram um material de enxerto ósseo sintético usando uma proteína recombinante abreviada como RCPhC1. O desenvolvimento fornece uma fonte de material versátil para a fabricação de enxertos ósseos sintéticos por meio de engenharia flexível. Usando estudos pré-clínicos em modelos de defeitos ósseos caninos e roedores, a equipe demonstrou maior eficiência dos enxertos ósseos para regenerar o tecido ósseo com maturidade estrutural. Na ortopedia clínica, a perda de volume e função do tecido é uma marca registrada da lesão, inflamação crônica, e doenças metabólicas e genéticas. Embora o tecido ósseo possa se regenerar ativamente por meio da proliferação e diferenciação osteogênica do estroma mesenquimal ou das células-tronco, grandes defeitos ósseos requerem intervenções cirúrgicas para reparar e reconstruir ossos com materiais de enxerto ósseo.
p Globalmente, Os cirurgiões ortopédicos realizam aproximadamente 2,2 milhões de procedimentos de enxerto ósseo anualmente em um mercado global extremamente caro. O tecido ósseo humano é composto de matriz extracelular orgânica, minerais de cálcio e fósforo cristalizados que formam a hidroxiapatita. Os materiais de enxerto ósseo podem imitar a estrutura e composição bioquímica do tecido ósseo. Os cirurgiões ortopédicos e pesquisadores usaram enxertos ósseos autólogos (células e tecidos obtidos do mesmo indivíduo) para reparar defeitos ósseos devido a questões minerais e imunológicas, embora complicações nos locais da cirurgia possam levar a métodos alternativos de enxerto, como aloenxertos (células e tecidos obtidos de um indivíduo diferente). O desenvolvimento mais recente da biomimética, biomateriais sintéticos para engenharia de tecido ósseo atendem a uma necessidade urgente no setor de saúde de desenvolver novos materiais de enxerto sem usar tecido humano ou animal.
p
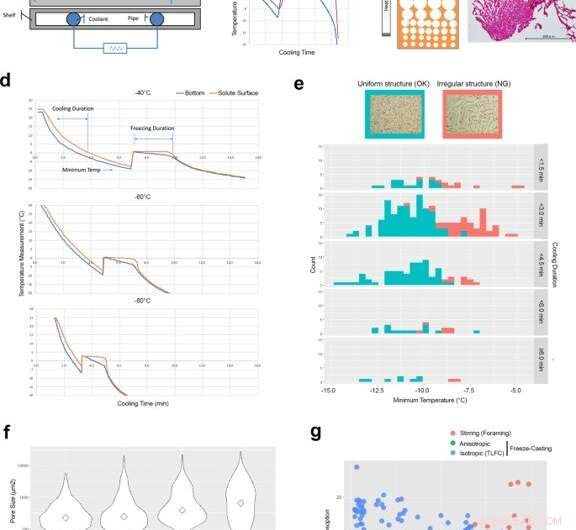 p Fatores de controle de engenharia para desenvolver estruturas isotrópicas modeladas em gelo por fundição por congelamento de camada fina (TLFC). (a) Diagrama do aparelho de fundição por congelamento. (b) Medição de temperatura típica do fundo do copo de resfriamento (azul) e da superfície do soluto (vermelho) durante o processo de fundição por congelamento. Houve uma discrepância significativa entre o copo de resfriamento e a superfície do soluto durante o período de congelamento. (c) Diagrama da estrutura anisotrópica modelada em gelo e a microestrutura RCPhC1 real contendo a zona de poros pequenos. A barra de escala é igual a 500 μm. d TLFC reduziu a discrepância de temperatura entre o copo de resfriamento (azul) e a superfície do soluto (vermelho) durante o período de congelamento. (e) O efeito da temperatura mínima e da duração do resfriamento na estrutura isotrópica dos poros internos. A estrutura de poro uniforme (azul) se desenvolveu quando a temperatura mínima estava abaixo de -10 ° C, mas não foi afetada pela duração do resfriamento. A estrutura de poro interno irregular (vermelho) desenvolveu-se mais frequentemente quando a temperatura mínima estava acima de −10 ° C. A barra de escala é igual a 500 μm. A área verde mostra as contagens de bolos liofilizados uniformemente. A área vermelha mostra as contagens de bolos desidratados irregularmente. (f) O efeito da temperatura do bloco no tamanho do poro interno. Os diamantes mostram valores medianos. As temperaturas mais baixas do bloco aumentaram o número de poros pequenos. A barra de escala é igual a 500 μm. (g) A estrutura interna desenvolvida pela agitação (círculos vermelhos), Os métodos de fundição por congelamento anisotrópico (círculos verdes) e isotrópicos (círculos azuis) foram avaliados por meio de análises de absorção de água e decomposição ácida. As esponjas RCPhC1 foram tentativamente reticuladas desidrotérmicas a 130 ° C durante 7 h. As linhas azuis nos painéis b e d indicam o registro de temperatura do termopar na parte inferior das soluções. As linhas vermelhas indicam que na superfície da solução. Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
Engenharia do polipeptídeo recombinante e do material de enxerto
p Fatores de controle de engenharia para desenvolver estruturas isotrópicas modeladas em gelo por fundição por congelamento de camada fina (TLFC). (a) Diagrama do aparelho de fundição por congelamento. (b) Medição de temperatura típica do fundo do copo de resfriamento (azul) e da superfície do soluto (vermelho) durante o processo de fundição por congelamento. Houve uma discrepância significativa entre o copo de resfriamento e a superfície do soluto durante o período de congelamento. (c) Diagrama da estrutura anisotrópica modelada em gelo e a microestrutura RCPhC1 real contendo a zona de poros pequenos. A barra de escala é igual a 500 μm. d TLFC reduziu a discrepância de temperatura entre o copo de resfriamento (azul) e a superfície do soluto (vermelho) durante o período de congelamento. (e) O efeito da temperatura mínima e da duração do resfriamento na estrutura isotrópica dos poros internos. A estrutura de poro uniforme (azul) se desenvolveu quando a temperatura mínima estava abaixo de -10 ° C, mas não foi afetada pela duração do resfriamento. A estrutura de poro interno irregular (vermelho) desenvolveu-se mais frequentemente quando a temperatura mínima estava acima de −10 ° C. A barra de escala é igual a 500 μm. A área verde mostra as contagens de bolos liofilizados uniformemente. A área vermelha mostra as contagens de bolos desidratados irregularmente. (f) O efeito da temperatura do bloco no tamanho do poro interno. Os diamantes mostram valores medianos. As temperaturas mais baixas do bloco aumentaram o número de poros pequenos. A barra de escala é igual a 500 μm. (g) A estrutura interna desenvolvida pela agitação (círculos vermelhos), Os métodos de fundição por congelamento anisotrópico (círculos verdes) e isotrópicos (círculos azuis) foram avaliados por meio de análises de absorção de água e decomposição ácida. As esponjas RCPhC1 foram tentativamente reticuladas desidrotérmicas a 130 ° C durante 7 h. As linhas azuis nos painéis b e d indicam o registro de temperatura do termopar na parte inferior das soluções. As linhas vermelhas indicam que na superfície da solução. Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
Engenharia do polipeptídeo recombinante e do material de enxerto
p A equipe usou colágeno tipo I, abundantemente expresso em tecidos conjuntivos e membranas intersticiais como um dos principais componentes orgânicos do tecido ósseo. A sequência de proteínas do colágeno tipo I desempenha um papel importante no estabelecimento da resistência mecânica do osso. A equipe primeiro clonou o DNA complementar (cDNA) - uma cópia de DNA de uma molécula de RNA mensageiro (mRNA) que codifica o polipeptídeo (sequência de proteína) RCPhC1, em um vetor de expressão. Para conseguir isso, eles usaram uma espécie de levedura metilotrófica conhecida como Pichia pastoris para transferir a sequência e gerar bancos de células mestre e de trabalho. A equipe confirmou a composição de aminoácidos do polipeptídeo sintético e caracterizou extensivamente o produto.
p Em seguida, eles projetaram a estrutura interna do material de enxerto para atender aos requisitos específicos do tecido-alvo. Para gerar uma estrutura de poro uniforme, Portanto, Fushimi et al. projetou um protocolo de fundição por congelamento de camada fina (TLFC). A abordagem de congelamento versátil gerou um grande número de poros com paredes finas para formar um andaime RCPhC1 isotrópico com várias estruturas internas.
p
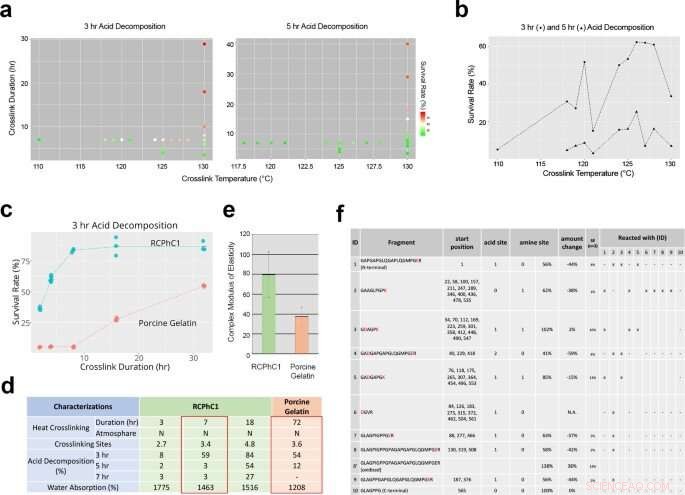 p Fatores de engenharia que afetam a reticulação desidrotérmica de RCPhC1 para controlar a taxa de biodegradação e a resistência mecânica. (a) O efeito da temperatura de reticulação e duração da reticulação na taxa de biodegradação avaliada por análise de decomposição ácida in vitro. (b) A temperatura de reticulação não influenciou linearmente a taxa de sobrevivência de decomposição de ácido. Considerando a esterilização a jusante, a temperatura de reticulação foi fixada em 130 ° C. (c) A duração da reticulação foi considerada o fator de controle predominante, o que aumentou linearmente a taxa de sobrevivência de decomposição ácida de RCPhC1 por até 10 h. O material de gelatina suína respondeu de forma semelhante à duração da reticulação, embora requeira uma duração muito mais longa. (d) Propriedade física de RCPhC1 reticulado desidrotérmico. A propriedade física equivalente da gelatina suína reticulada desidrotérmica requer uma duração de reticulação 10 vezes mais longa. (e) A resistência mecânica de RCPhC1 reticulado desidrotérmico (130 ° C, 7 h) foi significativamente maior do que a de gelatina suína reticulada desidrotérmica (130 ° C, 72 h). A barra de erro representa s.d. (f) RCPhC1 reticulado desidrotérmico (130 ° C, 7 h) foi tratada com tripsina e submetida a LC de alto desempenho. A co-migração de fragmentos de peptídeo indicou vários locais de reticulação. Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
Perfil de reticulação desidrotérmica e otimização do material para regeneração óssea
p Fatores de engenharia que afetam a reticulação desidrotérmica de RCPhC1 para controlar a taxa de biodegradação e a resistência mecânica. (a) O efeito da temperatura de reticulação e duração da reticulação na taxa de biodegradação avaliada por análise de decomposição ácida in vitro. (b) A temperatura de reticulação não influenciou linearmente a taxa de sobrevivência de decomposição de ácido. Considerando a esterilização a jusante, a temperatura de reticulação foi fixada em 130 ° C. (c) A duração da reticulação foi considerada o fator de controle predominante, o que aumentou linearmente a taxa de sobrevivência de decomposição ácida de RCPhC1 por até 10 h. O material de gelatina suína respondeu de forma semelhante à duração da reticulação, embora requeira uma duração muito mais longa. (d) Propriedade física de RCPhC1 reticulado desidrotérmico. A propriedade física equivalente da gelatina suína reticulada desidrotérmica requer uma duração de reticulação 10 vezes mais longa. (e) A resistência mecânica de RCPhC1 reticulado desidrotérmico (130 ° C, 7 h) foi significativamente maior do que a de gelatina suína reticulada desidrotérmica (130 ° C, 72 h). A barra de erro representa s.d. (f) RCPhC1 reticulado desidrotérmico (130 ° C, 7 h) foi tratada com tripsina e submetida a LC de alto desempenho. A co-migração de fragmentos de peptídeo indicou vários locais de reticulação. Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
Perfil de reticulação desidrotérmica e otimização do material para regeneração óssea
p Fushimi et al. em seguida, submeteu o material a um tratamento de reticulação desidrotérmico para testar o efeito da temperatura e duração da reticulação em sua composição. Depois de testar o produto a jusante para contaminação microbiana, a temperatura durante o processo de fabricação foi confirmada para ser eficaz para esterilização por calor seco. Testes adicionais mostraram como a composição única de aminoácidos da proteína recombinante contribuiu para sua robusta eficiência de reticulação hidrotérmica. Em seguida, a equipe otimizou o material de proteína recombinante para enxerto ósseo, regulando a concentração do material polipeptídico e sua temperatura de congelamento com base no volume de osso induzido por enxerto em um modelo de defeito ósseo da calvária (crânio) de rato. Quatro semanas após enxertar o material no modelo animal, a equipe usou estimativa de volume ósseo baseada em micro tomografia computadorizada (micro TC). Os resultados indicaram uma concentração ideal de 7,5 por cento RCPhC1, uma temperatura de congelamento de -40 a -60 graus Celsius, e reticulação desidrotérmica a 130 ° C durante 7 horas para ser mais adequado para o fabrico de material de enxerto ósseo recombinante.
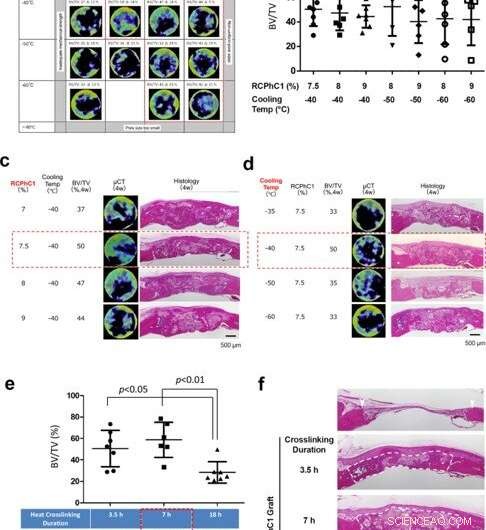 p Otimização dos fatores de controle de engenharia. (a) Otimização de fatores combinados de concentração de soluto RCPhC1 e temperatura de bloco TLFC, com a reticulação desidrotérmica tentativa a 130 ° C durante 7 h. O intervalo ideal foi reduzido para a concentração de RCPhC1 entre 7,5 e 9% e a temperatura do bloco TLFC entre −40 e −60 ° C (bloco pontilhado vermelho). (b) Medições de BV / TV dentro do grupo da faixa ótima de concentração de RCP1C1 e temperatura de resfriamento. Não houve diferença estatística entre os grupos. (c) O efeito da concentração do soluto RCPhC1 na regeneração óssea. A barra de escala é igual a 500 μm. (d) O efeito da temperatura do bloco TLFC na regeneração óssea. A barra de escala é igual a 500 μm. (e) O efeito da duração da reticulação desidrotérmica na formação óssea. (n =7; teste de comparação múltipla de Tukey) (f). O efeito da duração da reticulação desidrotérmica na manutenção do espaço de cicatrização de feridas no defeito ósseo da calvária de rato. Pontas de flechas brancas mostram bordas defeituosas. Linhas brancas pontilhadas circundam o tecido recém-formado. A barra de escala é igual a 500 μm. Linhas horizontais em b, e e representa a média ± dp. Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
p Otimização dos fatores de controle de engenharia. (a) Otimização de fatores combinados de concentração de soluto RCPhC1 e temperatura de bloco TLFC, com a reticulação desidrotérmica tentativa a 130 ° C durante 7 h. O intervalo ideal foi reduzido para a concentração de RCPhC1 entre 7,5 e 9% e a temperatura do bloco TLFC entre −40 e −60 ° C (bloco pontilhado vermelho). (b) Medições de BV / TV dentro do grupo da faixa ótima de concentração de RCP1C1 e temperatura de resfriamento. Não houve diferença estatística entre os grupos. (c) O efeito da concentração do soluto RCPhC1 na regeneração óssea. A barra de escala é igual a 500 μm. (d) O efeito da temperatura do bloco TLFC na regeneração óssea. A barra de escala é igual a 500 μm. (e) O efeito da duração da reticulação desidrotérmica na formação óssea. (n =7; teste de comparação múltipla de Tukey) (f). O efeito da duração da reticulação desidrotérmica na manutenção do espaço de cicatrização de feridas no defeito ósseo da calvária de rato. Pontas de flechas brancas mostram bordas defeituosas. Linhas brancas pontilhadas circundam o tecido recém-formado. A barra de escala é igual a 500 μm. Linhas horizontais em b, e e representa a média ± dp. Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
p
Regeneração robusta de tecido ósseo vital em modelos pré-clínicos com materiais de enxerto
p Com base nas condições ideais verificadas experimentalmente, Fushimi et al. fabricou os enxertos ósseos RCPhC1 com grânulos porosos. Usando o modelo de defeito ósseo da calvária em rato, eles mostraram como o enxerto ósseo induziu a regeneração óssea de forma robusta dentro da estrutura interna dos poros, enquanto se degradam gradualmente in vivo, para indicar biocompatibilidade e biointegração eficaz. Eles compararam este resultado com um xenoenxerto de osso esponjoso descelularizado bovino (vaca) comercialmente disponível e não observaram uma regeneração óssea significativamente maior. A equipe então testou o material de enxerto ósseo em um modelo pré-clínico canino de extração dentária para compreender a cicatrização de feridas na cavidade dentária, onde o alvéolo de extração tratado com o enxerto ósseo mostrou formação óssea melhorada em 12 semanas. Por esta hora, como esperado, o enxerto ósseo foi amplamente substituído por tecido ósseo.
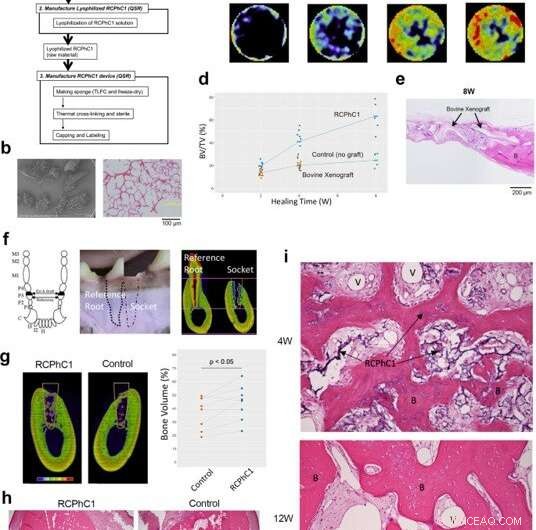 p Teste de eficácia pré-clínica do material RCPhC1 otimizado para enxerto ósseo em modelos de roedores e caninos. (a) Fluxograma do processo de fabricação do enxerto ósseo RCPhC1. A barra de escala é igual a 100 μm. (b) O enxerto ósseo RCPhC1 foi preparado como grânulos porosos de tamanho 300-1200 µm para melhor manuseio. A barra de escala é igual a 100 μm. (c) Curso de tempo de regeneração óssea induzida por enxerto ósseo RCPhC1 no modelo de defeito calvarial de rato. A análise histológica (linha superior) revelou tecido ósseo recém-formado (B) dentro do material de enxerto RCPhC1, que foi reabsorvido com o tempo. Uma série de curso de tempo de microCT in vivo (linha inferior) descreveu o aumento progressivo no tecido ósseo. (d) Curso de tempo de medição de BV / TV de defeito ósseo da calvária de rato implantado com enxerto ósseo RCPhC1, xenoenxerto de osso esponjoso decelularizado bovino e sem controle de enxerto. (e) Avaliação histológica de xenoenxerto bovino implantado em defeito ósseo de calvária de rato. A estrutura física do xenoenxerto bovino foi semelhante à do enxerto ósseo RCPhC1. Na periferia do defeito, xenoenxerto bovino foi visto fundido ao osso neoformado (B). No centro do defeito, grânulos de xenoenxerto bovino foram circundados por tecido fibroso. A barra de escala é igual a 200 μm. (f) Modelo de extração dentária canina. O terceiro pré-molar canino (P3) tem raízes mesiais e distais quase idênticas. O terceiro pré-molar foi hemi-seccionado e apenas a raiz distal foi extraída. Um lado do alvéolo ósseo pós-extração foi preenchido com RCPhC1 enquanto o outro lado foi deixado para cicatrizar sem qualquer tratamento adicional. A raiz medial remanescente foi tratada endodonticamente e serviu de referência. A barra de escala é igual a 4 mm. (g) Corte transversal MicroCT que descreve a regeneração óssea no alvéolo de extração (linha branca) após 12 semanas (12 W) de cicatrização. O volume ósseo dentro do alvéolo foi significativamente maior no alvéolo implantado com enxerto ósseo RCPhC1 do que no alvéolo de controle não tratado (n =8; teste t pareado bilateral). A barra de escala é igual a 4 mm. (h) Corte histológico do alvéolo de extração (linha branca) em 12 W. O alvéolo que recebeu o enxerto ósseo RCPhC1 exibiu maior regeneração óssea. Linhas brancas pontilhadas mostram interfaces de soquete. A barra de escala é igual a 1 mm. (i) Avaliação histológica da regeneração óssea associada ao enxerto ósseo RCPhC1 (I). Foi observada formação vascular abundante (II) no tecido da medula óssea de osso em regeneração (III) após 4 semanas (4 W) de cura. O enxerto ósseo RCPhC1 foi amplamente reabsorvido após 12 W de cura. O osso regenerado continha osteócitos vitais (IV). Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
p Teste de eficácia pré-clínica do material RCPhC1 otimizado para enxerto ósseo em modelos de roedores e caninos. (a) Fluxograma do processo de fabricação do enxerto ósseo RCPhC1. A barra de escala é igual a 100 μm. (b) O enxerto ósseo RCPhC1 foi preparado como grânulos porosos de tamanho 300-1200 µm para melhor manuseio. A barra de escala é igual a 100 μm. (c) Curso de tempo de regeneração óssea induzida por enxerto ósseo RCPhC1 no modelo de defeito calvarial de rato. A análise histológica (linha superior) revelou tecido ósseo recém-formado (B) dentro do material de enxerto RCPhC1, que foi reabsorvido com o tempo. Uma série de curso de tempo de microCT in vivo (linha inferior) descreveu o aumento progressivo no tecido ósseo. (d) Curso de tempo de medição de BV / TV de defeito ósseo da calvária de rato implantado com enxerto ósseo RCPhC1, xenoenxerto de osso esponjoso decelularizado bovino e sem controle de enxerto. (e) Avaliação histológica de xenoenxerto bovino implantado em defeito ósseo de calvária de rato. A estrutura física do xenoenxerto bovino foi semelhante à do enxerto ósseo RCPhC1. Na periferia do defeito, xenoenxerto bovino foi visto fundido ao osso neoformado (B). No centro do defeito, grânulos de xenoenxerto bovino foram circundados por tecido fibroso. A barra de escala é igual a 200 μm. (f) Modelo de extração dentária canina. O terceiro pré-molar canino (P3) tem raízes mesiais e distais quase idênticas. O terceiro pré-molar foi hemi-seccionado e apenas a raiz distal foi extraída. Um lado do alvéolo ósseo pós-extração foi preenchido com RCPhC1 enquanto o outro lado foi deixado para cicatrizar sem qualquer tratamento adicional. A raiz medial remanescente foi tratada endodonticamente e serviu de referência. A barra de escala é igual a 4 mm. (g) Corte transversal MicroCT que descreve a regeneração óssea no alvéolo de extração (linha branca) após 12 semanas (12 W) de cicatrização. O volume ósseo dentro do alvéolo foi significativamente maior no alvéolo implantado com enxerto ósseo RCPhC1 do que no alvéolo de controle não tratado (n =8; teste t pareado bilateral). A barra de escala é igual a 4 mm. (h) Corte histológico do alvéolo de extração (linha branca) em 12 W. O alvéolo que recebeu o enxerto ósseo RCPhC1 exibiu maior regeneração óssea. Linhas brancas pontilhadas mostram interfaces de soquete. A barra de escala é igual a 1 mm. (i) Avaliação histológica da regeneração óssea associada ao enxerto ósseo RCPhC1 (I). Foi observada formação vascular abundante (II) no tecido da medula óssea de osso em regeneração (III) após 4 semanas (4 W) de cura. O enxerto ósseo RCPhC1 foi amplamente reabsorvido após 12 W de cura. O osso regenerado continha osteócitos vitais (IV). Crédito:Nature Communications Materials, doi:10.1038 / s43246-020-00089-9
p
Perspectiva de andaimes sintéticos na engenharia de tecido ósseo
p Desta maneira, Hideo Fushimi e colegas otimizaram um simples, mas um processo de engenharia crítico para regular a concentração de soluto de um polipeptídeo recombinante da proteína de cadeia alfa I do colágeno tipo I humano com substituições de aminoácidos direcionadas, abreviado como RCPhC1. A equipe primeiro implantou o construto em um modelo de defeito ósseo da calvária de rato para entender os fatores de engenharia ideais para fabricar o enxerto ósseo. Eles projetaram o material de enxerto ósseo para apoiar a migração de células-tronco mesenquimais (MSCs) em direção à área do defeito e forneceram um microambiente estimulante para a diferenciação osteogênica. O material de enxerto ósseo sozinho mostrou um padrão de cicatrização ideal na ausência de fatores de crescimento e células-tronco para regenerar o osso. O material pode ser usado para gerar dispositivos médicos específicos para tecidos e estruturas de enxerto com versatilidade de fabricação significativa em engenharia de tecido ósseo. p © 2020 Science X Network




