Moléculas de ligação ao gelo impedem o crescimento do gelo, agir como anticongelante natural
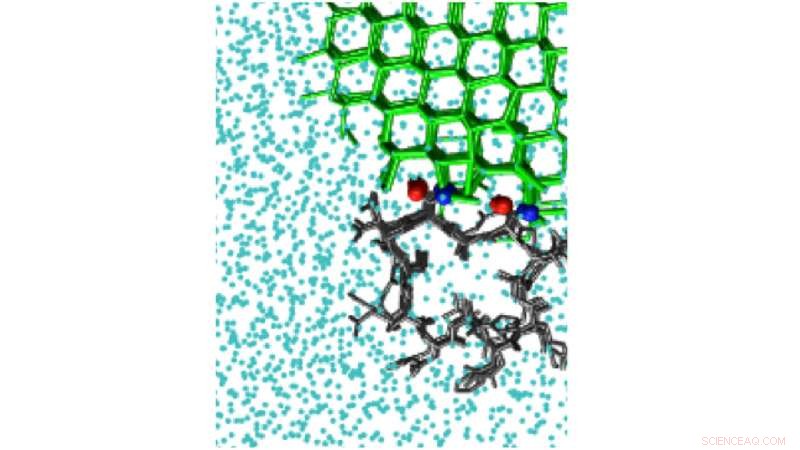 p Simulações de polarização de gelo podem detectar o local de ligação ao gelo da proteína anticongelante hiperativa do besouro Tenebrio molitor, TmAFP. Crédito:Pavithra M. Naullage
p Simulações de polarização de gelo podem detectar o local de ligação ao gelo da proteína anticongelante hiperativa do besouro Tenebrio molitor, TmAFP. Crédito:Pavithra M. Naullage
p Certas moléculas se ligam fortemente à superfície do gelo, criando uma interface curva que pode interromper o crescimento de gelo. Alguns insetos, plantas, e criaturas marinhas contêm moléculas de proteína deste tipo que atuam como agentes anticongelantes naturais, permitindo que os organismos resistam a temperaturas de congelamento. p No
The Journal of Chemical Physics , os cientistas relatam um método computacional para modelar a ligação do gelo usando uma técnica de polarização para conduzir a formação de gelo na simulação.
p As proteínas anticongelantes atuam ligando-se a uma interface existente entre o gelo e a água líquida. A superfície curva resultante impede o crescimento de gelo. Existem também moléculas de nucleação de gelo que catalisam a formação de gelo a partir da água líquida super-resfriada.
p Ambos os fenômenos requerem uma compreensão da maneira como as moléculas se ligam ao gelo. Compreender a ligação do gelo é importante para aplicações tão diversas como criopreservação de órgãos e modelagem climática, mas nenhum método computacional para modelar eficientemente este fenômeno existiu até o momento.
p "A vantagem central da abordagem de simulação de polarização do gelo é que ela identifica simultaneamente a superfície de ligação do gelo, a face de gelo a que se liga, e o modo de ligação, "disse a autora Valeria Molinero.
p Os investigadores criaram dois tipos de modelos. Um tipo é um modelo de todos os átomos que contém todos os átomos nas fases líquida e de gelo da água, bem como na molécula do tipo anticongelante. O outro tipo de modelo estudado é chamado de modelo de granulação grossa, que economiza recursos computacionais ao combinar átomos em estruturas mais simples.
p O estudo analisou várias moléculas que ligam o gelo, incluindo álcool polivinílico, um inibidor de recristalização de gelo sintético, bem como proteínas anticongelantes naturais, como um do besouro Tenebrio molitor. As proteínas apresentam um desafio de simulação, uma vez que têm superfícies muito pequenas que prendem o gelo. Isso limita o tamanho do cristal de gelo que eles podem ligar.
p Alguns sistemas possuem mais de um local onde o gelo pode se ligar. Este é o caso da proteína anticongelante natural da diatomácea Frailariopsis cylindrus. Para determinar se uma proteína como esta tem mais de uma superfície de ligação ao gelo, SII, os investigadores desenvolveram um método que apelidaram de "limite e repetição".
p “Nesta estratégia, primeiro realizamos uma simulação tendenciosa para detectar um IBS. Então, limitamos aquele IBS para evitar a formação de gelo nele e realizamos uma segunda simulação de polarização para descobrir se o gelo se forma em outros locais, "disse Molinero.
p Os métodos desenvolvidos neste estudo mostram uma grande promessa para uma série de aplicações, incluindo a descoberta de moléculas para proteger os tecidos congelados durante o armazenamento, promovendo a compreensão das proteínas anticongelantes naturais, e em modelos climáticos, onde a nucleação do gelo na atmosfera desempenha um papel fundamental.
