 p Crédito CC0:domínio público
p Crédito CC0:domínio público
p Cientistas do NUS descobriram um novo mecanismo para redução eletroquímica seletiva de dióxido de carbono (CO
2 ) a etanol usando catalisadores compostos de cobre-prata (Cu-Ag). p Redução eletroquímica de CO
2 a combustíveis e produtos químicos, quando alimentado por eletricidade renovável, é um passo em frente na redução das emissões de carbono. Os materiais de cobre (Cu) são os catalisadores escolhidos para esse processo porque têm as atividades eletroquímicas mais altas para produtos multicarbono. Contudo, sua seletividade em relação ao etanol (C
2 H
5 OH), um combustível valioso e matéria-prima química, é sempre inferior ao do etileno (C
2 H
4 ) A preferência pela produção de etileno em relação ao etanol surge do mecanismo de dimerização do CO para a produção de C
2 moléculas de CO
2 , onde a formação de etileno, que tem uma barreira de energia mais baixa, é preferido em relação ao etanol.
p Uma equipe de pesquisa liderada pelo Prof Yeo Boon Siang, Jason, do Departamento de Química da NUS, em colaboração com uma equipe liderada pelo Dr. Federico Calle-Vallejo da Universidade de Barcelona, mostrou que um influxo de moléculas de CO, fornecido por cocatalisadores de prata (Ag), ativa uma via mecanística de outra forma bloqueada em Cu, que converte CO
2 gás para etanol.
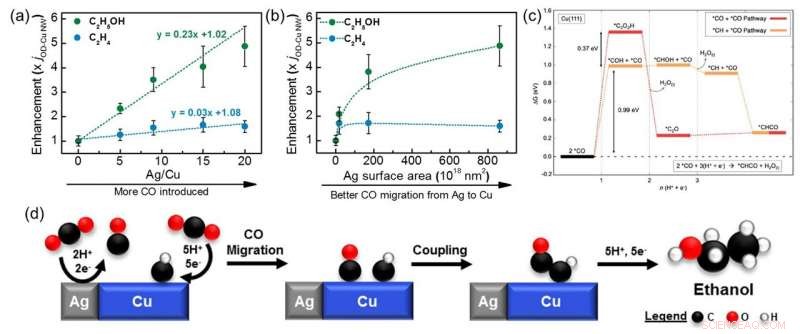 p Gráficos mostrando como o aumento da produção de etanol (verde) e etileno (azul) em compósitos de cobre-prata (Cu-Ag) varia com diferentes (a) razões Ag / Cu e (b) tamanhos de partículas de Ag. Um aumento de cinco vezes foi observado para o etanol, enquanto o etileno não foi significativamente impactado. (c) Diagrama de nível de energia mostrando as etapas de acoplamento CO + CO (vermelho) e CO + CH (laranja) em Cu (111). Uma barreira inferior é necessária para o acoplamento CO + CH, tornando-o mais favorável do que o passo CO + CO. (d) Esquema mostrando o mecanismo de redução de CO2 a etanol em compósitos Cu-Ag via acoplamento CO + CH. Crédito:ACS Catalysis
p Gráficos mostrando como o aumento da produção de etanol (verde) e etileno (azul) em compósitos de cobre-prata (Cu-Ag) varia com diferentes (a) razões Ag / Cu e (b) tamanhos de partículas de Ag. Um aumento de cinco vezes foi observado para o etanol, enquanto o etileno não foi significativamente impactado. (c) Diagrama de nível de energia mostrando as etapas de acoplamento CO + CO (vermelho) e CO + CH (laranja) em Cu (111). Uma barreira inferior é necessária para o acoplamento CO + CH, tornando-o mais favorável do que o passo CO + CO. (d) Esquema mostrando o mecanismo de redução de CO2 a etanol em compósitos Cu-Ag via acoplamento CO + CH. Crédito:ACS Catalysis
p Uma série de catalisadores compostos Cu-Ag, fabricado a partir de uma mistura de nanofios de Cu derivados de óxidos e pós de Ag, foram testados para seu CO eletroquímico
2 atividades de redução. Durante CO
2 redução, Ag converte CO
2 para CO e essas moléculas de CO migram para os sítios ativos de Cu para posterior redução em hidrocarbonetos (etileno) e álcoois (etanol). Os pesquisadores variaram a razão Ag / Cu e os tamanhos das partículas de Ag nos compósitos para aumentar o influxo de CO do Ag para os sítios ativos no material de Cu. Os resultados experimentais mostraram que o aumento do influxo de CO aumentou a produção de etanol em até cinco vezes, com pouco impacto na produção de eteno. Simulações teóricas sobre o mecanismo de reação mostram que, em vez da etapa CO + CO que resulta na formação de etileno, o CO + CH
x etapa foi a etapa de formação da ligação C-C dominante na interface Cu-Ag. O etanol foi o único produto quando a reação prossegue através do CO + CH
x Passo, que se verificou ocorrer em sítios ativos diferentes daqueles que facilitaram a formação de etileno por meio da etapa CO + CO.
p Outros planos decorrentes desta descoberta pela equipe de pesquisa incluem maximizar os locais ativos por meio do projeto do catalisador e da produção em escala crescente usando uma configuração de célula de fluxo de alto rendimento.
p Prof Yeo disse, “O conceito de que uma via previamente fechada pode ser aberta por um influxo de intermediários, como demonstrado neste trabalho, abre novas possibilidades para descobrir novos mecanismos sintéticos que antes poderiam ser inacessíveis. "

