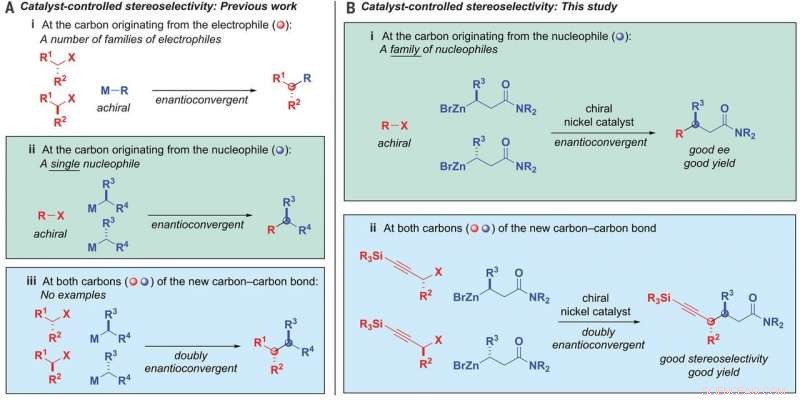
Formação de ligação alquil-alquil. (A) Estereosseletividade controlada por catalisador - trabalho anterior. (B) Estereosseletividade controlada por catalisador - este estudo. ee, excesso enantiomérico; M, metal; R, substituinte; X, saindo do grupo. Crédito: Ciência (2020). DOI:10.1126 / science.aaz3855
Uma equipe de pesquisadores do California Institute of Technology encontrou um catalisador de níquel que liga o alquil nucleófilo e os alquil eletrófilos para formar um único estereoisômero com dois centros quirais. Em seu artigo publicado na revista Ciência , o grupo descreve seu processo. Jianyu Xu e Mary Watson, da University of Delaware, publicaram um artigo em Perspectiva sobre o trabalho realizado pela equipe na mesma edição do jornal.
Na quimica, as reações que resultam em materiais com ligações carbono-carbono são desejáveis porque são usadas em aplicações de grande escala, como produtos farmacêuticos e agrícolas. Essas reações normalmente dependem de catalisadores à base de metais de transição - mas existem limitações que impedem que muitos sejam usados. Muitos só funcionam com compostos alquil, o que pode levar a reações colaterais indesejáveis. Também, muitas dessas reações resultam em misturas racêmicas de produtos, resultando em ineficiências (misturas racêmicas são aquelas que têm quantidades iguais de enantiômeros destros e esquerdos de uma molécula quiral).
Ligar misturas racêmicas de dois alquilos enquanto mantém o controle da estereoquímica de ambas as extremidades do produto tem sido historicamente considerado muito difícil. Mas agora, isso mudou, graças ao trabalho da equipe do CIT, e isso levou a um método para realizar reações que levam a materiais desejáveis com ligações carbono-carbono.
Em seu trabalho, a equipe desenvolveu um catalisador de níquel que permite que um alquil nucleófilo se ligue a um alquil eletrófilo. Notavelmente, ambos são compostos de carbono racêmicos. Eles usaram um ligante que era bidentado - que permitia que pontos abertos no níquel se ligassem ao oxigênio nos nucleófilos.
A reação também envolveu o uso de nucleófilos de amida β-zincada e eletrófilos de haleto propargílico. E foi controlado pelo catalisador. Substituindo as informações quirais em ambos os produtos iniciais e, em seguida, reunindo-os novamente de uma forma predefinida, as ligações carbono-carbono foram formadas. O resultado foi um único estereoisômero que tinha dois centros quirais. Ao usar o catalisador de níquel, o grupo acoplou uma mistura racêmica com nucleófilos e eletrófilos com até 95 por cento de estereosseletividade e 82 por cento de rendimento. Os testes também mostraram que era compatível com 19 grupos funcionais.
© 2020 Science X Network