Descobertas fundamentais para futuras nanoferramentas:os químicos distinguem várias forças fracas
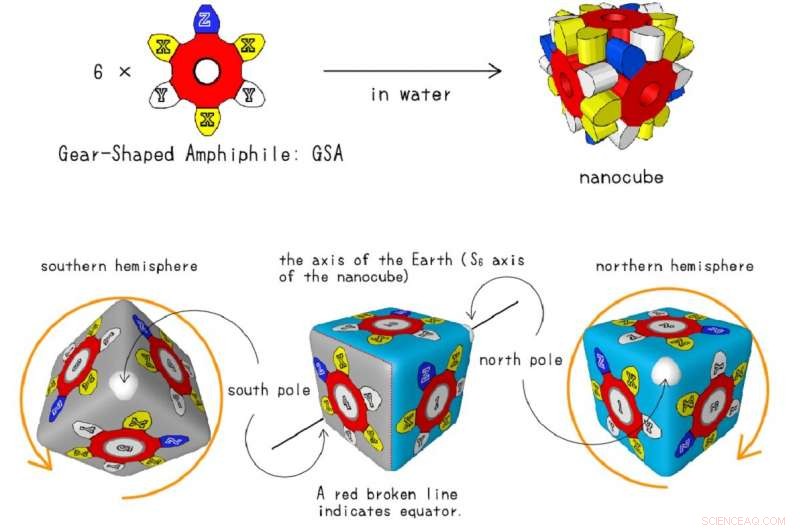
 p Dobre seu próprio nanocubo! Embora os nanocubos usados no projeto de pesquisa se construam, você pode dobrar o seu próprio usando este modelo. Cada X amarelo representa locais onde os pesquisadores da Universidade de Tóquio usaram átomos diferentes com diferentes níveis de polarizabilidade. Crédito:Shuichi Hiraoka, CC-BY-ND
p Dobre seu próprio nanocubo! Embora os nanocubos usados no projeto de pesquisa se construam, você pode dobrar o seu próprio usando este modelo. Cada X amarelo representa locais onde os pesquisadores da Universidade de Tóquio usaram átomos diferentes com diferentes níveis de polarizabilidade. Crédito:Shuichi Hiraoka, CC-BY-ND
p O processo de construção de um minúsculo cubo revelou alguns dos mistérios fundamentais de como as moléculas se unem em ambientes naturais. Os pesquisadores esperam aplicar esse conhecimento a projetos futuros de criação de estruturas complexas que podem imitar a vida. p Quando duas moléculas rodeadas por água se movem uma em direção à outra, parte de sua atração inicial às vezes se deve à força química para repelir a água - o efeito hidrofóbico.
p Uma vez que as moléculas estão próximas umas das outras, mas ainda não formalmente vinculado, uma força muito mais fraca torna-se importante - a força de dispersão.
p "Nosso sonho é controlar a força de dispersão e fornecer um princípio de design simples para usar a força de dispersão para construir estruturas complexas de automontagem, "disse o professor Shuichi Hiraoka, líder do laboratório onde a pesquisa foi realizada no Departamento de Ciências Básicas da Universidade de Tóquio.
p As forças de dispersão são um tipo de forças de van der Waals, algumas das interações químicas mais fracas conhecidas na natureza. Embora fraco, As forças de van der Waals são importantes; eles ajudam as lagartixas a subir pelas paredes e foram previamente identificados em 2018 pelo mesmo grupo de pesquisa como travando as moléculas em forma de engrenagem ou floco de neve dos nanocubos de automontagem.
p Medir a força de dispersão em condições naturais, como quando as moléculas estão em solução com água, tem sido impossível. A força é tão fraca que não pode ser identificada separadamente das outras forças em jogo.
p Contudo, em novos experimentos, a equipe de pesquisa usou seus nanocubos de automontagem como ferramentas para amplificar as diferenças na força de dispersão.
p As moléculas que compõem as laterais dos cubos foram modificadas para conter átomos selecionados por sua polarizabilidade, significando sua capacidade de resposta ao campo elétrico circundante. Cada nanocubo totalmente montado continha 18 desses átomos polarizáveis.
p O efeito combinado de 18 átomos foi suficiente para criar diferenças mensuráveis na força de dispersão, dependendo de qual átomo polarizável estava ligado.
 p O nanocubo totalmente montado é representado nesta ilustração. Cada X amarelo é um local onde os pesquisadores da Universidade de Tóquio usaram átomos diferentes selecionados por sua polarizabilidade. O efeito combinado de 18 átomos de polaridade variável em cada nanocubo permitiu aos pesquisadores medir as diferenças na força de dispersão. Crédito:Shuichi Hiraoka, CC-BY.
p O nanocubo totalmente montado é representado nesta ilustração. Cada X amarelo é um local onde os pesquisadores da Universidade de Tóquio usaram átomos diferentes selecionados por sua polarizabilidade. O efeito combinado de 18 átomos de polaridade variável em cada nanocubo permitiu aos pesquisadores medir as diferenças na força de dispersão. Crédito:Shuichi Hiraoka, CC-BY.
p A força de dispersão é calculada matematicamente após o uso de uma técnica chamada calorimetria de titulação isotérmica para medir a quantidade de calor liberado quando as moléculas se ligam.
p Átomos mais polarizáveis criaram forças de dispersão mais fortes e tornaram os nanocubos mais estáveis. Dependendo do valor estimado do efeito hidrofóbico, a força de dispersão contribui de 0,6 a 2,2 vezes mais força atrativa e estabilidade para o cubo do que o efeito hidrofóbico.
p Os pesquisadores planejam usar esse conhecimento sobre átomos mais polarizáveis criando forças de dispersão mais fortes para projetar futuras estruturas moleculares artificiais com formas mais complexas e funções aumentadas.
p "Por exemplo, poderíamos projetar moléculas com áreas de superfície de ligação maiores e colocar átomos polares ao longo das bordas para aumentar a estabilidade geral por meio da atração de forças de dispersão, "disse Hiraoka.
p
Resolvendo um mistério no design de medicamentos
p Hiraoka afirma que as medições para nanocubos construídos com hidrogênio normal em comparação com o deutério, o isótopo "pesado" do hidrogênio, deve ser relevante para a teoria do desenho de medicamentos. Pesquisas por outros grupos levaram a relatórios conflitantes entre os químicos sobre se a troca do hidrogênio pelo deutério duas vezes mais pesado e maior criaria uma força de dispersão mais forte.
p Como uma regra geral, átomos maiores são mais polarizáveis e os pesquisadores obtiveram novos dados indicando que o aumento da polarizabilidade levou a forças de dispersão mais fortes. Contudo, em alguns casos, o hidrogênio menor realmente produz uma força de dispersão mais forte do que o deutério pesado, mas outros relatórios mostraram a diferença oposta ou insignificantemente pequena entre os dois átomos.
p "Em nossos experimentos, a diferença entropia-entalpia é completamente equilibrada. A energia livre liberada pelos nanocubos com hidrogênio ou deutério é essencialmente idêntica, então pode não haver diferença entre eles, "disse Hiraoka.
p Uma diferença essencial entre as pesquisas anteriores e esses experimentos é que a equipe UTokyo usou uma condição mais realista de estar em solução com água e ampliou o efeito usando o design de nanocubos.

