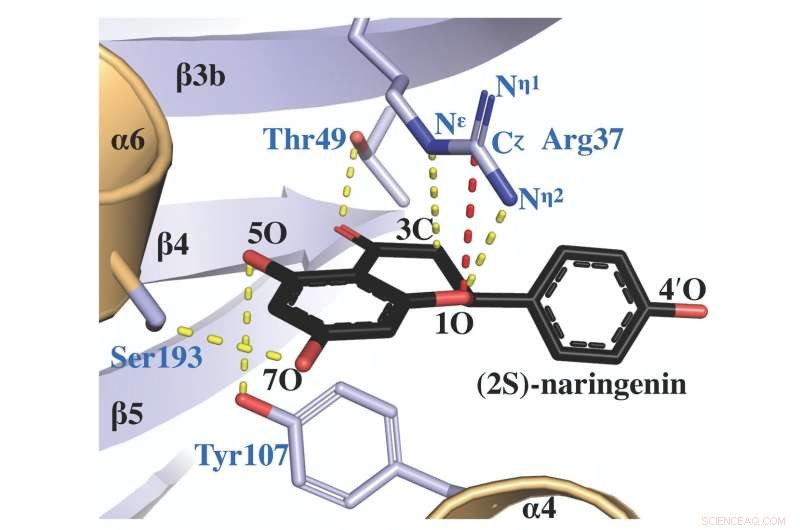
A estrutura cristalina da proteína de raios-X da chalcona isomerase, complexado com uma molécula de produto chamada (2S) -naringenina, revela como o sítio ativo arginina (rotulado como Arg 37) facilita a catálise do isômero correto. Crédito:Salk Institute / ACS Catalysis
As plantas podem fazer muitas coisas incríveis. Entre seus talentos, eles podem fabricar compostos que os ajudam a repelir pragas, atrair polinizadores, curar infecções e se proteger de temperaturas excessivas, seca e outros perigos no meio ambiente.
Pesquisadores do Instituto Salk que estudam como as plantas desenvolveram as habilidades de produzir esses produtos químicos naturais descobriram como uma enzima chamada isomerase de chalcona evoluiu para permitir que as plantas tornassem produtos vitais para sua própria sobrevivência. A esperança dos pesquisadores é que esse conhecimento informe a fabricação de produtos benéficos para os humanos, incluindo medicamentos e colheitas melhoradas. O estudo foi publicado na versão impressa do Catálise ACS em 6 de setembro, 2019.
"Desde que as plantas terrestres apareceram pela primeira vez na Terra há cerca de 450 milhões de anos, eles desenvolveram um sofisticado sistema metabólico para transformar o dióxido de carbono da atmosfera em uma miríade de produtos químicos naturais em suas raízes, brotos e sementes, "diz Salk Professor Joseph Noel, o autor sênior do artigo. "Este é o culminar do trabalho que temos feito em meu laboratório nos últimos 20 anos, tentando entender a evolução química das plantas. Ele nos dá conhecimento detalhado sobre como as plantas desenvolveram essa habilidade única de fazer algumas moléculas muito incomuns, mas importantes. "
Uma pesquisa anterior no laboratório de Noel analisou como essas enzimas evoluíram a partir de proteínas não enzimáticas, incluindo o estudo de versões mais primitivas deles que aparecem em organismos como bactérias e fungos.
Como uma enzima, A chalcona isomerase atua como um catalisador para acelerar as reações químicas nas plantas. Também ajuda a garantir que os produtos químicos produzidos na planta estejam na forma adequada, já que as moléculas com a mesma fórmula química podem ter duas variações diferentes que são imagens espelhadas uma da outra (chamadas de isômeros).

Salk Professor Joseph Noel, retratado em seu laboratório, próximo a uma máquina de espectroscopia de NMR, que é usado para decifrar os detalhes das estruturas eletrônicas das moléculas. Crédito:Salk Institute
“Na indústria farmacêutica, é importante que os medicamentos produzidos sejam da versão correta, ou isômero, porque usar o errado pode levar a efeitos colaterais indesejados, "diz Noel, que é diretor do Centro Jack H. Skirball de Salk para Biologia Química e Proteômica e detém a cadeira Arthur e Julie Woodrow. "Ao estudar como a chalcona isomerase funciona, podemos aprender mais sobre como acelerar a fabricação dos isômeros corretos de produtos farmacêuticos e outros produtos que podem ser importantes para a saúde humana. "
No estudo atual, os pesquisadores usaram várias técnicas de biologia estrutural para investigar a forma única da enzima e como sua forma muda à medida que interage com outras moléculas. Eles identificaram a parte da estrutura da isomerase de chalcona que permitiu que ela catalisasse reações incrivelmente rápidas, ao mesmo tempo que garantiam que ela era adequada, isômero biologicamente ativo. Essas reações levam a uma série de atividades nas plantas, incluindo a conversão de metabólitos primários como fenilalanina e tirosina em moléculas especializadas vitais chamadas flavonóides.
Descobriu-se que um determinado aminoácido, arginina, que foi um dos muitos aminoácidos ligados entre si na isomerase de chalcona em um local, moldado pela evolução, que lhe permitiu desempenhar um papel fundamental na forma como as reações da chalcona isomerase foram catalisadas.
"Fazendo estudos estruturais e modelagem computacional, pudemos ver as posições muito precisas da arginina dentro do sítio ativo da enzima à medida que a reação prosseguia, "diz o primeiro autor Jason Burke, um ex-pesquisador de pós-doutorado no laboratório de Noel que agora é professor assistente na California State University San Bernardino. "Sem aquela arginina, não funciona da mesma maneira. "
Burke acrescenta que esse tipo de catalisador é há muito procurado por químicos orgânicos. “Este é um exemplo da natureza já resolvendo um problema que os químicos vêm analisando há muito tempo, " ele adiciona.
"Ao compreender a chalcona isomerase, podemos criar um novo conjunto de ferramentas que os químicos poderão usar para as reações que estão estudando, "Noel diz." É absolutamente vital ter esse tipo de conhecimento básico para ser capaz de projetar sistemas moleculares que possam realizar uma tarefa específica, mesmo na próxima geração de plantações nutricionalmente densas, capazes de transformar o gás de efeito estufa dióxido de carbono em moléculas essenciais para vida."