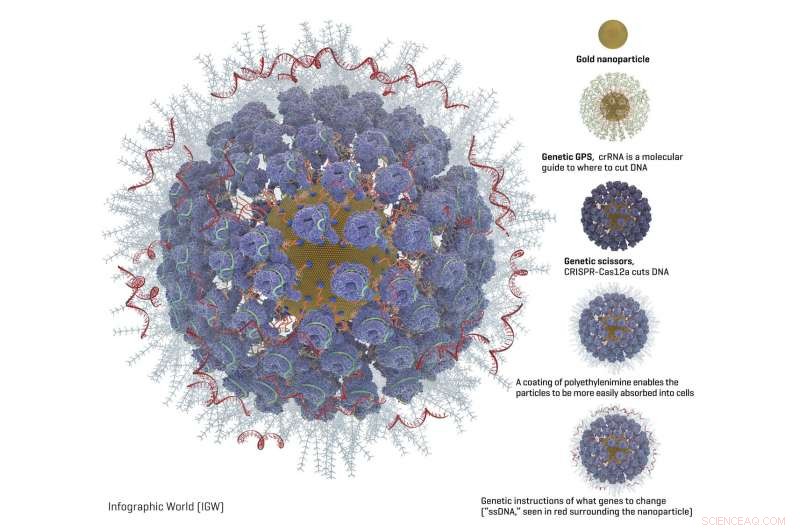
Gráfico de uma nanopartícula de ouro totalmente carregada com CRISPR e outras ferramentas de edição de genes. Crédito:o laboratório Adair em Fred Hutch.
Cientistas do Fred Hutchinson Cancer Research Center deram um passo para tornar a terapia genética mais prática, simplificando a maneira como as instruções de edição de genes são entregues às células. Usando uma nanopartícula de ouro em vez de um vírus inativado, eles entregaram com segurança ferramentas de edição de genes em modelos de laboratório de HIV e doenças hereditárias do sangue, conforme relatado em 27 de maio em Materiais da Natureza .
É a primeira vez que uma nanopartícula de ouro carregada com CRISPR foi usada para editar genes em um subconjunto raro, mas poderoso de células-tronco do sangue, a fonte de todas as células do sangue. A nanopartícula de ouro com CRISPR levou a uma edição de genes bem-sucedida em células-tronco do sangue, sem efeitos tóxicos.
"À medida que as terapias genéticas avançam nos ensaios clínicos e se tornam disponíveis para os pacientes, precisamos de uma abordagem mais prática, "disse a autora sênior Dra. Jennifer Adair, um membro assistente da Divisão de Pesquisa Clínica da Fred Hutch, acrescentando que os métodos atuais de realização de terapia genética são inacessíveis para milhões de pessoas em todo o mundo. "Eu queria encontrar algo mais simples, algo que entregaria passivamente a edição de genes às células-tronco do sangue. "
Embora o CRISPR tenha tornado mais rápido e fácil entregar com precisão modificações genéticas ao genoma, ainda tem desafios. Fazer com que as células aceitem as ferramentas de edição de genes CRISPR envolve um pequeno choque elétrico que pode danificar e até matar as células. E se forem necessárias edições genéticas precisas, então, moléculas adicionais devem ser projetadas para entregá-los - adicionando custo e tempo.
Nanopartículas de ouro são uma alternativa promissora porque a superfície dessas minúsculas esferas (cerca de 1 bilhão do tamanho de um grão de sal de cozinha) permite que outras moléculas se colem a elas facilmente e permaneçam aderidas.

Drs. Jen Adair (à esquerda) e Reza Shahbazi examinam um lote de teste de nanopartículas de ouro em seu laboratório em Fred Hutch. A solução é vermelha porque quando os íons de ouro se agrupam para formar nanopartículas, elétrons na superfície começam a oscilar e refletir a luz em diferentes comprimentos de onda. Então, quando a luz atinge as partículas de ouro, elétrons refletem a luz de maneira diferente. Crédito:Robert Hood, Fred Hutch
"Projetamos as nanopartículas de ouro para cruzar rapidamente a membrana celular, esquivar das organelas celulares que procuram destruí-las e ir direto ao núcleo da célula para editar genes, "disse o Dr. Reza Shahbazi, Fred Hutch, pesquisador de pós-doutorado, que trabalhou com nanopartículas de ouro para entrega de drogas e genes por sete anos.
Shahbazi fez as partículas de ouro com ouro de laboratório que é purificado e vem como um líquido em uma pequena garrafa de laboratório. Ele misturou o ouro purificado em uma solução que faz com que os íons de ouro individuais formem partículas minúsculas, que os pesquisadores então mediram quanto ao tamanho. Eles descobriram que um determinado tamanho - 19 nanômetros de largura - era o melhor por ser grande e pegajoso o suficiente para adicionar materiais de edição de genes à superfície das partículas, embora ainda seja pequeno o suficiente para as células absorvê-los.
Empacotado nas partículas de ouro, a equipe de Fred Hutch adicionou estes componentes de edição de genes (diagrama disponível):
Em seguida, os pesquisadores isolaram células-tronco do sangue com um marcador de proteína em sua superfície chamado CD34. Essas células positivas para CD34 contêm as células progenitoras produtoras de sangue que dão origem a todo o sangue e ao sistema imunológico.

À medida que os íons de ouro se aglomeram para formar nanopartículas, os elétrons em sua superfície refletem a luz em um comprimento de onda diferente - daí a tonalidade vermelha. O tubo de laboratório em primeiro plano contém íons de ouro antes de formarem nanopartículas e carregados com ferramentas de edição de genes. Crédito:Robert Hood, Fred Hutch
"Essas células reabastecem o sangue do corpo todos os dias, tornando-os um bom candidato para terapia genética única, porque durará toda a vida enquanto as células se substituem, "Adair disse.
Observando células-tronco de sangue humano em uma placa de laboratório, os pesquisadores descobriram que suas nanopartículas de ouro totalmente carregadas foram absorvidas naturalmente pelas células dentro de seis horas após serem adicionadas e dentro de 24 a 48 horas eles puderam ver a edição de genes acontecendo. Eles observaram que o parceiro de proteína Cas12a CRISPR era melhor em entregar edições genéticas muito precisas às células do que o parceiro de proteína cas9 mais comumente usado.
O efeito de edição de genes atingiu um pico oito semanas depois que os pesquisadores injetaram as células em modelos de camundongos; 22 semanas após a injeção, as células editadas ainda estavam lá. Os pesquisadores de Fred Hutch também encontraram células editadas na medula óssea, baço e timo dos modelos de camundongos, um sinal de que as células sanguíneas em divisão nesses órgãos poderiam continuar o tratamento sem que os camundongos precisassem ser tratados novamente.
"Acreditamos ter um bom candidato para duas doenças - HIV e hemoglobinopatias - embora também estejamos avaliando outros alvos de doenças onde pequenas mudanças genéticas podem ter um grande impacto, bem como maneiras de fazer mudanças genéticas maiores, "Adair disse." O próximo passo é aumentar a quantidade de edição de genes que acontece em cada célula, o que é definitivamente factível. Isso o tornará mais perto de ser uma terapia eficaz. "
No estudo, os pesquisadores relatam que 10 a 20 por cento das células assumiram as edições de genes, que é um começo promissor, mas os pesquisadores gostariam de ter 50% ou mais das células sendo editadas, que eles acreditam ter uma boa chance de combater essas doenças.