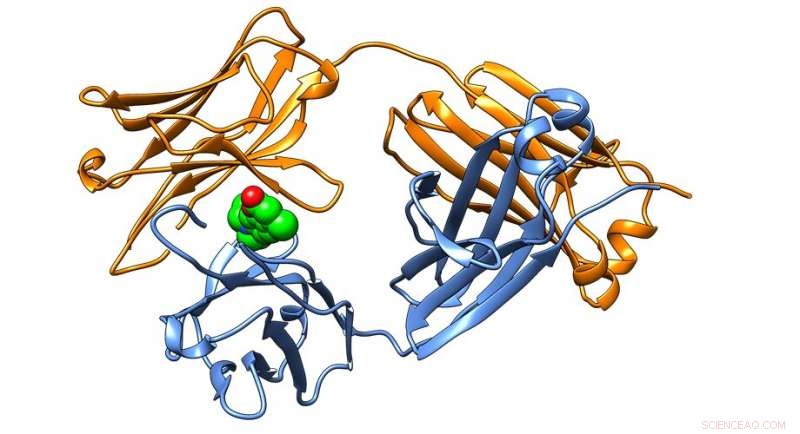
Estrutura cristalina de uma proteína de anticorpo encontrada em amiloidoses de cadeia leve, estabilizado com sucesso por pequenas moléculas identificadas no Kelly Lab. Crédito:The Scripps Research Institute
Cientistas da Scripps Research identificaram um grupo de pequenas moléculas que evitam mudanças estruturais nas proteínas que estão na origem da amiloidose AL, uma doença progressiva e freqüentemente fatal.
As pequenas moléculas se ligam a proteínas de imunoglobulina, que desempenham um papel essencial no sistema imunológico do corpo, e, em seguida, estabilizar as subunidades da proteína denominada cadeias leves de imunoglobulina. A ligação e a estabilização das cadeias leves em sua forma nativa evita que elas se dobrem incorretamente e formem as placas tóxicas encontradas em pacientes com amiloidose AL.
Ao rotular cadeias leves com fluoróforos e acoplar mudanças de forma para clivagem por proteinase K, quase um milhão de pequenas moléculas foram examinadas quanto à sua capacidade de prevenir as mudanças estruturais associadas à doença usando a polarização de fluorescência. Usando essa estratégia como base para uma tela de alto rendimento e várias contra-telas distintas para eliminar artefatos, a equipe descobriu vários candidatos a drogas de pequenas moléculas que impediam que as cadeias leves de imunoglobulina se dobrassem e se agregassem em um tubo de ensaio. A abordagem, se bem sucedido em humanos, pode mudar o curso da doença.
"Porque identificamos o local de ligação da pequena molécula de cadeia leve de imunoglobulina que confere estabilização por cristalografia, acreditamos que essas descobertas representam um modelo para a produção de um medicamento muito necessário para a amiloidose AL, "diz o professor de química da Scripps Research Jeffery Kelly, Ph.D., quem liderou a pesquisa. "Se pudermos bloquear a agregação de cadeias leves recentemente secretadas e evitar que sejam degradadas em fragmentos propensos à agregação, esperamos desacelerar ou mesmo interromper a progressão da doença, especialmente para os pacientes que apresentam envolvimento cardíaco. "
A amiloidose é uma doença rara e provavelmente subdiagnosticada que assume várias formas. AL amiloidose, também chamada de amiloidose de cadeia leve, é a segunda doença amilóide sistêmica mais comum, com cerca de 4, 500 novos casos todos os anos nos EUA
As células plasmáticas de pessoas com amiloidose AL produzem um componente de anticorpos conhecido como cadeias leves de imunoglobulina, frequentemente em vez de anticorpos, como resultado de um câncer de células plasmáticas. As cadeias leves dobram-se incorretamente e / ou aglomeram-se em pequenas fibras que são tóxicas para os órgãos. Hora extra, esses chamados depósitos de amiloide interferem progressivamente na função saudável do coração, rins, fígado e outras partes do corpo.
Gareth Morgan da Scripps Research, Ph.D., autor principal do estudo, enfatiza que os pacientes com AL com envolvimento de órgãos, particularmente envolvimento cardíaco, geralmente estão muito doentes para tolerar a quimioterapia. A esperança é que os estabilizadores cinéticos da cadeia leve da imunoglobulina sejam capazes de servir como um primeiro tratamento para esses pacientes, para que possam, em última instância, tolerar a quimioterapia.
As descobertas da equipe de pesquisa Scripps aparecem no Proceedings of the National Academy of Sciences . Além de descrever sua abordagem de estabilização cinética para o tratamento da amiloidose AL, os pesquisadores dizem que imaginam um método direto para identificar os pacientes que teriam maior probabilidade de se beneficiar com o tratamento.
Kelly diz que o mecanismo do medicamento que a equipe identificou é análogo a um medicamento diferente que também se originou na Scripps Research:Tafamidis, que estabiliza a proteína transtirretina para tratar a doença amilóide sistêmica mais comum que afeta o coração ou outros órgãos. Kelly inventou tafamidis junto com Evan Powers, Ph.D., para tratar amiloidoses transtirretina. Agora propriedade da Pfizer, tafamidis é aprovado na Europa sob o nome de Vyndaqel e foi recentemente submetido ao FDA para aprovação nos EUA.
Nicholas Yan, um estudante de pós-graduação e co-primeiro autor do estudo, está agora desenvolvendo estabilizadores cinéticos de cadeia leve de imunoglobulina mais potentes e seletivos com propriedades semelhantes a drogas para serem usados em humanos, estudos sendo realizados em colaboração com Reji Nair, Ph.D., um pós-doutorado, também em colaboração com outros da Scripps Research.