
Pulverizar sal nas estradas é uma medida de segurança. Crédito:stoatphoto / Shutterstock.com
Brrr… está frio lá fora! As crianças estão correndo para a televisão na esperança de ouvir que haverá um dia de neve; os corredores de pão e leite nos supermercados estão vazios por causa de uma tempestade de neve iminente; e caminhões utilitários estão espalhando água salgada ou salgada nas estradas.
Todos nós sabemos por que os dois primeiros acontecem - as crianças estão animadas para um dia de folga na escola repleto de chocolate quente e bonecos de neve. Os adultos estão estocando o necessário. Mas o que há com esses caminhões?
Eles estão trabalhando para proteger os motoristas de condições escorregadias, pulverizando sal-gema ou uma solução de água salgada para evitar a formação de gelo. Este sal é muito semelhante ao sal que você tem em sua mesa de jantar - é o mesmo cloreto de sódio, NaCl. Existem algumas misturas patenteadas que contêm outros sais - como cloreto de potássio (KCl) e cloreto de magnésio (MgCl) - mas não são tão comumente usados.
O sal rodoviário não é tão puro quanto o que você usa na comida; tem uma cor cinza acastanhada, principalmente devido à contaminação mineral. Submeter o meio ambiente a este sal por meio do escoamento pode ter algumas consequências indesejadas, incluindo efeitos negativos nas plantas, animais aquáticos e zonas húmidas.
Mas é uma maneira barata e eficaz de proteger as estradas do gelo devido a um princípio científico simples:depressão do ponto de congelamento das soluções. O ponto de congelamento da água pura, a temperatura na qual se torna gelo, é de 32 graus Fahrenheit. Então, se houver neve, granizo ou chuva congelante e o solo está a 32 F ou mais frio, gelo sólido se formará nas ruas e calçadas.
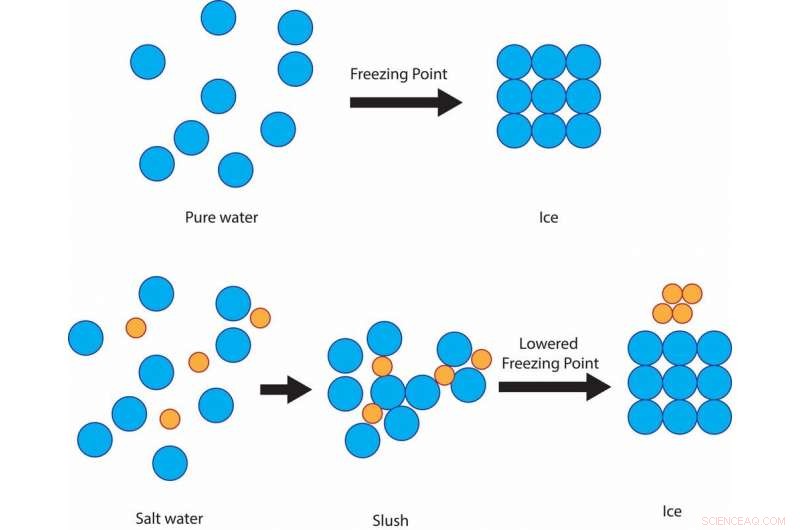
O sal impede que as moléculas de água se solidifiquem em cristais de gelo a 32 F, em vez de ficar lamacento nessa temperatura, antes de congelar por volta de 15 F. Crédito:Julie Pollock, CC BY-ND
Se a água for misturada com sal, no entanto, a temperatura de congelamento da solução é inferior a 32 F. O sal impede a capacidade das moléculas de água de formarem cristais de gelo sólidos. O grau de depressão do ponto de congelamento depende de quão salgada é a solução.
É importante ressaltar que o sal deve estar em solução com água em estado líquido para que este princípio seja obedecido. É por isso que muitas cidades borrifam uma solução de sal antes de qualquer formação de gelo.
O sal que é despejado em cima do gelo depende do sol ou da fricção dos pneus do carro que passam sobre ele para derreter inicialmente o gelo em uma lama que pode se misturar com o sal e não voltar a congelar. O pré-tratamento com sal sólido depende da superfície da estrada mais quente para derreter inicialmente qualquer neve ou chuva congelante para que possa se misturar adequadamente com o sal. É também por isso que o pré-tratamento de pontes - que são mais frias do que outras estradas - normalmente não funciona, e por que você vê os sinais de "ponte congela antes da estrada".
Essas soluções de sal diminuem a temperatura de congelamento da água para cerca de 15 F. Assim, infelizmente para pessoas que enfrentam temps verdadeiramente frias, o tratamento com sal não elimina o gelo das estradas.
Uma estratégia alternativa usada nessas temperaturas mais baixas é colocar areia no gelo. A areia não muda a temperatura de derretimento, ele apenas fornece uma superfície áspera para os pneus evitarem escorregões e deslizamentos.
A ciência da depressão do ponto de congelamento pode ser aplicada a qualquer solução, e muitos grupos de pesquisa têm se concentrado no desenvolvimento de alternativas com menos consequências ambientais negativas. Eles incluem aditivos como melaço e suco de beterraba. Então, talvez você possa limpar não apenas o sal branco da parte inferior de seu jeans após uma caminhada no inverno, mas sal rosa também.
Este artigo foi republicado de The Conversation sob uma licença Creative Commons. Leia o artigo original. 