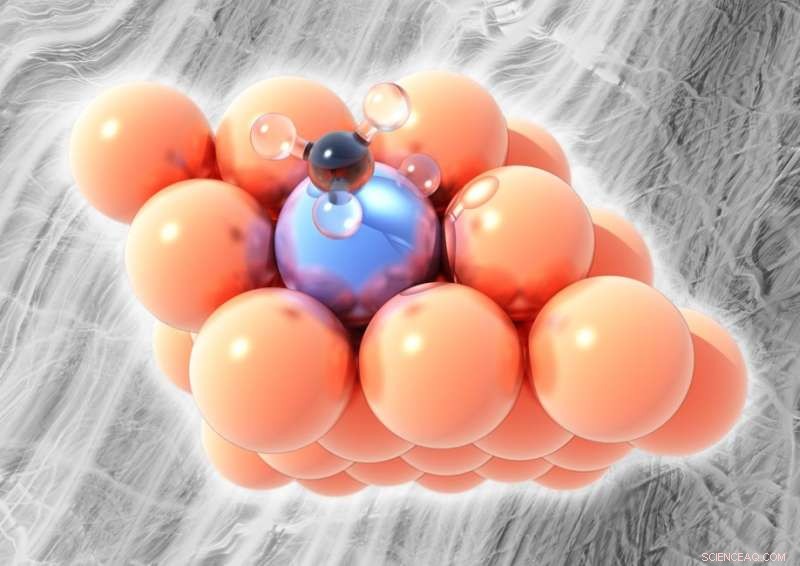
 p Na foto, a liga de átomo único de platina-cobre. O cobre (laranja) é incapaz de quebrar as ligações entre o carbono (preto) e o hidrogênio (transparente) em derivados de metano, exceto em temperaturas mais altas, mas um único átomo de platina (azul gelo) na camada superficial da liga pode quebrar os átomos de hidrogênio em temperaturas relativamente baixas sem formar coque. Crédito:Michail Stamatakis, UCL
p Na foto, a liga de átomo único de platina-cobre. O cobre (laranja) é incapaz de quebrar as ligações entre o carbono (preto) e o hidrogênio (transparente) em derivados de metano, exceto em temperaturas mais altas, mas um único átomo de platina (azul gelo) na camada superficial da liga pode quebrar os átomos de hidrogênio em temperaturas relativamente baixas sem formar coque. Crédito:Michail Stamatakis, UCL
p Os avanços tecnológicos na estimulação de poços de petróleo e gás na última década agora permitem a produção de gás natural a partir do gás de xisto aprisionado em formações rochosas subterrâneas. Com o aumento repentino da disponibilidade de gás de xisto, os cientistas recuperaram o interesse na ativação de carbono-hidrogênio (C – H), o processo de quebrar ligações C – H de gases como o metano para formar cadeias de hidrocarbonetos que podem ser usados como combustível. p Mas os cientistas estão muito longe de coletar esses combustíveis do gás de xisto - a maioria dos catalisadores para a ativação de C – H quebram muitos átomos de hidrogênio, deixando para trás um sólido de carbono indesejado chamado coque.
p Desejando uma liga de metal que funcionasse como um catalisador para a ativação de C – H, embora permanecesse resistente ao coque, uma equipe liderada por Charles Sykes na Tufts University concebeu uma liga feita de platina de metal reativo e cobre de metal inerte. Em uma série de experimentos de laboratório, A equipe de Sykes analisou cobre puro, platina pura, e uma liga de átomo único de platina-cobre (SAA) para determinar as interações de cada material com hidrocarbonetos derivados de metano, moléculas que são encontradas naturalmente no gás de xisto. A equipe descobriu que o SAA platina-cobre era resistente à coqueificação.
p Após esta descoberta, o grupo Multiscale Computational Catalysis &Materials Science liderado por Michail Stamatakis na University College London usou os recursos de computação de alto desempenho (HPC) no Oak Ridge Leadership Computing Facility (OLCF) para desmascarar detalhes dos experimentos por meio de simulações. Matthew Darby, com pós-doutorado na época e agora recebedor do prêmio de doutorado do Conselho de Pesquisa em Engenharia e Ciências Físicas do Reino Unido trabalhando no grupo Stamatakis, realizou os cálculos para o projeto.
p Darby descobriu que em baixas temperaturas, a platina retira rapidamente os hidrogênios do metano, levando à formação de depósitos de carbono; o cobre é incapaz de quebrar as ligações C – H, exceto em altas temperaturas. A liga de platina-cobre da equipe, Contudo, foi encontrado para quebrar com eficiência ligações C – H em temperaturas intermediárias sem formar coque. Como cobre puro, a liga também foi capaz de formar cadeias de metano de duas e três moléculas - e poderia conseguir isso a uma temperatura mais de 100 graus Celsius mais fria do que o necessário para o cobre.
p "Esses cálculos são muito caros do ponto de vista computacional. Para alguns, se você os executou em seu laptop, pode levar vários meses para executar um cálculo, "Darby disse." No OLCF, pode demorar um ou dois dias porque você tem centenas de núcleos para trabalhar. "
p Supercomputadores poderosos no OLCF, um Centro de Usuários do Escritório de Ciências do Departamento de Energia dos EUA (DOE) localizado no Laboratório Nacional de Oak Ridge do DOE, resolver problemas científicos complexos em energia, materiais, química, e muitos outros domínios científicos. Os resultados das simulações da equipe explicam as reações da platina e do cobre com o metano e oferecem um novo catalisador resistente ao coque.
p Armado com este novo conhecimento, os experimentalistas da Tufts criaram uma réplica em micronível do desempenho de uma fábrica química real para obter ainda mais insights sobre o processo. O projeto demonstra que a teoria pode ser usada para refinar experimentos, fornecendo uma compreensão fundamental, preparando o terreno para um trabalho experimental em larga escala.
p
Um problema de coque
p Combustíveis comuns que existem como cadeias de moléculas de hidrocarbonetos incluem propano, frequentemente usado em fornos para aquecimento, e butano, o líquido encontrado na maioria dos isqueiros. Usando a ativação C – H, os cientistas podem iniciar reações dentro do hidrocarboneto mais simples - metano - e, assim, encorajar essas moléculas a se unirem para formar combustíveis úteis. Porque as formações de xisto são abundantes e fontes de hidrocarbonetos mais longos (por exemplo, petróleo bruto) estão acabando, os cientistas estão procurando maneiras de converter cataliticamente o metano nesses combustíveis.
p Metais de transição, como platina e níquel, são catalisadores eficazes, mas também causam a formação de grandes quantidades de depósitos obstrutivos de coque. Esta camada de carbono reveste a parte superior do metal, tornando as moléculas de metano restantes incapazes de reagir com o resto do material metálico.
p "A coca é um grande problema na química industrial, "Darby disse." Assim que for depositado, você tem que tirar o seu metal do reator, limpe-o, e colocá-lo de volta. Isso envolve fechar a gigantesca fábrica de produtos químicos ou aquecer o metal a temperaturas perigosamente altas. "
p Contraintuitivo para sua capacidade de separar rapidamente os hidrogênios do metano, a platina e o níquel são limitados na produção de hidrocarbonetos de cadeia mais longa por causa da coqueificação. Recentemente, os cientistas procuraram ligas feitas de um metal ativo, como platina ou níquel, e um metal inerte, como cobre ou prata. Mas mesmo com esses tipos de ligas, a coqueificação continua a ser um problema.
p A equipe de Sykes desenvolveu um novo SAA, ou liga de átomo único, com apenas 1 átomo de platina para cada 100 átomos de cobre, para combater a coqueificação. Os átomos de platina foram isolados na camada superficial do metal para garantir que não reagissem abertamente. Os experimentos mostraram que átomos de platina únicos no cobre ainda reagem para quebrar as ligações C – H, mas não na medida em que o coque é formado.
p Darby então simulou platina pura, cobre puro, e o SAA para determinar a qual das três superfícies um átomo de carbono se liga mais fortemente. Ele repetiu este processo com carbono ligado a um, dois, três, e quatro hidrogênios, bem como átomos de hidrogênio por conta própria. Ele descobriu que essas moléculas se ligam ao cobre com maior afinidade do que à platina, e muito mais energia é necessária para o cobre quebrar as ligações C – H. Os resultados são essenciais para explicar por que o cobre é um catalisador ineficaz.
p "A platina pode quebrar as ligações C – H milhões de vezes mais rápido do que o cobre, e a liga está em algum lugar no meio, "Darby disse." Antes deste SAA, as pessoas não conseguiam ligar duas ou três moléculas de metano a baixas temperaturas sem desativar o metal. Mostramos que podemos obter até três. "
p A descoberta é importante porque nunca houve uma liga que pudesse quebrar efetivamente as ligações C – H e também permanecer resistente ao coque.
p "Nosso SAA demonstra que uma solução para este problema poderia ser possível, "Darby disse." Espero que isso ajude a estimular a comunidade química a tentar mais combinações de SAA e ver se podemos realmente encontrar a liga que será perfeita para isso. "
p
Partículas do tamanho de átomo
p As simulações foram realizadas em recursos OLCF usando o Vienna ab initio Simulation Package (VASP), um código projetado para modelar materiais em escala atômica. O VASP é o mais popular de seu tipo e é perfeitamente adaptado para uso em computadores paralelos de alto desempenho, como os do OLCF.
p "Modelamos as coisas em um nível de átomo, "Darby disse." Nós modelamos 100 partículas do tamanho de um átomo:o catalisador e as moléculas de metano. Em seguida, calculamos quanta energia é necessária para converter o metano em outra coisa. "
p Ao comparar esses cálculos entre si, Darby foi capaz de explicar as descobertas experimentais. Ao reproduzir tudo no experimento, a equipe poderia ver até o nível do átomo e simular o número de vezes que ligações específicas se quebrariam - algo que é impossível contar em um experimento.
p A esperança da equipe é que um dia uma liga seja capaz de ligar até oito metanos (o composto de octanagem), que pode então ser usado para abastecer carros. Os resultados do projeto e o trabalho contínuo do grupo Stamatakis permitirão que os experimentalistas se concentrem nos sistemas de ligas mais importantes, em vez de testar sistemas aleatórios.
p "Com a experiência, é principalmente tentativa e erro, "Darby disse." Simulações nos dão um roteiro. "
