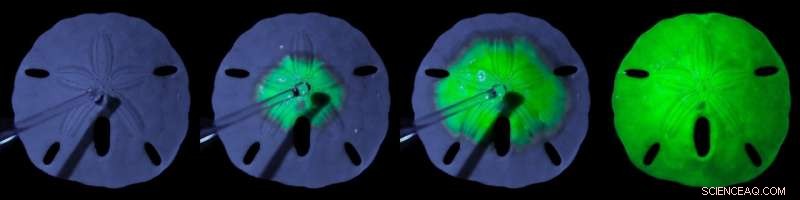
Esta série de fotos mostra um esqueleto de dólar de areia convertendo-se gradualmente em uma perovskita emissora de luz. Os instantâneos dessa conversão são obtidos em 0s, 5s, 15s, e 40 anos. Crédito:Noorduin Lab, AMOLF
Pesquisadores da AMOLF descobriram uma maneira de fazer estruturas de carbonato de cálcio adequadas para uso em eletrônica. Eles fazem isso modificando a composição do material para que se torne um semicondutor sem perder sua forma. Isso pode levar a células solares mais eficientes e estáveis. Esta pesquisa foi publicada na revista Química da Natureza em 4 de junho, 2018.
Em princípio, seria possível realizar o experimento na praia usando a concha oval branca de um choco ou o esqueleto de um ouriço-do-mar, disse Wim Noorduin, líder do grupo Self Organizing Matter no AMOLF. "O experimento envolve não mais do que pingar dois líquidos sobre a estrutura de carbonato de cálcio. A conversão é concluída em alguns minutos. Se você acender uma lâmpada UV na estrutura, você pode ver a conversão ocorrendo diante de seus olhos:O esqueleto do ouriço-do-mar, que inicialmente parece azul sob a lâmpada, muda para uma estrutura verde brilhante com cada gota. "
Noorduin converte estruturas de carbonato de cálcio, como o esqueleto de um ouriço-do-mar, em perovskita, um novo material altamente promissor para células solares. "Na verdade, isso é alquimia, "diz Noorduin." Midas transformou tudo em ouro, e agora estamos transformando o carbonato de cálcio em perovskita. "
O carbonato de cálcio é altamente abundante na Terra, e podem ser encontrados em minas de giz e esqueletos de animais, por exemplo. Noorduin já havia encontrado uma maneira de fazer uma variedade de microestruturas de cálcio para entender como a natureza o faz. Mas o material tem poucas aplicações. Perovskita, Contudo, oferece mais possibilidades, e é um novo material altamente promissor para células solares. As células solares produzidas a partir do semicondutor perovskita são mais eficientes e mais baratas do que as células solares de silício tradicionais. Eles também são objeto de pesquisas cada vez maiores. "Ao converter uma estrutura predeterminada de carbonato de cálcio na perovskita funcional, agora temos controle sobre a forma e função do material, "diz Noorduin.
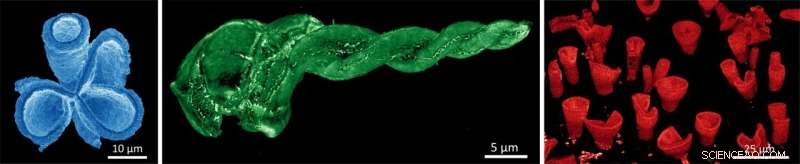
Microestruturas semicondutoras 3D:ao escolher a composição específica do íon durante a reação de conversão, podemos ajustar a cor em todo o espectro visível do azul ao verde ao vermelho. O coral azul é cloreto de chumbo metil amônio, a espiral verde é brometo de metil amônio de chumbo e os vasos vermelhos são iodeto de metil amônio de chumbo. As imagens são tiradas com um microscópio eletrônico modificado que coleta luz, esta técnica é chamada de catodoluminescência (CL). Crédito:Noorduin Lab, AMOLF
Noorduin espera que o novo material leve a células solares aprimoradas. Como os pesquisadores agora têm controle sobre a forma da célula solar, eles podem produzir uma estrutura que captura a luz do sol com mais eficácia. Além disso, a vida útil da atual geração de células solares feitas de perovskita é muito curta, pois a perovskita se degrada muito rapidamente. "Achamos que nossas microestruturas de perovskita são muito mais estáveis. As células solares feitas desse material devem, portanto, durar mais, "diz Noorduin." Além disso, podemos produzir estruturas perovskita em todas as cores desejadas. Isso significa que o material também pode ser usado para LEDs em várias aplicações, como telas, "diz a pesquisadora.
Com o novo processo, desenvolvido por Noorduin's Ph.D. pesquisadores Lukas Helmbrecht e Hans Hendrikse, é possível converter todas as estruturas de carbonato de cálcio, como o esqueleto de um ouriço-do-mar ou as microestruturas de Noorduin, em perovskite. Este processo diz respeito à conversão controlada de uma estrutura cristalina em outra, que é um processo difícil em química. Uma estrutura de cristal é semelhante a uma coleção de bolas de gude empilhadas. Os íons no carbonato de cálcio são diferentes daqueles na perovskita, e o empilhamento também é diferente. Os pesquisadores substituem todos os íons no carbonato de cálcio - primeiro, os íons de cálcio carregados positivamente com ferros de chumbo, e então os ferros de carbonato carregados negativamente com cloreto, por exemplo. Finalmente, eles adicionam outro íon, metil amônio. Este último ingrediente dá origem a um novo padrão de empilhamento como resultado do qual a perovskita é produzida.
O experimento é simples, uma vez que você sabe como fazê-lo, diz Noorduin. A dificuldade de converter carbonato de cálcio em perovskita é que tudo é diferente:não apenas a composição de cátions carregados positivamente e ânions carregados negativamente, mas também a estrutura cristalina, diz Noorduin. "As condições de reação, como concentração e nível de pH, deve estar exatamente certo, caso contrário, a estrutura se desfaz imediatamente. Levamos seis meses para descobrir essas condições exatas. "
Por exemplo, a troca dos cátions na primeira etapa deve ser perfeita. A segunda etapa é ainda mais difícil porque a estrutura do cristal deve mudar. Também descobrimos que era vital garantir que essa última etapa ocorresse muito rapidamente para evitar que a estrutura se desintegrasse.
Outros materiais
O método de troca iônica pode ser usado em uma ampla variedade de materiais. Não apenas carbonato de cálcio, mas também carbonato de bário e carbonato de estrôncio são adequados, e possivelmente sulfatos também. Os pesquisadores do AMOLF esperam que a reação também possa ser expandida para outros tipos de perovskita para possibilitar uma ampla gama de aplicações. "We can apply the principles to other materials such as catalysts. In those cases, you want to be able to control the material's surface shape and composition as well."