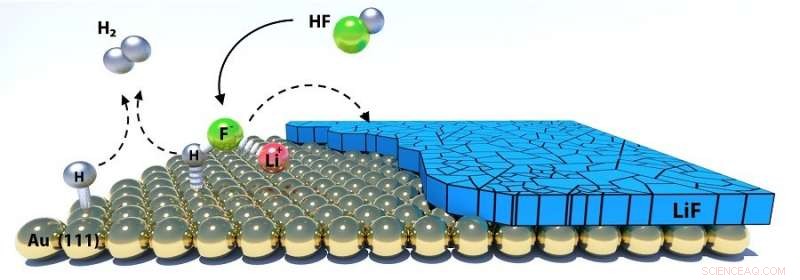
O mecanismo de reação para converter a impureza de fluoreto de hidrogênio (HF) do eletrólito em fluoreto de lítio (LiF) na interfase de eletrólito sólido (SEI) com liberação de gás hidrogênio (H2). A camada SEI é mostrada em um substrato de átomos de ouro (Au), que serve como um sistema de modelo simplificado. Os cientistas determinaram esse mecanismo usando métodos computacionais avançados (teoria do funcional da densidade e simulações de dinâmica molecular). Crédito:Laboratório Nacional de Argonne
Disponível comercialmente desde 1970, a bateria de íon de lítio é agora a fonte de alimentação robusta em muitas aplicações. Ele pode ser encontrado em telefones celulares, laptops e veículos elétricos. Ainda, muito sobre a ciência básica que ocorre nos níveis atômico e molecular durante a carga e descarga permanece um mistério.
Em um novo estudo publicado em Catálise Natural , uma equipe do Laboratório Nacional de Argonne do Departamento de Energia dos EUA (DOE) relata um avanço na compreensão da química da camada microscopicamente fina que se forma na interface entre o eletrólito líquido e o eletrodo sólido. Os pesquisadores da bateria comumente se referem a essa camada como "interfase de eletrólito sólido" ou SEI.
Muito trabalho científico nas últimas décadas foi dedicado a compreender o SEI na bateria de íon de lítio. Os cientistas sabem que o SEI se forma no eletrodo negativo de grafite, é extremamente fino (menos de um milésimo de milímetro), e toma forma principalmente durante a primeira carga da bateria. Também está bem estabelecido que o SEI evita que reações prejudiciais ocorram na interface, enquanto, ao mesmo tempo, permite que os íons de lítio importantes rédea livre se movam entre o eletrólito e o eletrodo.
Todas as baterias de íon de lítio boas têm SEIs funcionando bem. Como Dusan Strmcnik - co-investigador principal e engenheiro químico assistente na divisão de Ciência de Materiais (MSD) - observou, "O desempenho da bateria é altamente dependente da qualidade do SEI. Se a química e o papel dos componentes individuais do SEI forem compreendidos, o SEI pode ser ajustado para melhorar o desempenho da bateria. "
"Mais importante, tal compreensão melhoraria significativamente nossa capacidade de previsão da vida útil da bateria, que é de valor extremamente alto para um fabricante de carros elétricos, "Strmcnik acrescentou.
A equipe internacional de pesquisadores, que inclui colaboradores da Universidade de Copenhagen, a Technische Universität München na Alemanha e o BMW Group, decifrou a química por trás de um dos componentes mais comuns do SEI em baterias de íon de lítio típicas, fluoreto de lítio. Com base em resultados experimentais e computacionais, suas descobertas mostraram que esta fase se forma durante a carga da bateria pela reação eletroquímica do fluoreto de hidrogênio, produzindo gás hidrogênio e fluoreto de lítio sólido.
Esta reação depende muito do material do eletrodo, que poderia ser um metal, grafeno ou material grafítico, e assim demonstra a importância da catálise na operação da bateria. A equipe descobriu um novo método para monitorar a concentração de fluoreto de hidrogênio, uma impureza altamente prejudicial que se forma a partir de uma reação entre traços de umidade e o sal (LiPF6) no eletrólito. Essa capacidade de monitoramento deve ser vital para futuros estudos científicos básicos do SEI.
Para Argonne Distinguished Fellow e co-investigador principal Nenad Markovic, os resultados do estudo já estão tendo impacto comercial. "Nossas descobertas já estão sendo implementadas em células de íon-lítio no Centro de Competência de Células de Bateria do BMW Group. Elas também abrirão novas oportunidades para a melhoria dos sistemas existentes, e o design de novos, tecnologias de íon-lítio. "
o Catálise Natural o artigo é intitulado "Transformação eletrocatalítica de impureza HF em H2 e LiF em baterias de íon-lítio."