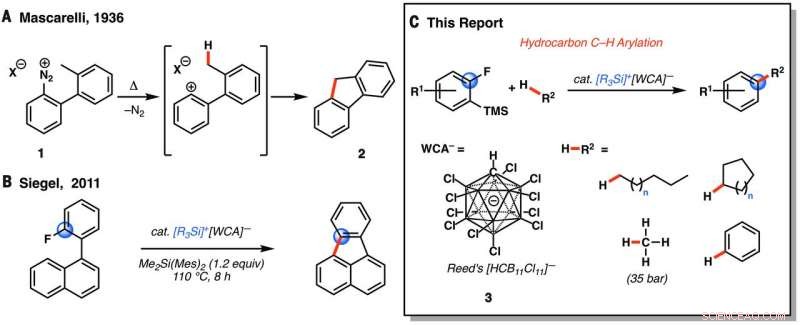
Reações envolvendo putativos fenil cátions. (A) reação de Mascarelli (12). (B) Reação intramolecular de Friedel-Crafts de Siegel de fluoretos de arila (15). (C) Nossa estratégia de funcionalização dual C – F / C – H. R =etilo ou triisopropilo; R1 =aril, alquil, haleto, ou éter silílico; WCA, ânion de coordenação fraca; TMS, trimetilsililo; Mes, mesitilo; Mim, metilo; gato., catalítico. Crédito:(c) Ciência (2017). DOI:10.1126 / science.aam7975
(Phys.org) —Uma equipe de químicos da Universidade da Califórnia desenvolveu uma maneira mais barata de funcionalizar alcanos não ativados (hidrocarbonetos como o etano, metano e propano) usando catalisadores muito mais abundantes. Em seu artigo publicado na revista Ciência , a equipe descreve o projeto de reação que eles criaram que supera desafios anteriores relacionados a perfis de reatividade de alta energia.
Atualmente, alcanos não ativados são considerados difíceis de funcionalizar - a maioria usa uma abordagem que envolve a abertura de ligações C-H de hidrocarbonetos usando um processo que envolve metais preciosos e caros. Neste novo esforço, a equipe encontrou uma maneira de usar silício e boro como catalisadores. Isso é importante porque a indústria precisa converter alcanos, como gás natural e petróleo, em produtos mais valiosos.
Alcanos reagem com relativa facilidade em altas temperaturas, como é visto em motores de combustão interna, mas tais reações são consideradas extremamente difíceis de controlar. A funcionalização de alcanos permite obter mais deles do que apenas seu potencial de energia, permite extrair componentes que podem ser usados como precursores para a criação de produtos químicos raros que, em alguns casos, são consideravelmente mais valiosos. Porque eles são relativamente inertes, e as ligações entre o carbono e o hidrogênio são fortes, eles são difíceis de funcionalizar. Para quebrar esses laços fortes, a equipe fez ainda mais fortes.
O grupo começou com anéis de benzeno, prepará-los com substitutos de silício e flúor. Em seguida, eles iniciaram um ciclo usando silício ativado adicional, que eles emparelharam com o carborano - isso forçou o flúor a criar um intermediário aril que foi capaz de quebrar as ligações do alcano C-H (que incluía principalmente o metano). O anel resultante então liberou silício, o que manteve a reação em andamento. A equipe observa que a reação pode ser conduzida em faixas de temperatura de 30 ° a 100 ° C. Ainda não está claro se o processo pode ser dimensionado para ser econômico, mas se assim for, pode levar a uma queda nos preços de alguns produtos, particularmente aqueles baseados em gás natural cada vez mais abundante.
O grupo está programado para fazer uma apresentação sobre seu trabalho na próxima reunião da ACS.
© 2017 Phys.org