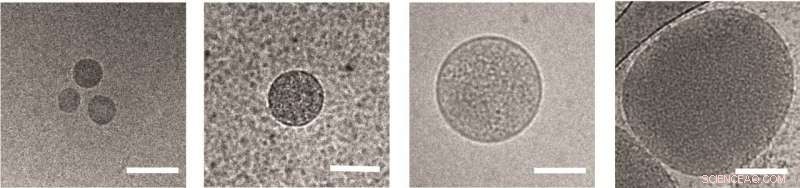
 p Nanovesículas liberadas de glóbulos vermelhos infectados por Plasmodium falciparum , visto sob um microscópio eletrônico. Barra de escala:100 nm Crédito:Weizmann Institute of Science
p Nanovesículas liberadas de glóbulos vermelhos infectados por Plasmodium falciparum , visto sob um microscópio eletrônico. Barra de escala:100 nm Crédito:Weizmann Institute of Science
p Os esforços globais para erradicar a malária dependem crucialmente da capacidade dos cientistas de superar o parasita da malária. E
Plasmodium falciparum é notoriamente inteligente:é rápido para desenvolver resistência contra medicamentos e tem um ciclo de vida tão complexo que bloqueá-lo de forma eficaz com uma vacina até agora se revelou difícil. Em um novo estudo relatado em
Nature Communications , pesquisadores do Instituto de Ciência Weizmann, junto com colaboradores na Irlanda e Austrália, mostraram que
Plasmodium falciparum é ainda mais tortuoso do que se pensava:não apenas se esconde das defesas imunológicas do corpo, ele emprega uma estratégia ativa para enganar o sistema imunológico. p Entre as doenças transmissíveis, a malária perde apenas para a tuberculose em número de vítimas, colocando em risco quase metade da população da Terra. Mais de 200 milhões de pessoas são infectadas todos os anos; cerca de meio milhão morre, a maioria crianças menores de cinco anos. "A malária é uma das doenças mais devastadoras do mundo - é uma verdadeira desgraça para os países de baixa renda, onde mata mil crianças todos os dias, "diz a Dra. Neta Regev-Rudzki do Departamento de Ciências Biomoleculares de Weizmann." Para combater a malária, precisamos entender a biologia básica de
Plasmodium falciparum e descobrir o que o torna um assassino tão perigoso. "
p Regev-Rudzki havia descoberto anteriormente, em seus estudos de pós-doutorado no laboratório do Prof. Alan Cowman no Walter e Eliza Hall Institute of Medical Research em Melbourne, Austrália, que esses parasitas se comunicam entre si durante o estágio de incubação no sangue. Eles fazem isso liberando nanovesículas em forma de saco - com menos de 1 mícron de diâmetro - que contêm pequenos segmentos do DNA do parasita. Aparentemente, esses sinais ajudam os parasitas a aprender quando é hora de começar a se transformar em formas masculinas e femininas, ambos podem ser transportados por mosquitos para novos hospedeiros. Essa descoberta foi ainda mais surpreendente porque as nanovesículas precisam cruzar seis membranas separadas para comunicar a mensagem de um parasita dentro de um glóbulo vermelho para outro.
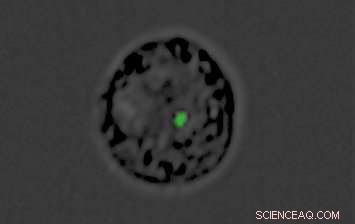 p Monócito convertido em isca pelo parasita da malária:o ponto verde é a "carga" de material genético dentro da nanovesícula produzida pelo parasita. Crédito:Weizmann Institute of Science
p Monócito convertido em isca pelo parasita da malária:o ponto verde é a "carga" de material genético dentro da nanovesícula produzida pelo parasita. Crédito:Weizmann Institute of Science
p No novo estudo, realizado em colaboração com o Prof. Andrew G. Bowie do Trinity College Dublin e outros pesquisadores, Regev-Rudzki e sua equipe Weizmann descobriram que, em paralelo com a comunicação com outros parasitas,
Plasmodium falciparum usa esse mesmo canal de comunicação para outro propósito:enviar uma mensagem enganosa ao sistema imunológico da pessoa infectada. Nas primeiras 12 horas após infectar os glóbulos vermelhos, os parasitas enviam nanovesículas cheias de DNA que penetram nas células chamadas monócitos. Normalmente, monócitos formam a primeira linha de defesa do sistema imunológico contra invasão estrangeira, detectar o perigo de longe e alertar outros mecanismos imunológicos para montar uma resposta eficaz. Naturalmente, o sistema imunológico envia sua próxima linha de defesa para essas células.
p Mas de fato, as nanovesículas converteram os monócitos em iscas. Enquanto o sistema imunológico está ocupado defendendo o organismo contra o perigo falso, a verdadeira infecção prossegue dentro dos glóbulos vermelhos, permitindo que o parasita se multiplique sem obstáculos a uma velocidade estonteante. No momento em que o sistema imunológico descobre seu erro, tempo precioso foi perdido, e a infecção é muito mais difícil de conter.
p A equipe de Regev-Rudzki identificou um sensor molecular chave, uma proteína chamada STING que se torna ativada quando as nanovesículas do parasita penetram nos monócitos. É o STING que envia o alerta falso para o sistema imunológico, enganando-o fazendo-o "pensar" que seus monócitos estão em perigo. Quando os cientistas "eliminaram" o gene que fabrica o STING, a cadeia de reações moleculares que geravam o alerta enganoso foi interrompida.
p "Nós descobrimos uma estratégia subversiva que o parasita da malária emprega para prosperar no sangue humano, "Regev-Rudzki diz." Ao interferir com essa subversão do sistema imunológico, pode ser possível no futuro desenvolver formas de bloquear a infecção malárica. "

